
 ,反应中其还原剂是Na2O2.
,反应中其还原剂是Na2O2.分析 (1)过氧化钠和二氧化碳反应生成碳酸钠和氧气,过氧化钠和水反应生成氢氧化钠和氧气;
(2)碳酸氢钠可与盐酸反应,碳酸钠可与水、二氧化碳反应生成碳酸氢钠;
(3)碳酸氢钠和石灰水反应生成碳酸钙和碳酸钠.
解答 解:(1)反应生成碳酸钠和氧气,反应中O元素的化合价既升高又降低,该反应及转移电子数为 ,反应过氧化钠既是氧化剂也是还原剂,充分反应后固体质量比原增加1.4g,设参加反应的Na2O2的质量为x,则
,反应过氧化钠既是氧化剂也是还原剂,充分反应后固体质量比原增加1.4g,设参加反应的Na2O2的质量为x,则
2Na2O2+2CO2=2Na2CO3+O2 质量差
156g 56
x 1.4g
x=3.9g,
故答案为: ;Na2O2;3.9克
;Na2O2;3.9克
(2)碳酸氢钠可与盐酸反应,离子方程式为HCO3-+H+=CO2↑+H2O,碳酸钠可与水、二氧化碳反应生成碳酸氢钠,反应的离子方程式为CO32-+H2O+CO2═2HCO3-,
故答案为:HCO3-+H+=CO2↑+H2O; CO32-+H2O+CO2═2HCO3-;
(3)碳酸氢钠和石灰水反应生成碳酸钙和碳酸钠,反应的离子方程式为2HCO3-+2OH-+Ca2+═CaCO3↓+H2O+CO32-,故答案为:2HCO3-+2OH-+Ca2+═CaCO3↓+H2O+CO32-.
点评 本题考查较为综合,涉及氧化还原反应以及元素化合物知识,为高频考点,把握反应中元素的化合价为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| 实验一 | 实验二 | |
| 装置 | 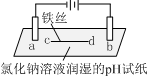 | 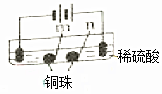 |
| 现象 | a、d处试纸变蓝;b处变红,局部褪色;c处无明显变化 | 两个石墨电极附近有气泡产生;n处有气泡产生;… |
| A. | a、d处:2H2O+2e-=H2↑+2OH- | |
| B. | b处:2Cl--2e-=Cl2↑ | |
| C. | 根据实验一的原理,实验二中m处能析出铜 | |
| D. | n处发生了反应:2H++2e-=H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | ① | ② | ③ | ④ |
| pH | 10 | 10 | 4 | 4 |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
| A. | 相同体积③、④溶液分别与NaOH完全反应,消耗NaOH物质的量:③>④ | |
| B. | 分别加水稀释10倍,四种溶液的pH:①>②>④>③ | |
| C. | ①、④两溶液等体积混合,所得溶液中c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| D. | Va L ④溶液与Vb L ②溶液混合(近似认为混合溶液体积=Va+Vb),若混合后溶液pH=5,则Va:Vb=9:11 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 判断如图装置的名称:B池为电解池(填“原电池”或“电解池”)当C2极析出224mL气体(标准状况)时:锌的质量减少(填“增加”或“减少”).
判断如图装置的名称:B池为电解池(填“原电池”或“电解池”)当C2极析出224mL气体(标准状况)时:锌的质量减少(填“增加”或“减少”).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的核外电子数不同 | |
| B. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的中子数分别为78和80 | |
| C. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的质量数不同,是同种元素 | |
| D. | 关${\;}_{34}^{78}$Se和${\;}_{34}^{80}$Se的质子数相同,是同一种核素 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
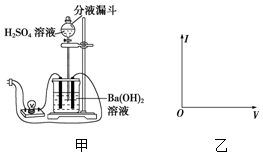 使用中学常用的实验器材,设计一个实验观察Ba(OH)2与H2SO4在溶液中的反应导电性的变化,并回答问题:
使用中学常用的实验器材,设计一个实验观察Ba(OH)2与H2SO4在溶液中的反应导电性的变化,并回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含有等物质的量的Ba(OH)2、KOH的混合溶液中通入CO2,与CO2反应的物质依次是:KOH、Ba(OH)2、BaCO3 | |
| B. | 向含有等物质的量的Fe2+、Ag+、Cu2+的混合溶液中加入Zn,与Zn反应的离子依次是:Ag+、Cu2+、Fe2+ | |
| C. | 向含有等物质的量的AlO2-、OH-、CO32-的混合溶液中滴加盐酸,与盐酸反应的物质依次是:AlO2-、Al(OH)3、OH-、CO32- | |
| D. | 在含有等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气,与氯气反应的离子依次是:I-、Br-、Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
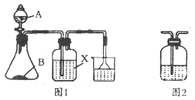 某化学兴趣小组探究二氧化硫和氯气二者的制法和性质,做下列有关实验:
某化学兴趣小组探究二氧化硫和氯气二者的制法和性质,做下列有关实验:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com