
�����������������ͻ�ѧ���ԣ����������������Ǹ�����ҵ����Ҫԭ�ϡ��ʻ����ᴿ�����漰��������Ӧ����Ϊ��
��Ni(s)��4CO(g)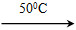 Ni(CO)4(g)��Q
Ni(CO)4(g)��Q
��Ni(CO)4(g)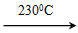 Ni(s)��4CO(g)
Ni(s)��4CO(g)
���������գ�
(1)���¶Ȳ��������£�Ҫ��߷�Ӧ����Ni(CO)4�IJ��ʣ��ɲ�ȡ�Ĵ�ʩ��____________��____________ ��
(2)����Ӧ�ڴﵽƽ����������������䣬�����¶ȣ����´ﵽƽ��ʱ_______________ ��
a��ƽ�ⳣ��K�������� b��CO��Ũ�ȼ�С
c��Ni��������С d��v��[Ni(CO)4]����
(3)�����ʻ����ᴿ�����IJ�������____________________________________________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�״�������ˮ������Ӧ������������Ӧ����ʽ���£�
CH3OH(g)��H2O(g)  CO2(g)��3H2(g)����H>0
CO2(g)��3H2(g)����H>0
(1)һ�������£������Ϊ2 L�ĺ����ܱ������г���1 mol CH3OH(g)��3 mol H2O(g)��20 s��û�������ѹǿ�Ƿ�Ӧǰ��1.2�������ü״���ʾ�÷�Ӧ������Ϊ________��
(2)�ж�(1)�п��淴Ӧ�ﵽƽ��״̬��������(�����)________��
��v��(CH3OH)��v��(CO2)
�ڻ��������ܶȲ���
�ۻ�������ƽ����Է�����������
��CH3OH��H2O��CO2��H2��Ũ�ȶ����ٷ����仯
(3)��ͼ��P�ǿ�����ƽ�л����Ļ������ر�K������ͬ�¶�ʱ����A�����г���1 mol CH3OH(g)��2 mol H2O(g)����B�����г���1.2 mol CH3OH(g)��2.4 mol H2O(g)���������ֱ���������Ӧ����֪��ʼʱ����A��B�������Ϊa L���Իش�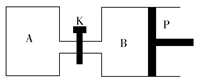
�ٷ�Ӧ�ﵽƽ��ʱ����B�����Ϊ1.5aL������B��CH3OHת����Ϊ________��A��B��������H2O(g)������ٷֺ����Ĵ�С��ϵΪ��B(�>����<������)________A��
������K��һ��ʱ������´ﵽƽ�⣬����B�����Ϊ________L(��ͨ��������������Բ��ƣ��Ҳ������¶ȵ�Ӱ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��������Դ�����ϴ������ǿɳ�����չ����Ҫ���档
��1����̼��������ֱ�Ӻϳ��Ҵ�ȼ���ѽ�����ģ���������ȡ��CO��H2Ϊԭ�Ϻϳ��Ҵ�����ѧ��Ӧ����ʽ��2CO(g)+4H2(g)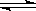 CH3CH2OH(g)+H2O(g)�����ܱ������г���10 mol CO��20mol H2���ڴ��������·�Ӧ�����Ҵ���CO��ת����(��)���¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��
CH3CH2OH(g)+H2O(g)�����ܱ������г���10 mol CO��20mol H2���ڴ��������·�Ӧ�����Ҵ���CO��ת����(��)���¶ȡ�ѹǿ�Ĺ�ϵ����ͼ��ʾ��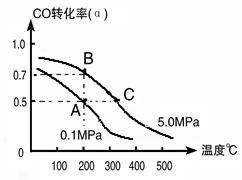
����A��B�����ʾ��ijʱ�̴ﵽ��ƽ��״̬����ʱ��A��ʱ���������Ϊ10L������¶��µ�ƽ�ⳣ����K�� ��
����A��C���㶼��ʾ�ﵽ��ƽ��״̬�����Է�Ӧ��ʼ����ƽ��״̬�����ʱ��tA tC������ڡ�����С�ڡ����ڡ�����
�۹�ҵ�ϻ����Բ�ȡ��CO2��H2Ϊԭ�Ϻϳ��Ҵ������Ҹ�����ѧ�������Ƴ磬��������ͬ�����£���CO��ȡCH3CH2OH��ƽ�ⳣ��ԶԶ������CO2��ȡCH3CH2OH��ƽ�ⳣ�������Ʋ⻯ѧ�������Ͽ���CO2��ȡCH3CH2OH���ŵ���Ҫ�ǣ� ��
��2��Ŀǰ��ҵ��Ҳ������CO2�������״���һ�������·�����ӦCO2(g)��3H2(g) CH3OH(g)��H2O(g)������6mol CO2��8 mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯����������ͼ��ʾ��ʵ�ߣ���
CH3OH(g)��H2O(g)������6mol CO2��8 mol H2����2L���ܱ������У����H2�����ʵ�����ʱ��仯����������ͼ��ʾ��ʵ�ߣ���
�����ڴ����ͼ�л���״������ʵ�����ʱ��仯���ߡ�
�ڽ��ı�ijһʵ�������ٽ�������ʵ�飬���H2�����ʵ�����ʱ��仯��ͼ��������ʾ������I��Ӧ��ʵ�������ı��� �����ߢ��Ӧ��ʵ�������ı��� ��
��3��Hg��ˮ����Ⱦ���ؽ���Ԫ��֮һ��ˮ��Һ�ж��۹�����Ҫ������̬��Cl����OH����Ũ�ȹ�ϵ����ͼ��ʾ��ͼ�е����ʻ�����ֻ��Hg(OH)2Ϊ�����pCl=��1gc(Cl��)��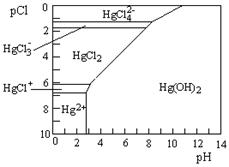
������˵������ȷ���� ��
A��Ϊ�˷�ֹHg2��ˮ�⣬����Hg(NO3)2��ҺʱӦ��Hg(NO3)2��������Ũ�������ϡ��
B����c(C1��) ��10��1 mol��L��1ʱ����Ԫ��һ��ȫ����HgCl42����ʽ����
C��HgCl2��һ��������ʣ�����뷽��ʽ�ǣ�HgCl2��HgCl�� + C1��
D������ҺpH������4��pCl��2�ı���6ʱ����ʹHgCl2ת��ΪHg(OH)2
��HgCl2�ֳơ����������۵�549K���������������侧���� ��������ͣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
25 ��ʱ�������Ϊ2 L���ܱ������У���̬A��B��C�����ʵ���n��ʱ��t�ı仯��ͼ1��ʾ����֪�ﵽƽ������¶ȣ�A��ת���ʽ�����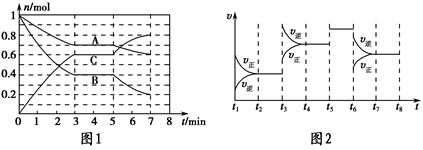
| t2��t3 | t4��t5 | t5��t6 | t7��t8 |
| K1 | K2 | K3 | K4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪��2NO2(g) N2O4(g)����H��0���ں��º��������£���һ����NO2��N2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������У���Ӧ�����и����ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ��ͼ����ʾ����ش�
N2O4(g)����H��0���ں��º��������£���һ����NO2��N2O4�Ļ������ͨ���ݻ�Ϊ2L���ܱ������У���Ӧ�����и����ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ��ͼ����ʾ����ش�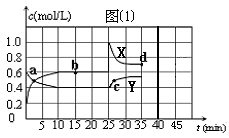
��1��a��ʱ��v(��) v���棩�����������������=������X�ߡ�Y���д���N2O4���� ��
��2����Ӧ�ڵ�10 min�ﵽƽ�⣬��ǰ10 min����N��2��ʾ�Ļ�ѧ��Ӧ����v(N��2)= mol��L-1��min-1�����¶��£���Ӧ��ƽ�ⳣ��K= (���÷�����ʾ)��
��3���ڵ�25���ӣ����еIJ����� ��
��4��a��b��c��d�ĵ��Ӧ��ʱ�̣�NO2���ʵ���Ũ����С�����˳���� ���ٴ�ƽ��ʱ��d��NO2�����������b��ʱ �������С������ȡ�����
��5�������ڵ�35���Ӵ���������ȥ0.4mol N2O4���������ʵ�����ʹ��Ӧ�ڵ�40���Ӵﵽƽ�⣬����ͼ���л����ӵ�35�����Ժ��������ʵ����ʵ���Ũ��c��ʱ��t�ı仯��ϵ������ע����������Ӧ�����ʡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ˮú��ת���ɺϳ�����Ȼ��ϳɸ�����Ʒ��ʯ����Ʒ�ǻ����ļ�Ϊ��Ҫ������ȥˮ�������ˮú����Ҫ��H2��CO��CO2��������H2S��CH4��������ȥH2S�ɲ��ô���Ǵ�ת����������CH4ת����CO���õ�CO��CO2��H2�Ļ�����壬������ĺϳɼ״�ԭ������
(1)��ˮú������Ҫ��ѧ��Ӧ����ʽΪ��C(s)+H2O(g) CO(g)+H2(g)���˷�Ӧ�����ȷ�Ӧ��
CO(g)+H2(g)���˷�Ӧ�����ȷ�Ӧ��
�ٴ˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ ��
������������̼��ת���ʵĴ�ʩ�� ��
| A������C(s) | B������H2O(g) | C�������¶� | D������ѹǿ |
 CO(g)+2H2O(g) ��H="-519" kJ/mol����ҵ��Ҫѡ����ʵĴ������ֱ��X��Y��Z���ִ�����������ʵ��(����������ͬ)
CO(g)+2H2O(g) ��H="-519" kJ/mol����ҵ��Ҫѡ����ʵĴ������ֱ��X��Y��Z���ִ�����������ʵ��(����������ͬ)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��10 L���ܱ������У��������»�ѧ��Ӧ��CO2��g����H2��g�� CO��g����H2O��g���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO��g����H2O��g���仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
| t/�� | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��֪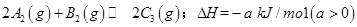 ����һ���д����Ĺ̶��ݻ��������м���2mol
����һ���д����Ĺ̶��ݻ��������м���2mol 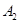 ��1mol
��1mol 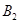 ����500��ʱ��ַ�Ӧ��ƽ���
����500��ʱ��ַ�Ӧ��ƽ���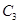 ��Ũ��Ϊw mol/L���ų�����b kJ��
��Ũ��Ϊw mol/L���ų�����b kJ��
��1���Ƚ�a______b�������������
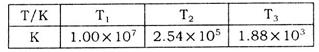
��2���±�Ϊ��ͬ�¶��¸÷�Ӧ��ƽ�ⳣ�����ɴ˿���֪������ ���������������������
���������������������
����ԭ���������У�ֻ����2mol 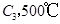 ʱ��ַ�Ӧ��ƽ�����������ckJ��
ʱ��ַ�Ӧ��ƽ�����������ckJ��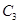 ��Ũ��________�������������w mol/L��
��Ũ��________�������������w mol/L��
��3������ͬ������Ҫ��õ�2akJ��������������ʵ����ʵ���������
A��4mol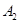 ��2mol
��2mol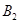 B��4mol
B��4mol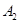 ��2mol
��2mol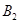 ��2mol
��2mol 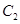
C��4mol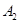 ��4mol
��4mol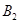 D��6mol
D��6mol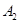 ��4mol
��4mol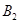
��4��Ϊʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����___________��
A����ʱ�����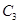 ���� B���ʵ������¶�
���� B���ʵ������¶�
C������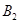 ��Ũ�� D��ѡ���Ч�Ĵ���
��Ũ�� D��ѡ���Ч�Ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
| �� �ȣ��棩 | 360 | 440 | 520 |
| Kֵ | 0.036 | 0.010 | 0.0038 |
 CO(g) + 3H2(g) ��ȡ����֪�÷�Ӧ�У�����ʼ������е�
CO(g) + 3H2(g) ��ȡ����֪�÷�Ӧ�У�����ʼ������е�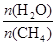 �㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ������ͼ��ʾ��
�㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ������ͼ��ʾ��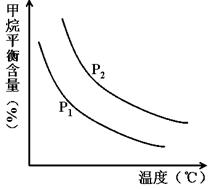
 CO2 (g) + H2(g) ��ȡ��
CO2 (g) + H2(g) ��ȡ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com