
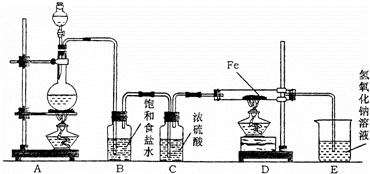
某研究性学习小组设计如图装置制取氯气并以氯气为原料进行实验.
(1)装置A烧瓶中发生反应的化学方程式为 ;
(2)装置B中饱和食盐水的作用是 ,装置C中浓硫酸的作用是 ;
(3)实验时,先点燃A处的酒精灯,再点燃D处酒精灯,写出D中反应的化学方程式 ,写出E中反应的离子方程式 ;
(4)若实验中用12mol•L﹣1浓盐酸10mL与足量的MnO2反应,生成Cl2的物质的量总是小于0.03mol,试分析可能存在的原因是:① ,② .
欲使反应生成Cl2的物质的量最大程度的接近0.03mol,则在装置气密性良好的前提下实验中应采取的措施是 .
考点: 氯气的实验室制法;氯气的化学性质.
专题: 实验题.
分析: (1)浓盐酸和二氧化锰在加热条件下反应生成氯化锰、氯气和水,注意稀盐酸和二氧化锰不反应;
(2)根据氯化氢和氯气的性质分析选用除杂试剂;浓硫酸常常干燥能和碱反应气体;
(3)先生成氯气充满装置后再加热D处铁和氯气发生反应,氯气有强氧化性,能把二价铁离子氧化为三价铁离子,尾气吸收需要用氢氧化钠溶液吸收氯气;
(4)反应过程中浓盐酸是易挥发性酸,随反应进行盐酸浓度减小,稀盐酸和二氧化锰不能生成氯气;反应过程中尽可能减少反应为损失,缓慢加热减少氯化氢的挥发;
解答: 解:(1)浓盐酸和二氧化锰在加热条件下反应生成氯化锰、氯气和水MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
,注意稀盐酸和二氧化锰不反应.
故答案为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)制取的氯气中混有氯化氢气体和水蒸气,氯化氢极易溶于水,氯气也能溶于水,所以不能用水除去氯化氢气体;氯气和 水反应生成盐酸和次氯酸,食盐水中含有氯离子,能抑制氯气的溶解,所以要想除去氯气中的氯化氢应饱和食盐水;浓硫酸常常干燥能和碱反应气体,故选浓硫酸.
故答案为:除去HCl;吸收水蒸气;
(3)实验开始需要先生成氯气充满装置后,再加热D处铁和氯气发生反应,氯气有强氧化性,和铁反应生成氯化铁,反应的化学方程式为:2Fe+3Cl2=2FeCl3;尾气吸收需要用氢氧化钠溶液吸收氯气,反应的离子方程式为,Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;
故答案为:A;D;2Fe+3Cl2=2FeCl3; Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;
(4)反应过程中浓盐酸是易挥发性酸,随反应进行盐酸浓度减小,稀盐酸和二氧化锰不能生成氯气;若实验中用12mol•L﹣1浓盐酸10mL与足量的MnO2反应,生成Cl2的物质的量总是小于0.03mol,原因是HCl挥发,浓盐酸变稀不再反应;欲使反应生成Cl2的物质的量最大程度的接近0.03mol,反应过程中尽可能减少反应为损失,缓慢加热减少氯化氢的挥发;
故答案为:HCl挥发,浓盐酸变稀不再反应;慢慢滴加浓盐酸,缓缓加热;
点评: 本题考查了氯气的实验室制法及化学性质,难度不大,氯气的氧化性、二价铁离子和三价铁离子的检验是2015届高考的热点,注意方向反应过程的量的变化,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式是()
A. 浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑
B. 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+
C. NaHCO3溶液与稀H2SO4反应:CO32﹣+2H+═H2O+CO2↑
D. 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质:①O2②三氯甲烷③CH3CH2CH2OH④O3⑤CHCl3 CH3OCH2CH3⑦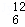 C ⑧CH3CH(OH)CH3⑨
C ⑧CH3CH(OH)CH3⑨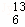 C ⑩CH3OH.
C ⑩CH3OH.
其中属于同系物的有 (填序号,下同),
互为同分异构体的有 ,
互为同素异形体的有 ,
属于同位素的有 ,
是同一种物质的有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式的是()
A. 硫酸铝溶液中加入过量氨水:Al3++3OH﹣═Al(OH)3↓
B. 碳酸钠溶液中加入澄清石灰水:Ca(OH)2+CO32﹣═CaCO3↓+2OH﹣
C. 冷的氢氧化钠溶液中通入氯气:Cl2+2OH﹣═ClO﹣+Cl﹣+H2O
D. 稀硫酸中加入铁粉:2Fe+6H+═2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于过氧化钠的叙述正确的是()
A. 过氧化钠能与酸反应生成盐和水,所以过氧化钠是碱性氧化物
B. 可用Na2O2除去N2中的水蒸气
C. 过氧化钠与水反应时,过氧化钠是氧化剂,水是还原剂
D. 过氧化钠与二氧化碳反应时,过氧化钠既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
物质制备过程中离不开物质的提纯.以下除杂方法不正确的是()
选项 目的 实验方法
A 除去Na2CO3固体中的NaHCO3 置于坩埚中加热至恒重
B 除去NaCl中少量KNO3 将混合物制成热饱和溶液,冷却结晶,过滤
C 除去CO2中的HCl气体 通过NaHCO3(aq,饱和),然后干燥
D 除去C2H5Br中的Br2 加入足量Na2SO3(aq),充分振荡,分液
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
①2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O
②K2Cr2O7+6FeSO4+7H2SO4=3Fe2(SO4)3+K2SO4+7H2O
③Fe2(SO4)3+2HI=2FeSO4+I2+H2SO4
下列结论正确的是()
A. ①②③均是氧化还原反应
B. 氧化性强弱顺序是K2Cr2O7>Fe2(SO4)3>I2
C. 反应②中氧化剂与还原剂的物质的量之比为6:1
D. 反应③中0.1mol还原剂共失去电子数为6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
对一份稀溶液作初步分析发现,溶液无色、澄清,其中可能含有SO42﹣、Na+、CO32﹣、H+、NO3﹣、NH4+、Cl﹣ 等离子中的若干种.然后又做了如下实验,以确认这些离子是否大量存在.
①用pH试纸测溶液的pH,试纸显红色;
②取2毫升溶液,用氯化钡和稀硝酸进行检验,结果生成了白色沉淀;
③对②中所得混合物充分静置后,取上层清夜用硝酸银溶液和稀硝酸检验,结果又生成了白色沉淀;
④另取2毫升溶液,加入足量氢氧化钠溶液并加热,没有产生能使湿润红色石蕊试纸变蓝的气体.
试回答下述问题:
(1)原溶液中一定存在的离子是
(2)原溶液中一定不存在的离子是
(3)按上述操作,原溶液中还不能肯定是否存在的阳离子是Na+检验该阳离子方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取NaCl质量分别是()
A. 950mL,111.2g B. 500mL,117g
C. 1000mL,117g D. 1000mL,111.2g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com