
| A�� | �ŵ�ʱ������6mol���ӷ���ת�ƣ�����2mol K2FeO4������ | |
| B�� | �ŵ�ʱ��������ӦΪ��FeO42-+4H2O+3e-�TFe��OH��3+5OH- | |
| C�� | ���ʱ����صĸ�������ӵ�Դ���������� | |
| D�� | ���ʱ������������Һ��pH��С |
���� ���ݵ�ط�Ӧʽ֪��ZnԪ�ػ��ϼ���0�۱�Ϊ+2�ۣ�����Zn���������ŵ�ʱ��������ӦʽΪZn+2OH--2e-�TZn��OH��2��������ӦʽΪFeO42-+4H2O+3e-=Fe��OH��3+5OH-�����ʱ�����������缫��Ӧʽ���������缫��Ӧʽ�����෴���ŵ�ʱ������������������������෴���ݴ˷������
��� �⣺A���ŵ�ʱ�������ϵ缫��ӦʽΪFeO42-+4H2O+3e-=Fe��OH��3+5OH-������6mol���ӷ���ת�ƣ�����2mol K2FeO4����ԭ����A����
B��������FeO42-�õ��ӷ�����ԭ��Ӧ�������ĵ缫��ӦʽΪFeO42-+4H2O+3e-=Fe��OH��3+5OH-����B��ȷ��
C�����ʱ����صĸ�������ӵ�Դ�ĸ�����������C����
D�����ʱ�������ϵ缫��ӦʽΪZn��OH��2+2e-=Zn+2OH-��������������Һ��pH���D����
��ѡB��
���� ���⿼����ԭ��غ͵���ԭ��������Ԫ�ػ��ϼ����ص缫�Ĺ�ϵ�ǽⱾ��ؼ�����д�缫��Ӧʽ��ѧϰ�ѵ㣬Ҳ�ǿ����ȵ㣬Ҫ����������д��������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʯ��-Ca��OH��2 | B�� | �ؾ�ʯ-BaCO3 | C�� | �̷�-CuSO4•5H2O | D�� | С�մ�-NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=13����Һ�У�Fe3+��NH4+��NO3-��CO32- | |
| B�� | c��OH-��=0.1mol•L-1����Һ�У�K+��Ba2+��NO3-��Cl- | |
| C�� | 0.1mol•L-1��NaAlO2��Һ�У�Na+��Al3+��HCO3-��SO42- | |
| D�� | pH=1����Һ�У�K+��Fe2+��Cl-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
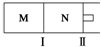 M��N���������о�������Ӧ��A��g��+3B��g��?2C��g����H=-192kJ•mol-1�������̶�������������������ƶ�����M��N�У���ͨ��x mol A��y mol B�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䣮����˵����ȷ���ǣ�������
M��N���������о�������Ӧ��A��g��+3B��g��?2C��g����H=-192kJ•mol-1�������̶�������������������ƶ�����M��N�У���ͨ��x mol A��y mol B�Ļ�����壬��ʼM��N�ݻ���ͬ�������¶Ȳ��䣮����˵����ȷ���ǣ�������| A�� | ��x��y=1��2����ƽ��ʱ��M�е�ת���ʣ�A��B | |
| B�� | ��x��y=1��3����M�зų�����172.8 kJʱ��A��ת����Ϊ90% | |
| C�� | ��x=1.2��y=1��N�дﵽƽ��ʱ���Ϊ2 L������C 0.4 mol����ͨ��0.4mol Aʱ��v����v�� | |
| D�� | ��ʼʱ���ֱ���M��N���������м���1molA��1molC���ﵽƽ��ʱ������M��N������A�����������M��N |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ֽ�����һ���й㷺Ӧ�õġ�����ء�����ͼ���ּ���ֽ��ز��ñ���ֽƬ��Ϊ����ʹ����壬ֽ������ֱ���п�Ͷ������̣������йظ�ֽ���˵�����������ǣ�������
ֽ�����һ���й㷺Ӧ�õġ�����ء�����ͼ���ּ���ֽ��ز��ñ���ֽƬ��Ϊ����ʹ����壬ֽ������ֱ���п�Ͷ������̣������йظ�ֽ���˵�����������ǣ�������| A�� | ZnΪ����������������Ӧ | |
| B�� | ��ع���ʱ��������MnO2����Zn | |
| C�� | ������Ӧ��MnO2+e-+H2O�TMnO��OH��+OH- | |
| D�� | ����ܷ�Ӧ��Zn+2MnO2+2H2O�TZn��OH��2+2MnO��OH�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ࡢ��֬���������������ڷ���������Ӧ���վ�ֻ�õ�CO2��H2O | |
| B�� | ��������Һ�л���������NaCl���ɼ���������Һ����˳�ȥ���� | |
| C�� | ��ʳƷ��װ���ڷ���С��װ����ʯ�Һ����ۿ��Է�ֹʳƷ�ܳ��ͱ��� | |
| D�� | װ�����绯�˵�̺�����ϰ塢����ʯ�Ⱦ����ͷų���Ⱦ�����ļ�ȩ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ���ǰCuSO4��Һ�����ʵ���Ũ��Ϊ2 mol/L | |
| B�� | ����������Һ��c��H+��=2 mol/L | |
| C�� | ��n��e-��=0.6 molʱ��V��H2����V��O2��=3��2 | |
| D�� | ��������Һ���Ⱥ����16 g CuO��3.6gˮ������Һ�ɻָ�Ϊ���ǰ��Ũ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �����ҳص��Һ���� AgNO3 ��Һ�������ʵ����ʯī���϶��� | |
| B�� | �׳�ͨ�� CH3OH �ĵ缫��ӦʽΪ CH3OH+6e-+2H2O�TCO32-+8H+ | |
| C�� | ��Ӧһ��ʱ������ҳ��м���һ���� Cu��OH��2 ���壬��ʹ CuSO4��Һ�ָ��� ԭŨ�� | |
| D�� | �׳������� 224mL����״���£�O2����ʱ�����������ϲ��� 1.16g ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com