
����Ŀ�������ǻ����л�����ԭ��֮һ���㷺����ũҩ��Ƥ�Ⱦ�ϡ�ҽҩ���ȹ�ҵ��
(1)��ҵ�����ü����������ϵת��ͼ��ͼ��
��Ӧ![]() ���ʱ�
���ʱ�![]() ________
________![]() ��
��
(2)ij��ѧС���о���ͬѹǿ�����Է�Ӧ![]() ��Ӱ�졣
��Ӱ�졣![]() �£���һ���ݻ��ɱ���ܱ������У�����һ������
�£���һ���ݻ��ɱ���ܱ������У�����һ������![]() ��
��![]() ����ò�ͬѹǿ�£�ƽ��ʱ�����������Ũ�����±���
����ò�ͬѹǿ�£�ƽ��ʱ�����������Ũ�����±���
������ | ��Ӧѹǿ | ����Ũ�� | ||
|
|
| ||
1 |
| 0.3 | 0.3 | 0.9 |
2 |
|
|
| 0.4 |
3 |
| 0.4 | 0.4 |
|
�Իش��������⣺
��ƽ��ʱ��ʵ��1������Ӧ����________(����>������<������=��)ʵ��3���淴Ӧ���ʡ�
����ʵ��1�����ݿɼ���![]() ʱ���÷�Ӧ��ƽ�ⳣ��
ʱ���÷�Ӧ��ƽ�ⳣ��![]() ________��
________��
��![]() ________
________![]() ��
��
(3)���о����ֲ��õ绹ԭ��Ҳ�ɽ�![]() ת��Ϊ�������ͬʱ�������
ת��Ϊ�������ͬʱ�������![]() ��ת��Ч�ʡ�����ԭ����ͼ��ʾ������������ȷ����________��
��ת��Ч�ʡ�����ԭ����ͼ��ʾ������������ȷ����________��

A.![]() ���ĵ缫��ӦʽΪ
���ĵ缫��ӦʽΪ![]()
B.��������![]() ��
��![]() ���ƶ�
���ƶ�
C.![]() ��������ԭ��Ӧ���������ݳ�
��������ԭ��Ӧ���������ݳ�
D.��������![]() Ũ����С
Ũ����С
(4)�������;֮һ������������������Һ������������Һ�м���������ǿ��ʴ���Һ��![]() �仯�����ܱ�����Һ
�仯�����ܱ�����Һ![]() ����ȶ���(��֪����ĵ���ƽ�ⳣ��
����ȶ���(��֪����ĵ���ƽ�ⳣ��![]() )
)
���ֽ���Ũ�ȼ������������Һ��ϣ����![]() ��
��![]() ������Һ�������ӷ���ʽ��ʾ������ǿ�����
������Һ�������ӷ���ʽ��ʾ������ǿ�����![]() ������Һ�У�
������Һ�У�![]() �仯�����ԭ����________��
�仯�����ԭ����________��
������![]() ��Һ����
��Һ����![]() Ϊ4�Ļ�����Һ�������________
Ϊ4�Ļ�����Һ�������________![]() (�𰸱���һλС��)
(�𰸱���һλС��)![]() ��Һ��
��Һ��
���𰸡�+31.4 �� 10 0.2 AD HCOOH+OH-=HCOO-+H2O 642.9
��������
���ݸ�˹���ɣ������Ӧ�ȣ�������������ƽ��ʱʵ��3��ƽ��Ũ�ȴ���ʵ��1��ƽ��Ũ�ȣ��жϷ�Ӧ���ʴ�С����������ʵ��1���ݣ�����ƽ�ⳣ��Kֵ�������¶Ȳ��䣬Kֵ�������ʵ��2�е�a�����ݻ�����Һ��ԭ�����ͼ�������NaOH������кͣ�pH�仯�����ݻ�����Һ����ԭ���������NaOH�������
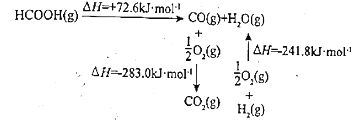
(1)��ͼʾ��֪��HCOOH(g)CO (g)+H2O(g)��H=+72.6kJ/mol����CO(g)+ ![]() O2(g)=CO2(g)��H=-283.0kJ/mol����H2(g)+
O2(g)=CO2(g)��H=-283.0kJ/mol����H2(g)+![]() O2(g)=H2O(g)��H=-241.8kJ/mol�����ø�˹���ɣ�����+��-�ۿɵ�HCOOH(g)CO2(g)+H2(g)���ʱ���H=��+72.6kJ/mol��+��-283.0kJ/mol��-��-241.8kJ/mol��=+31.4kJ/mol����Ϊ+31.4��
O2(g)=H2O(g)��H=-241.8kJ/mol�����ø�˹���ɣ�����+��-�ۿɵ�HCOOH(g)CO2(g)+H2(g)���ʱ���H=��+72.6kJ/mol��+��-283.0kJ/mol��-��-241.8kJ/mol��=+31.4kJ/mol����Ϊ+31.4��
(2)��ʵ��1��2��3���ں��º�ѹ�½��У��ɱ������ݿ�֪ʵ��3ƽ��Ũ�ȱ�ʵ��1�Ĵ���ѹǿ�ϴ�Ӧ���ʽϴ�ƽ��ʱ��ʵ��1������Ӧ����С��ʵ��3���淴Ӧ���ʣ���Ϊ����
����![]() ��H=-31.4 kJ/mol��֪��ƽ�ⳣ��K=
��H=-31.4 kJ/mol��֪��ƽ�ⳣ��K= ![]() ������ʵ��1�����ݼ�K=
������ʵ��1�����ݼ�K=![]() =10����Ϊ10��
=10����Ϊ10��
�۷�Ӧ����ͬ�¶��½��У�ƽ�ⳣ��K���䣬��K=10����֪K=![]() =
=![]() =10�����a=0.2����Ϊ0.2��
=10�����a=0.2����Ϊ0.2��
(3)A��Sn���Դ����������Sn��Ϊ������CO2�õ����ӷ�����ԭ��Ӧת��ΪHCOO-���缫��ӦΪCO2+2e-+HCO3-=HCOO-+CO32-����A��ȷ��
B�����������������������ƶ�����K+�������ƶ�������Sn���ƶ�����B����
C��Pt��Ϊ������ʧȥ���ӣ�����������Ӧ��2H2O-4e-=4H++O2������O2�ݳ�����C����
D�����������缫��ӦCO2+2e-+HCO3-=HCOO-+CO32-��֪����������HCO3-Ũ����С����D��ȷ��
��ΪAD��
(4)�ٽ�����ǿ�����HCOOH-HCOONa������Һ�У�HCOOH����NaOH��Ӧ������pH�仯�������ӷ���ʽΪHCOOH+OH-=HCOO-+H2O����Ϊ��HCOOH+OH-=HCOO-+H2O��
������100mL2molL-1HCOOH��Һ����pHΪ4��c(H+)=10-4mol/L�Ļ�����Һ������HCOOH![]() HCOO-+H+��֪��Ka=
HCOO-+H+��֪��Ka=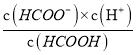 =
=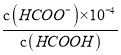 =1.8��10-4���ó�c(HCOO-)=1.8c(HCOOH)��ԭ��Һ��n(HCOOH)=0.2mol�������NaOH�����ʵ���Ϊx����ΪNaOH��HCOOH����HCOOH+NaOH=HCOONa+H2O��֪��n(NaOH)=n(HCOO-
=1.8��10-4���ó�c(HCOO-)=1.8c(HCOOH)��ԭ��Һ��n(HCOOH)=0.2mol�������NaOH�����ʵ���Ϊx����ΪNaOH��HCOOH����HCOOH+NaOH=HCOONa+H2O��֪��n(NaOH)=n(HCOO-![]() =
=![]() =0.6429L=642.9mL����Ϊ642.9��
=0.6429L=642.9mL����Ϊ642.9��


 ��ʦ�㲦��ϵ�д�
��ʦ�㲦��ϵ�д� Ӣ�żƻ���ĩ����ϵ�д�
Ӣ�żƻ���ĩ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ľṹ��ʽ��ͼ a�����������������
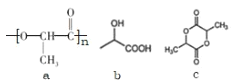
A.b �Ǻϳɾ�����ĵ���
B.1mol �����������Ʒ�Ӧ������ 2mol ����
C.n mol ������������ͼ a �ṹ��ͬʱ���� n molH2O
D.c ���ڻ�����1molc ˮ������ 2molNaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ÿ��������������ߵ��Ƴ����綯������Ϊ����������³�������˹��ȫ�綯����ʹ�õ��������(LiCoO2)��أ��乤��ԭ����ͼ��ʾ������ A �������ǽ���﮺�̼�ĸ��ϲ���(̼��Ϊ����﮵�����)�������Ϊһ���ܴ��� Li���ĸ߷��Ӳ��ϣ���Ĥֻ���ض�������ͨ������ط�ӦʽΪ��LixC6��Li1��xCoO2![]() C6��LiCoO2������˵������ȷ���ǣ� ��
C6��LiCoO2������˵������ȷ���ǣ� ��
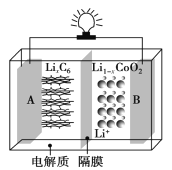
A. �ø�Ĥֻ���� Li��ͨ�����ŵ�ʱ Li������������ұ�
B. �ŵ�ʱ������﮵Ļ��ϼ�δ�����ı�
C. ���ʱ B ���������õ缫�ŵ�ʱ�ĵ缫��ӦʽΪ Li1��xCoO2��xLi����xe��=LiCoO2
D. �Ͼ������(LiCoO2)��ؽ������ŵ紦������ Li������ʯī�ж������ڻ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ж�����Ԫ��X��Y��Z��M��X��Yλ��ͬ���壬Z��Mλ��ͬ���壬Y��Zλ��ͬ���ڣ�X��Z��M������ͬһ���ڣ�Z�ĺ˵������M��2��������˵����ȷ����
A.�������ӵ������ԣ�![]()
B.��̬�⻯��ķе㣺![]()
C.X��Z��M�����ܴ���ͬһ���ӻ�������
D.Y2Z����Һ��c(Y+):c(Z2��) > 2��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��![]() ��
��![]() �������£���ijŨ�ȵ�������Һ�еμ�����������Һ��������Һ��
�������£���ijŨ�ȵ�������Һ�еμ�����������Һ��������Һ��![]() ��
��![]() �仯��ͼ��ʾ������˵����ȷ����( )
�仯��ͼ��ʾ������˵����ȷ����( )

A.������![]() ��Һ��Ũ�����
��Һ��Ũ�����
B.![]() ���
���![]() ��ˮ�ĵ���̶���ͬ
��ˮ�ĵ���̶���ͬ
C.�μ�![]() ��Һ��Ϊ��ˮϡ�ͣ���ͼ���߲���
��Һ��Ϊ��ˮϡ�ͣ���ͼ���߲���
D.�����¶ȣ��ζ�������pH+pOH��14
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Դ�����þ��й���ǰ����
(1)���в����ں�ˮ�����ķ���________(�����)��
A������ B�����ӽ�����
C�����˷� D����������
(2)��ͼ�ǴӺ�ˮ����ȡþ�ļ����̡�
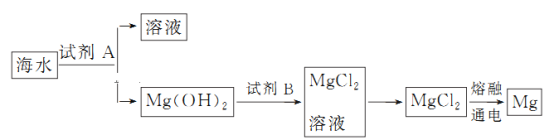
���Լ�B��________(�ѧʽ)��
������ˮMgCl2��ȡMg�Ļ�ѧ����ʽ��__________________________________________
(3)�������и�����I����ʽ���ڵĵ�Ԫ�ء�ʵ������ȡI2��;��������ʾ��
����![]() ������
������![]() ����������Һ
����������Һ![]() ��I����Һ
��I����Һ![]() ��I2ˮ��Һ
��I2ˮ��Һ![]() ��I2����Һ
��I2����Һ![]() ����I2
����I2
��.���в����ڲ������������õ�������________(�����)��
A���ƾ��� B��©��
C������ D��������
��.��������ʵ�����������________��
��.�ܲ��跴Ӧ�����ӷ���ʽ____________________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��������ʵ������������
A. ����������ͨ��CuSO4��Һ�пɵ�����ɫ��Һ
B. ����������ˮ���÷�ɢϵ�ɲ��������ЧӦ
C. ��������Һ��ϡ���ᷴӦ�����ɹ��ὺ��
D. ����������������ȼ�տ������Ȼ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����±�ΪԪ�����ڱ���һ���֣�����X��Y��Z��WΪ������Ԫ�أ�WԪ�صĺ˵����ΪXԪ�ص�2��������˵����ȷ���ǣ� ��

A. X��W��ZԪ�ص�ԭ�Ӱ뾶�����ǵ���̬�⻯������ȶ��Ծ����ε���
B. Y��Z��WԪ������Ȼ���о�����������̬���ڣ����ǵ�����������ˮ������������ε���
C. YX2�����ۻ���Һ̬WX3��������˷����Ӽ�������
D. ����Ԫ�������ɣ������Ʋ�TԪ�صĵ��ʾ��а뵼�����ԣ�T2X3���������Ժͻ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���ҳ����������������Ϊ36.5%���ܶ�Ϊ1.20 g��mL��1��
��1����Ũ������HCl�����ʵ���Ũ����________��
��2������100 mL��Ũ���ᣬ��Ҫ��״����HCl�����Ϊ________��
��3������100 mL 3.00 mol��L��1�����ᣬ������Ũ��������Ϊ________��
��4����10.0 mL 3.00 mol��L��1��������10.0 mL 1.00 mol��L��1��MgCl2��Һ��ϣ�������Һ��Cl�������ʵ���Ũ����________��(���Ϻ���Һ���������)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com