
| ГСЕэЮя | ПЊЪМГСЕэЪБЕФpH | ГСЕэЭъШЋЪБЕФpH |
| Mg(OH)2 | 9.6 | 11.1 |
| Fe(OH)3 | 2.7 | 3.7 |
| ЪЕбщВйзї | дЄЦкЯжЯѓКЭНсТл |
| ВНжш1ЃК | |
| ВНжш2ЃК | |
| ВНжш3ЃК | |
| ЁЁ | |
| ЪЕбщВйзї | дЄЦкЯжЯѓКЭНсТл |
| ВНжш1ЃКШЁЩйСПНўШЁвКгкЪдЙмAжаЃЌж№ЕЮЕЮМг0.1 molЁЄLЃ1 NaOHШмвКЃЌГфЗжеёЕДЃЌБпЕЮМгБпгУpHЪджНМьВтШмвКжБжСpHдк4ЁЋ9ЃЌОВжУ | гаКьКжЩЋГСЕэВњЩњЃЌЫЕУїНўШЁвКжаКЌFe3ЃЋ |
| ВНжш2ЃКгУЕЮЙмНЋЪдЙмAжаЩЯВуЧхвКзЊвЦжСЪдЙмBЃЌЯђЪдЙмBжаЕЮМгЙ§СП6 molЁЄLЃ1 NaOHШмвКЃЌГфЗжеёЕДЃЌОВжУ | гаАзЩЋГСЕэВњЩњЃЌЫЕУїНўШЁвКжаКЌMg2ЃЋ |
| ВНжш3ЃКСэШЁЩйСПНўШЁвКгкЪдЙмCжаЃЌЕЮМгЙ§СП6 molЁЄLЃ1 NaOHШмвКЃЌГфЗжеёЕДЃЌОВжУ | гаГСЕэВњЩњ |
| ВНжш4ЃКгУЕЮЙмНЋЪдЙмCжаЩЯВуЧхвКзЊвЦжСЪдЙмDЃЌЯђЪдЙмDжаж№ЕЮЕЮМг0.1 molЁЄLЃ1 HClжСзуСПЃЌБпЕЮБпеёЕД | гаАзЩЋГСЕэВњЩњШЛКѓГСЕэгжШмНтЃЌЫЕУїНўШЁвКжаКЌAl3ЃЋ |


 ЖсЙкН№ОэШЋФмСЗПМЯЕСаД№АИ
ЖсЙкН№ОэШЋФмСЗПМЯЕСаД№АИ
| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| AЃЎKSCN | BЃЎNaOH | CЃЎHCl | DЃЎBaCl2 |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЬюПеЬт
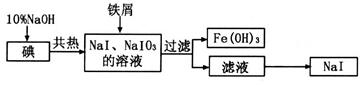
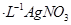 ШмвКЕЮЖЈжСжеЕуЃЌЯћКФ
ШмвКЕЮЖЈжСжеЕуЃЌЯћКФ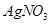 ШмвКЬхЛ§ЕФЦНОљжЕЮЊ19ЃЎ00mLЁЃ
ШмвКЬхЛ§ЕФЦНОљжЕЮЊ19ЃЎ00mLЁЃВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| ЮяжЪ | ЗжзгЪН | ШлЕуЃЈЁцЃЉ | ЗаЕуЃЈЁцЃЉ | УмЖШЃЈg/cm3ЃЉ | ЫЎШмад |
| Мз | C3H6O2 | Ѓ98 | 55ЃЎ5 | 0ЃЎ93 | ПЩШм |
| вв | C4H8O2 | Ѓ84 | 87 | 0ЃЎ90 | ПЩШм |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
| | ВйзїКЭЯжЯѓ | НсТл |
| A | ЯђДПМюжаЕЮМгзуСПХЈбЮЫсЃЌНЋЫљЕУЦјЬхЭЈШыБНЗгФЦШмвКжаЃЌШмвКБфЛызЧ | ЫсадЃКбЮЫс>ЬМЫс>БНЗг |
| B | ШЁФГШмвКЩйСПЃЌМгШыОбЮЫсЫсЛЏЕФBaCl2ШмвКЃЌГіЯжАзЩЋГСЕэ | ИУШмвКжавЛЖЈКЌгаДѓСПЕФSO42ЁЊ |
| C | ШЁЩйСПFe(NO3)2ЪдбљМгЫЎШмНтКѓМгЯЁH2SO4ЫсЛЏЃЌЕЮМгKSCNШмвКЃЌШмвКБфЮЊКьЩЋ | ИУFe(NO3)2ЪдбљвбОБфжЪ |
| D | ШЁдэЛЏЗДгІКѓЕФЛьКЯвКЕЮШыЪЂЫЎЕФЩеБжаЃЌдквКЬхБэУцГіЯжгЭЕЮ | дэЛЏЗДгІВЛЭъШЋ |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЕЅбЁЬт
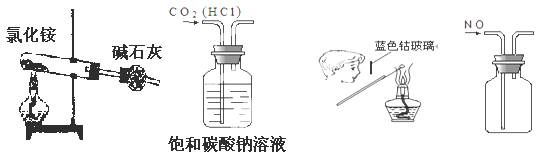
| AЃЎЪЕбщЪвжЦNH3 | BЃЎГ§ШЅCO2жаЕФHCl | CЃЎМьбщK2CO3жаЕФKЃЋ | DЃЎЪеМЏNO |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЪЕбщЬт
 CH3CH2Br+H2O
CH3CH2Br+H2O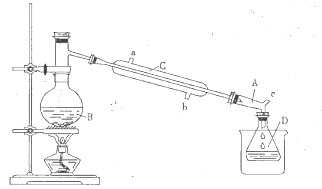
| ЮяжЪ | ЯрЖдЗжзгжЪСП | ЗаЕу/Ёц | УмЖШ/g/cm3 | ЫЎШмад |
| CH3CH2OH | 46 | 78.4 | 0.79 | ЛЅШм |
| CH3CH2Br | 109 | 38.4 | 1.42 | ФбШм |
| CH3CH2OCH2CH3 | 74 | 34.5 | 0.71 | ЮЂШм |
| CH2=CH2 | 28 | -103.7 | 0.38 | ВЛШм |
| ХЈСђЫсЃЈH2SO4ЃЉ | 98 | 338.0 | 1.38 | взШм |
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃКВЛЯъ ЬтаЭЃКЪЕбщЬт
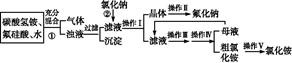
 ЁЁЁЁNH4F+ ЁЁЁЁH2SiO3Ё§+ЁЁЁЁCO2Ёќ+ЁЁЁЁЁЁЁЁ
ЁЁЁЁNH4F+ ЁЁЁЁH2SiO3Ё§+ЁЁЁЁCO2Ёќ+ЁЁЁЁЁЁЁЁ ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com