
| A. | C3H8 | B. | CH4 | C. | C2H6 | D. | C4H10 |
分析 混合气体22.4L,物质的量为$\frac{22.4L}{22.4L/mol}$=1mol,n(CO2)=$\frac{121g}{44g/mol}$=2.75g,n(H2O)=$\frac{40.5g}{18g/mol}$=2.25mol,根据混合物的平均分子式确定烷烃的分子式.
解答 解:混合气体22.4L,物质的量为物质的量为$\frac{22.4L}{22.4L/mol}$=1mol,n(CO2)=$\frac{121g}{44g/mol}$=2.75g,n(H2O)=$\frac{40.5g}{18g/mol}$=2.25mol,
该混合烃中平均C原子数为:$\frac{2.75mol}{1mol}$=2.75,平均H原子数为:$\frac{2.25mol×2}{1mol}$=4.5,
则该混合烃的平均分子式为:C2.75H4.5,
已知一种气体为丙炔,分子式为C3H4,则该烷烃分子中含有的C原子数小于3,含有的H原子数大于4,
满足条件的烷烃只有C2H6,
故选C.
点评 本题考查有关混合物反应的计算,题目难度中等,根据题干信息计算出平均分子式为解答关键,注意讨论法、平均分子式法在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.


 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案科目:高中化学 来源: 题型:选择题
 科学家研制出多种新型杀虫剂代替DDT,化合物M是其中的一种.下列关于M的说法错误的是( )
科学家研制出多种新型杀虫剂代替DDT,化合物M是其中的一种.下列关于M的说法错误的是( )| A. | M的分子式为C15H22O3 | |
| B. | 与FeCl3溶液发生反应后溶液不显紫色 | |
| C. | M可以发生银镜反应 | |
| D. | 1molM最多与1molH2完全加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素的相对原子质量逐渐增大 | B. | 核外电子排布呈周期性变化 | ||
| C. | 原子半径呈周期性变化 | D. | 元素主要化合价呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 它可能具有的性质是( )
它可能具有的性质是( )| A. | ①②④ | B. | ②③④ | C. | ①②③ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
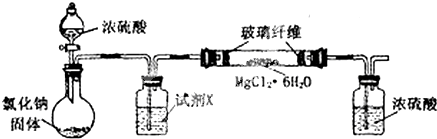
| 实验序号 | 氯化镁固体中氯元素含量/% | 温度/℃ | 粉碎方式 | 催化效果/g•g-1 |
| 1 | 70.97 | 20 | 滚动球磨 | 3.9×104 |
| 2 | 74.45 | 20 | 滚动球磨 | 5.0×104 |
| 3 | 74.45 | 20 | 振动球磨 | 5.9×104 |
| 4 | ω | 100 | 振动球磨 | 6.5×104 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
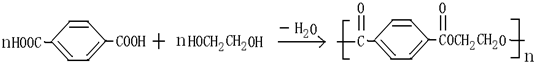
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com