
【题目】有关苯分子中的化学键描述正确的是( )
A. 每个碳原子的sp2杂化轨道中的其中一个形成大π键
B. 每个碳原子的未参加杂化的2p轨道形成大π键
C. 碳原子的三个sp2杂化轨道与其他形成两个σ键
D. 碳原子的未参加杂化的2p轨道与其他形成σ键
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】电镀行业产生的酸性含铬废水对环境有污染,其中所含的Cr(VI)是主要污染物,可采用多种方法处理将其除去。
查阅资料可知:
①在酸性环境下,Cr(VI)通常以Cr2O72-的形式存在,Cr2O72-+H2O ![]() 2CrO42-+2H+
2CrO42-+2H+
②Cr2O72-的氧化能力强于CrO42-
③常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下表:
阳离子 | Fe3+ | Fe2+ | Cr3+ |
开始沉淀的pH | 1.9 | 7.0 | 4.3 |
沉淀完全的pH | 3.2 | 9.0 | 5.6 |
I.腐蚀电池法
(1)向酸性含铬废水中投放废铁屑和焦炭,利用原电池原理还原Cr(VI)。下列关于焦炭的说法正确的是________(填字母序号)。
a. 作原电池的正极 b. 在反应中作还原剂 c. 表面可能有气泡产生
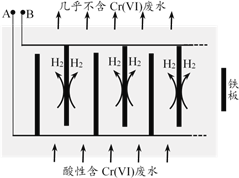
II.电解还原法
向酸性含铬废水中加入适量NaCl固体,以Fe为电极电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准。装置如右图所示。
(2)A极连接电源的________极,A极上的电极反应式是________。
(3)电解开始时,B极上主要发生的电极反应为2H++2e-=H2↑,此外还有少量Cr2O72-在B极上直接放电,该反应的电极反应式为________。
(4)电解过程中,溶液的pH不同时,通电时间(t)与溶液中Cr元素去除率的关系如右图所示。

①由图知,电解还原法应采取的最佳pH范围为________。
a. 2 ~ 4 b. 4 ~ 6 c. 6 ~ 10
②解释曲线I和曲线IV去除率低的原因:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某容积为1L的密闭容器中通入1mol CO2和3mol H2,发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH<0。下列有关说法正确的是
CH3OH(g)+H2O(g) ΔH<0。下列有关说法正确的是
A. 该反应在高温下才能自发进行
B. 再加入一定量CO2,则n(CH3OH)/n(CO2)减小
C. 温度升高,反应的平衡常数K增大
D. 当CO2和H2转化率相等时,该反应达到化学平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳和氮的化合物与人类生产、生活密切相关.

(1)在一恒温、恒容密闭容器中发生反应:Ni (s)+4CO(g)![]() Ni(CO)4(g),△H<0.利用该反应可以将粗镍转化为纯度达99.9%的高纯镍.下列说法正确的是 (填字母编号).
Ni(CO)4(g),△H<0.利用该反应可以将粗镍转化为纯度达99.9%的高纯镍.下列说法正确的是 (填字母编号).
A.增加Ni的量可提高CO的转化率,Ni的转化率降低
B.缩小容器容积,平衡右移,△H减小
C.反应达到平衡后,充入CO再次达到平衡时,CO的体积分数降低
D.当4v正[Ni(CO)4]=v正(CO)时或容器中混合气体密度不变时,都可说明反应已达化学平衡状态
(2)CO与镍反应会造成含镍催化剂的中毒.为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫.
已知:CO(g)+1/2QUOTE\*MERGEFORMATO2(g)=CO2(g)△H=﹣Q1 kJmol﹣1
S(s)+O2(g)=SO2(g)△H=﹣Q2 kJmol﹣1
则SO2(g)+2CO (g)=S(s)+2CO2(g)△H= .
(3)对于反应:2NO(g)+O2═2NO2(g),向某容器中充入10mol的NO和10mol的O2,在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下随温度变化的曲线(如图1).
①比较P1、P2的大小关系: .
②700℃时,在压强为P2时,假设容器为1L,则在该条件平衡常数的数值为 (最简分数形式)
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图2所示.该电池在使用过程中石墨I电极上生成氧化物Y,那么石墨II极电极反应式为 .若该燃料电池使用一段时间后,共收集到20mol Y,则理论上需要消耗标准状况下氧气的体积为 L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温时,Mg(OH)2的溶度积常数Ksp=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是( )
A. 所得溶液中的c(H+)=1.0×10-13 mol·L-1
B. 所得溶液中由水电离产生的c(H+)=1.0×10-13 mol·L-1
C. 所加的烧碱溶液pH=13.0
D. 所得溶液中的c(Mg2+)=5.6×10-10 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质属于常见氧化剂的一组是
A.Cl2、O2、FeCl3、KMnO4
B.O2、KMnO4、H2、C
C.Na、K、FeCl2、H2、CO
D.CuO、CO、Fe2O3、H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.将40g NaOH溶于水配成1L溶液,其物质的量浓度为1mol·L-1
B.标准状况下,18g水的体积约为22.4L
C.硫酸的摩尔质量是98 g
D.常温常压下,1 mol氧气的体积为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质(A、B、C、D)的物质的量变化如图所示,对该反应的推断合理的是 ( )

A. M点表示v(A)=v(B)
B. 0~6 s内,v(A)∶v(B)∶v(C)∶v(D)=3∶1∶1.5∶2
C. 反应进行到6 s时,各物质的物质的量浓度相等
D. 反应进行到6 s时,C的平均反应速率为 0.1 mol·L-1·s-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com