
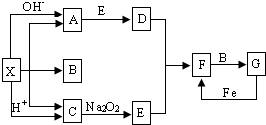
 如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出.常温下X是固体,B和G是液体,其余均为气体.根据如图关系推断:
如图是中学化学中常见物质之间的一些反应关系,其中部分产物未写出.常温下X是固体,B和G是液体,其余均为气体.根据如图关系推断:分析 常温下X是固体,B和G是液体,其余均为气体,气体C能与Na2O2反应得到气体E,应是二氧化碳与过氧化钠反应生成氧气,则C为CO2,E为O2,固体X既能与酸反应生成气体A,又能与碱反应生成气体C,故X应为碳酸形成的铵盐,则X为NH4HCO3或(NH4)2CO3,故A为NH3,B为H2O,D为NO,F为NO2,G为HNO3,据此解答.
解答 解:常温下X是固体,B和G是液体,其余均为气体,气体C能与Na2O2反应得到气体E,应是二氧化碳与过氧化钠反应生成氧气,则C为CO2,E为O2,固体X既能与酸反应生成气体A,又能与碱反应生成气体C,故X应为碳酸形成的铵盐,则X为NH4HCO3或(NH4)2CO3,故A为NH3,B为H2O,D为NO,F为NO2,G为HNO3.
(1)由上述分析可知,X为NH4HCO3或(NH4)2CO3,A为NH3,B为H2O,
故答案为:NH4HCO3或(NH4)2CO3;NH3;H2O;
(2)实验室收集气体D(NO)的方法为:排水法,收集F(NO2)的方法是:向下排空气法,
故答案为:排水;向下排空气;
(3)C→E是CO2与Na2O2反应生成碳酸钠与O2,反应的化学方程式为:2CO2+2Na2O2═2Na2CO3+O2,
故答案为:2CO2+2Na2O2═2Na2CO3+O2;
(4)F与B反应生成G是NO2与水反应生成硝酸与NO,反应的化学方程式为:3NO2+H2O═2HNO3+NO,
故答案为:3NO2+H2O═2HNO3+NO;
(5)Fe在浓硝酸中发生钝化现象,硝酸浓溶液可以在常温下用铁罐车储运,
故答案为:Fe在浓硝酸中发生钝化;
(6)硝酸溶液与足量的铜片反应停止后,加入稀硫酸可以观察到铜片表面继续产生气泡,离子方程式为:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O,
故答案为:3Cu+2NO3-+8H+═3Cu2++2NO↑+4H2O.
点评 本题考查无机物的推断,X能与酸碱反应、C到E的转化、物质的状态等是推断突破口,需要学生熟练掌握元素化合物性质,侧重分析与推断能力的考查,题目难度中等.


科目:高中化学 来源: 题型:多选题
| A. | 该反应一定是放热反应 | |
| B. | 该反应一定是吸热反应 | |
| C. | 该反应反应物的总能量一定大于产物的总能量 | |
| D. | 该反应产物的总能量一定大于反应物的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3•H2O?NH4++OH- | B. | Ba(OH)2═Ba2++2OH- | ||
| C. | H2SO4═2H++SO42- | D. | NaHCO3═Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x<y | B. | x>y | C. | x=y | D. | x≧y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Mg2+、Cl-、SO42- | B. | Na+、NH4+、SO42-、HCO3- | ||
| C. | Na+、Ba2+、NO3-、Cl- | D. | K+、Na+、NO3-、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间生成n摩尔A,同时生成3n摩尔B | |
| B. | A,B,C的浓度不再变化 | |
| C. | A,B,C的分子数之比为1:3:2 | |
| D. | V正=V逆=0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 书写热化学方程式时,只要在化学方程式的右端写上热量的符号和数值即可 | |
| B. | 凡是在加热或点燃条件下进行的反应都是吸热反应 | |
| C. | 把化学反应中物质的变化和反应的焓变同时表示出的化学方程式叫做热化学方程式 | |
| D. | 氢气在氧气中燃烧的热化学方程式是2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| [H2]/mol•L-1 | [Cl2]/mol•L-1 | v/mol•L-1•s-1 |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 4.0k |
| A. | m=1、n=1 | B. | m=$\frac{1}{2}$、n=$\frac{1}{2}$ | C. | m=$\frac{1}{2}$、n=1 | D. | m=1、n=$\frac{1}{2}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com