
2016��12��1�գ���Ϊ�������������������ʯīϩ����͵缫֮����ٴ��������˶������ԣ�������ʯīϩ��أ���ط�ӦʽΪLixC6+Li1-xCoO2  C6+LiCoO2,�乤��ԭ����ͼ�����й��ڸõ�ص�˵����ȷ����
C6+LiCoO2,�乤��ԭ����ͼ�����й��ڸõ�ص�˵����ȷ����
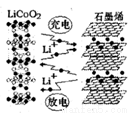
A. �õ�����ø�Ĥ��ѡ�����ӽ���Ĥ
B. �ŵ�ʱ��LiCoO2�������ĵ缫��ӦΪ��LiCoO2-xe-= Li1-xCoO2+xLi+
C. ʯīϩ��ص��ŵ�����ߵ�صĴ������������������ܶ�
D. �Ͼɵĸõ�ؽ��С��ŵ紦������Li+Ƕ��ʯīϩ�ж������ڻ���
 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��һ�������������Բ��ԣ��ģ���b�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ҹ���ѧ�ҷ�����ˮ��Һ﮵��Ϊ�綯������չɨ�����ϰ���װ��ԭ������ͼ��ʾ�����й��屡Ĥֻ����Li+ͨ��������ӵ�ص��ܷ�ӦΪxLi +Li1-xMn2O4 LiMn2O4�������й�˵���������
LiMn2O4�������й�˵���������
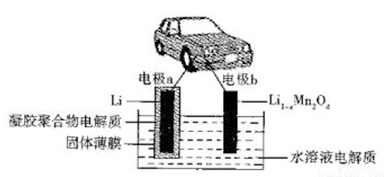
A. �ŵ�ʱ��Li+�������屡Ĥ���뵽ˮ��Һ�������
B. �ŵ�ʱ��������ӦΪLi1-xMn2O4+xLi++xe- LiMn2O4
LiMn2O4
C. �õ�ص�ȱ���Ǵ��ڸ���Ӧ:2Li +2H2O 2LiOH+H2��
2LiOH+H2��
D. ���ʱ���缫bΪ����������������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�Ͼ��и߶�ѧҵˮƽģ����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������Ԫ��X��Y��Z��W��R�����ǵ�ԭ��������������X��ԭ�Ӱ뾶��С��Ԫ�أ�Y��Rͬ������Rԭ�Ӻ˵��������Yԭ�Ӻ˵������2����Z��Wԭ�ӵ�����������֮����Y��Rԭ�ӵ�����������֮����ȡ�����˵����ȷ����
A. X��Yֻ���γ�һ�ֻ�����
B. W��R������������ˮ�������ԣ�W>R
C. Y��R�ֱ���X�γɵĻ���������ȶ��ԣ�Y>R
D. ԭ�Ӱ뾶��r(Z)<r(Y)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�Ͼ��и߶�ѧҵˮƽģ����Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ����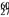 Co�������ڲ��Ƿ�������ơ����ȡ����жԵ�˵����ȷ����
Co�������ڲ��Ƿ�������ơ����ȡ����жԵ�˵����ȷ����
A. �˵����Ϊ27 B. ������Ϊ33 C. ������Ϊ60 D. ���������Ϊ60
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ�ൺ�и�����һ��ͳһ����������ۻ�ѧ�Ծ��������棩 ���ͣ������
�ú��ܷ��ϣ���Ҫ�ɷ�ΪCo������һ������Ni��Al203��Fe��SiO2�ȣ��Ʊ������ܾ��壨CoC2O4��2H2O���Ĺ�ҵ������ͼ����֪���ٲ����ܾ���������ˮ��RHΪ�л���(�ѵ��룩
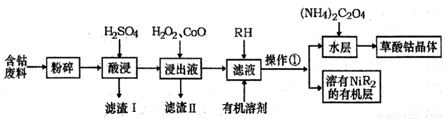
��1������I����Ҫ�ɷ���______���ѧʽ����д��һ�������������ʵĴ�ʩ_______��
��2�������� �õ�����Ҫ������________________��
��3��H2O2��һ����ɫ��������д������H2O2������Ӧ�����ӷ���ʽ__________��
��4�����������ܵ�Ŀ����__________��
��5�������ܾ���ֽ����Եõ������ܵ����������Co�Ļ��ϼ�Ϊ��2����3����ȡһ�����ܵ��������280mL 5mol/L����ǡ����ȫ�ܽ⣬���õ�CoCl2��Һ��2.24L����״��������ɫ���壬�ɴ˿�ȷ��������������Co��O�����ʵ���֮��Ϊ_________��
��6��ʵ���ҿ���������KMnO4��Һ�ζ���������ӣ�C2O42-�����ⶨ��Һ��C2O42-��Ũ�ȣ�д���˷�Ӧ�����ӷ���ʽ_________��KMnO4 ����Һ���������ữ�����������ữ����ʹ�ⶨ���________���ƫ�ߡ�����ƫ�͡�����Ӱ�족����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�찲��ʡ������ʮУ������3���������ۻ�ѧ�Ծ��������棩 ���ͣ��ƶ���
��֪����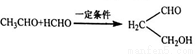 ��
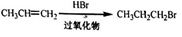
��
���ñ���������ʺϳɺ���С�����л���K���ϳ�·�����£�
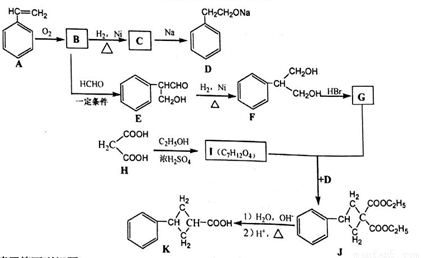
��ش��������⣺
��1��A��������_______��E�к��������ŵ�������_____��
��2��B��C �ķ�Ӧ������_______ ��F��G�ķ�Ӧ������____��
��3��G��I�Ľṹ��ʽ�ֱ�Ϊ_______��________��
��4��д��F��H��һ�������ºϳɸ߷��ӻ�����Ļ�ѧ��Ӧ����ʽ��_______��
��5��ͬʱ��������������E��ͬ���칹����ĿΪ________�֡�
�� �ܷ���������Ӧ���� �ܷ���ˮ�ⷴӦ����ˮ�����֮һ����FeCl3��Һ������ɫ��Ӧ��
��6����д����H2C=CHCH2BrΪԭ���Ʊ�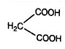 ���ο��������д���Ʊ��ĺϳ���·����ͼ�����Լ���ѡ����________
���ο��������д���Ʊ��ĺϳ���·����ͼ�����Լ���ѡ����________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�찲��ʡ������ʮУ������3���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��0.1000mol/L�ı�����ֱ�ζ�20.00mL��0.1000mol/L��ˮ��20.00mL��0.1000mol/L����������Һ�ĵζ�������ͼ��ʾ��������Ϊ�ζ��ٷ������ζ��������ܵζ���������������Ϊ�ζ���������ҺpH��������һ�����ָʾ������ɫ��ΧΪ4.4-6.2�������йصζ�����˵����ȷ����
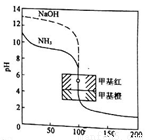
A. �ζ���ˮ��Һ���ζ�����Ϊ50��ʱ��������Ũ�ȼ���ڹ�ϵ��c(NH4+)+c(H+)=c(OH-)
B. �ζ�����Ϊ100��ʱ����Ϊ�ζ������з�Ӧǡ����ȫ��ʱ��
C. �ӵζ����߿����жϣ�ʹ�ü�����Ϊ�ζ������е�ָʾ��ȷ�Ը���
D. �ζ���ˮ��Һ���ζ�����Ϊ150��ʱ��������Һ������Ũ���д�С��ϵc(Cl-)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�����б�Ӧ�ظ߶���ѧ��ѧҵˮƽ���ԣ�������ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й����ʵ�������Ӧ�õ�˵���У�����ȷ����
A. Fe3�����������ԣ����ܽ�ӡˢ��·���ϵĽ���ͭ
B. ̼�ᱵ�����ᱵ��������ˮ��������������
C. ���������кܸߵ��۵㣬���������������ռ������
D. ����������а뵼�����ܣ������Ƴɹ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡ�������и߶�3���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪1g���ȼ���£�N2H4������ȼ������N2��H2O��g��ʱ���ų�16.7kJ����������÷�Ӧ���Ȼ�ѧ����ʽ��ȷ����( )
A. N2H4+O2=N2+2H2O��H= ��534.4kJ/mol
B. N2H4(g)+ O2(g)=N2(g)+2H2O(g)��H= ��16.7kJ/mol
C. N2H4(g)+O2(g)=N2(g)+2H2O(l)��H= ��534.4kJ/mol
D. N2H4(g)+O2(g)=N2(g)+2H2O(g)��H= ��534.4kJ/mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com