
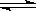 2NH3 (g)从两条途径分别建立平衡:
2NH3 (g)从两条途径分别建立平衡:| A.途径Ⅰ与途径Ⅱ所得混合气体的百分组成相同 |
| B.途径Ⅰ的平衡速率v (N2)与途径Ⅱ的平衡速率v (NH3)的比值为1∶2 |
| C.途径Ⅰ所得NH3的浓度与途径Ⅱ所得NH3的浓度之比为1∶2 |
| D.途径Ⅰ与途径Ⅱ所得平衡混合气体的物质的量之比为1∶2 |
 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案科目:高中化学 来源:不详 题型:填空题
 2/3Fe(s)+CO2(g)
2/3Fe(s)+CO2(g)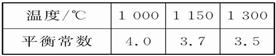
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
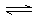 xC(g)+D(g),某温度时,在固定容积为2L的密闭容器内充入一定量的A、B,并保持温度不变。A、B、C、D物质的量随时间的变化如图所示:
xC(g)+D(g),某温度时,在固定容积为2L的密闭容器内充入一定量的A、B,并保持温度不变。A、B、C、D物质的量随时间的变化如图所示: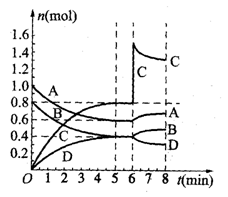
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法正确的( )
N2O4(g) ,平衡后,向容器内再充入1molNO2,下列说法正确的( )| A.容器内气体颜色先变深后变浅,最后比原来还要浅 |
| B.反应向正反应方向移动 |
| C.NO2的转化率变小 |
| D.N2O4的体积分数一定增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CH3OH(g) △H<0,各物质的浓度如下表
CH3OH(g) △H<0,各物质的浓度如下表
| A.2min-4min内用氢气表示的速率为0.3mol/(L?min) |
| B.达平衡时,CO的转化率为62.5% |
| C.反应在第2min时改变了条件,可能是加入了催化刺 |
| D.反应在第2min时改变了条件,可能增加了H2的浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.反应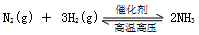 的化学平衡常数表达式为 的化学平衡常数表达式为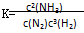 |
| B.化学平衡常数、弱电解质的电离平衡常数、溶度积常数均只受温度的影响 |
| C.对于弱电解质的电离平衡常数,当温度一定时,电离平衡常数越小,其酸性越强 |
| D.将AgNO3溶液和KCl溶液混合后,若c(Ag+)·c(Cl-)<KSP(AgCl),则溶液中无沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CO(g)+H2(g) ,ΔH>0,达到平衡,下列说法正确的是( )
CO(g)+H2(g) ,ΔH>0,达到平衡,下列说法正确的是( )| A.升高温度,平衡向逆反应方向移动 |
| B.加入固体碳,平衡向正反应方向移动 |
| C.加入水蒸气,平衡向逆反应方向移动 |
| D.扩大容器体积,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2SO3(g);
2SO3(g);
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2HI(g),下列情况能说明该反应一定达到平衡状态的是
2HI(g),下列情况能说明该反应一定达到平衡状态的是| A.混合气体的颜色不再改变 |
| B.混合气体的压强不再改变 |
| C.单位时间内拆开1mol H-H键,同时生成2mol H-I键 |
| D.混合气体的密度不再改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com