
| A.1:2:3 | B.3:2:1 | C.6:3:2 | D.6:3:1 |
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源:不详 题型:填空题
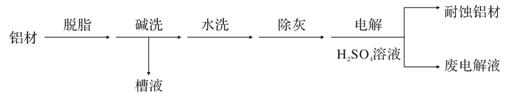
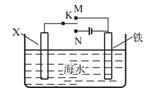
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
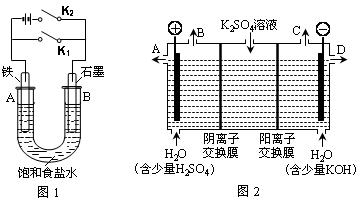

| A.溶液中Na+向B极移动 |
| B.从A极处逸出的气体能使湿润的KI淀粉试纸变蓝 |
| C.反应一段时间后加适量盐酸可恢复到电解前电解质的浓度 |
| D.若标准状况下从A极逸出2.24L气体,则外电路上通过的电子数目略大于0.2NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 序号 | 反应 | 平衡常数 |
| 1 | Au + 6HNO3(浓)= Au(NO3)3 + 3NO2↑+ 3H2O | << 1 |
| 2 | Au3+ + 4Cl— = AuCl4— | >>1 |
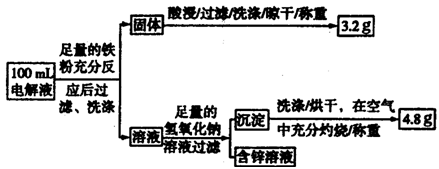
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
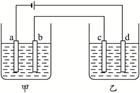
| | 甲池 | 乙池 |
| A | AgNO3溶液 | CuCl2溶液 |
| B | NaOH溶液 | AgNO3溶液 |
| C | NaCl溶液 | CuSO4溶液 |
| D | H2SO4溶液 | NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.①④ |
| C.②③ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.XYZM | B.XZMY | C.MZXY | D.XZYM |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钢板镀锌可以防止锈蚀 |
| B.高纯石英玻璃可用来制造光导纤维 |
| C.羊毛、蚕丝、棉花的主要成分都是纤维素 |
| D.生铁和普通钢都是铁碳合金 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com