
现有Fe2O3和Fe3O4组成的混合物W g,将其投入到V mL5mol/L的盐酸中,再加入22.4g铁粉,固体恰好完全溶解,收集到标准状况下气体4480mL。向反应后溶液中滴加KSCN溶液,无颜色变化,下列推断正确的是
A.转移电子为1.0mol B.W可能等于48.8
C.V可能等于360 D.发生的反应均为氧化还原反应
 习题精选系列答案
习题精选系列答案科目:高中化学 来源:2015-2016学年河南省高一上学期12月月考化学试卷(解析版) 题型:填空题
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,实验小组利用A制备Al(OH)3的操作流程如下:
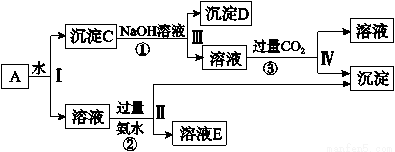
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中分离溶液和沉淀所采取的操作名称是______,该实验操作所用到的玻璃仪器有____ _。
(2)根据上述流程,写出D、E所含物质的化学式:沉淀D________;溶液E________、_______。
(3)写出②、③反应的离子方程式:
②__________ __ _;③________ _____。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上学期第二次模拟化学试卷(解析版) 题型:填空题
下图是一个化学过程的示意图。
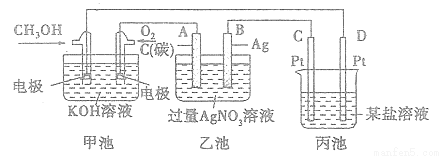
(1)图中甲池中OH-移向 极(填“CH3OH”或“O2”)。
(2)写出通入CH3OH的电极的电极反应式: 。
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为 极(填“A”或"B”),并写出此电极的反应式:____ 。
(4)乙池中总反应的离子方程式:____ 。
(5)当乙池中B(Ag)极的质量增加5.4g时,乙池的pH是 (若此时乙池中溶液的体积为500mL);此时丙池某电极析出1.60g某金属,则丙中的某盐溶液可能是 (填序号)。
A. MgSO4 B.CuSO4 C.AgNO3 D.AlCl3
查看答案和解析>>
科目:高中化学 来源:2016届江苏省南京市六校高三上学期12月联考化学试卷(解析版) 题型:实验题
氯酸钠(NaClO3)是无机盐工业的重要产品之一。
(1)工业上制取氯酸钠采用在热的石灰乳中通入氯气,然后结晶除去氯化钙后,再加入适量的 (填试剂化学式),过滤后即可得到。
(2)实验室制取氯酸钠可通过如下反应3C12+6NaOH 5NaC1+NaC1O3+3H2O
5NaC1+NaC1O3+3H2O
先往-5℃的NaOH溶液中通入适量C12,然后将溶液加热,溶液中主要阴离子浓度随温度的变化如右图所示,图中C表示的离子是 。
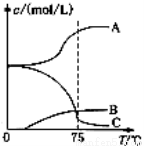
(3)某企业采用无隔膜电解饱和食盐水法生产氯酸钠。则反应化学方程式为: 。
(4)样品中C1O3-的含量可用滴定法进行测定,步骤如下:
步骤1:准确称取样品ag(约2.20g),经溶解、定容等步骤准确配制1000mL溶液。
步骤2:从上述容量瓶中取出10.00mL溶液于锥形瓶中,准确加入25mL 1.000mol/L (NH4)2Fe(SO4)2溶液(过量),再加入75mL硫酸和磷酸配成的混酸,静置10min。
步骤3:再在锥形瓶中加入100mL蒸馏水及某种指示剂,用0.0200mol/L K2Cr2O7标准溶液滴定至终点,消耗体积15.62mL。
步骤4: 。
步骤5:数据处理与计算。
①步骤2中反应的离子方程式为 ;静置10min的目的是 。
②步骤3中K2Cr2O7标准溶液应盛放在 (填仪器名称)中。
③为精确测定样品中C1O3-的质量分数,步骤4操作为 。
(5)在上述操作无误的情况下,所测定的结果偏高,其可能的原因的原因是 。
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第三次月考化学试卷(解析版) 题型:选择题
在T ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·cm-3,溶质的质量分数为w,其中含NH4+的物质的量为b mol。下列叙述中一定正确的是
A.溶质的质量分数为w=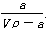 ×100%
×100%
B.溶质的物质的量浓度c= mol·L-1
mol·L-1
C.溶液中c(OH-)=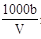 mol·L-1
mol·L-1
D.上述溶液中再加入VmL水后,所得溶液溶质的质量分数大于0.5w
查看答案和解析>>
科目:高中化学 来源:2016届上海市十三校高三上学期第一次联考化学试卷(解析版) 题型:实验题
索氏制碱又称氨碱法,其主要生产流程如右图:
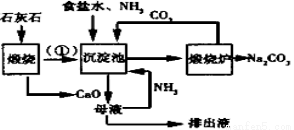
用化学方程式表示沉淀池中发生的反应 ,排出液的主要成分是 。
氨碱法制得的纯碱样品中可能会含有杂质(如NaCl)。现用两个实验方案测定纯碱样品的纯度。
方案1气体法 :称取样品m克装入Y型试管左侧(如右图)
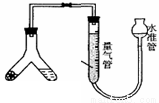
37.Y型试管另一端应装入试剂为 ,量气管中液体应为 。若最后读数时,发现水准管液面高于量气管(其他操作都正确),则计算所得纯碱样品的纯度值 (填“偏大”、“偏小”或“无影响”)。
方案2滴定法:
已知: 25℃时0.1 mol/L的NaHCO3溶液的pH约为8.3
0.1 mol/L的Na2CO3 溶液的pH约为11.6
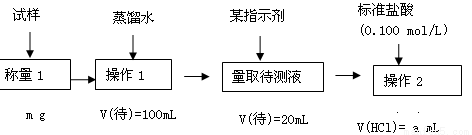
38.指示剂选用酚酞,则该纯碱样品的纯度为 。(请用所给数据的字母符号表示)
氨碱法中钠利用率不高,一些化工专家开始研究有机胺制碱法,其工艺流程如下:
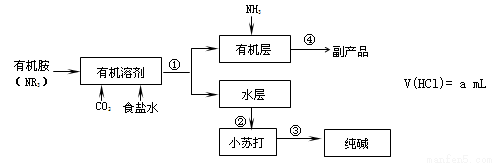
已知: NR3+ HCl →NR3 · HCl,且NR3 · HCl易溶于有机溶剂
NR3 · HCl+NH3→NR3 +NH4Cl
39.有机胺制碱法反应生成小苏打的化学方程式是 , 操作①是 。
40.副产品的成分是 ,本工艺流程中可循环利用的物质是 。
查看答案和解析>>
科目:高中化学 来源:2016届四川省高三上学期12月月考理综化学试卷(解析版) 题型:填空题
利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下。

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)实验室用98%(密度是1.84g/cm3)的浓硫酸配制250 mL 4.8 mol·L-1的H2SO4溶液,所用的玻璃仪器除烧杯、玻璃棒和量筒外,还需___________,需要取用________ml98%(密度是1.84g/cm3)的浓硫酸.
(2)酸浸时,为了提高浸取率可采取的措施有____________________(答出两点)。
(3)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:_________________。
(4)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | - | - | - |
沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。滤液Ⅱ中阳离子主要有________;但溶液的pH不能超过8,其理由是_________________________。
(5)钠离子交换树脂的反应原理为Mn++nNaR―→MRn+nNa+,利用钠离子交换树脂除去的滤液Ⅱ中的金属阳离子是_______________________________。
(6)写出上述流程中用SO2进行还原时发生反应的化学方程式:_______________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省高二上学期第三次月考化学试卷(解析版) 题型:选择题
2010年在上海举办的世博会主打环保牌,20辆氢燃料电池公交车、300辆氢燃料电池出租车投入运行,它们以氢气为能源,实现了真正的零污染。氢氧燃料电池的电解液为KOH溶液,下列有关该电池的叙述不正确的是
A.正极反应式为:O2+2H2O+4e-===4OH-
B.该燃料电池的总反应方程式为:2H2+O2===2H2O
C.工作一段时间后,电解液中KOH的物质的量浓度不变
D.用该电池电解CuCl2溶液,产生2.24 L Cl2(标准状况)时,有0.2 mol电子转移
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第二次段考化学试卷(解析版) 题型:实验题
某化学研究小组在使用FeSO4溶液与NaOH溶液制备Fe(OH)2沉淀过程中观察到生成的白色沉淀迅速转变为灰绿色,最后变为红褐色,该小组针对绿色物质展开研究。
【查阅文献】
文献名称 | 有关Fe(OH)2的描述 |
《大学普通化学(下册)》 | 白色沉淀,易被氧化成微绿色Fe3(OH)8 |
《化学教育》 | 白色沉淀,在冷水中易形成绿色的水合物Fe(OH)2·nH2O,热水中不易形成水合物 |
(1)写出Fe(OH)2在空气中被氧化为Fe(OH)3的化学方程式______________;
【提出假设】假设一:绿色物质是Fe(OH)2·nH2O;
假设二:________________;·······
【实验探究】针对上述假设与假设二,展开实验研究:
实验序号 | 实验步骤 | 实验现象 |
一 | ①在试管中加入20mL蒸馏水,加热煮沸,滴苯液封 ②保持较高温度,使用长滴管伸入液面下依次挤入一滴饱和FeSO4 溶液、一滴NaOH溶液 | 出现白色絮状沉淀,并能保持一段时间 |
二 | ①在试管中加入20mL蒸馏水 ②加入一滴饱和FeSO4 溶液、一滴NaOH溶液 | 出现白色沉淀,迅速转变为灰绿色,最后变为红褐色 |
三 | ①在试管中加入20mL蒸馏水,加热煮沸,滴苯液封 ②恢复室温后,使用长滴管伸入液面下依次挤入一滴饱和FeSO4 溶液、一滴NaOH溶液 | 出现白色沉淀,迅速转变为绿色沉淀 |
(1)实验室保存FeSO4溶液常需加入 (填化学式,下同),为检验某FeSO4溶液是否变质,可向溶液中加入______________;
(2)由实验一与实验 (填实验序号)的现象可推断假设 可能成立。
(3)为了进一步探究假设二是否成立,小组成员进行如下实验,请完成下表:
试剂:蒸馏水、NaOH溶液、苯、FeSO4溶液、氧气
实验步骤 | 实验现象与结论 |
①在试管中加入20mL蒸馏水,加热煮沸,滴苯液封 ② ③ | 若沉淀中出现绿色的迹象,则假设二成立; 若沉淀中没有出现任何绿色的迹象,则假设二不成立。 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com