
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A.100g46%甲酸(HCOOH)水溶液所含的氧原子数为5NA
B.14gFe发生吸氧腐蚀生成Fe2O3·xH2O,电极反应转移的电子数为0.75NA
C.8.8 g乙酸乙酯中含共用电子对的数目为1.3NA
D.标准状况下,22.4LCS2中所含的分子数目为 NA个
【答案】A
【解析】
A.100g46%甲酸(HCOOH)水溶液中甲酸的物质的量为![]() =1mol,水的物质的量为
=1mol,水的物质的量为![]() =3mol,则溶液中氧原子的总物质的量为1mol×2+3mol=5mol,则所含的氧原子数为5NA,故A正确;
=3mol,则溶液中氧原子的总物质的量为1mol×2+3mol=5mol,则所含的氧原子数为5NA,故A正确;
B.铁发生吸氧腐蚀电极反应式:Fe2e=Fe2+,14.0gFe物质的量为![]() =0.25mol,转移电子数为:0.25mol×2×NA=0.5NA,故B错误;
=0.25mol,转移电子数为:0.25mol×2×NA=0.5NA,故B错误;
C.乙酸乙酯分子中含有14对共用电子对,8.8g乙酸乙酯的物质的量为![]() =0.1mol,8.8g乙酸乙酯中共用电子对数为0.1mol×14×NAmol1=1.4NA,故C错误;
=0.1mol,8.8g乙酸乙酯中共用电子对数为0.1mol×14×NAmol1=1.4NA,故C错误;
D.标准状况下CS2是液体,不能用标况下气体的摩尔体积计算物质的量,则分子数目不能确定,故D错误;
答案选A。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实或实验现象的化学用语正确的是
A. 硫酸酸化的KI淀粉溶液久置后变蓝:4I-+O2 + 4H+ ![]() 2I2+2H2O
2I2+2H2O
B. 铁和稀硝酸反应制得浅绿色溶液:Fe + 4H+ + NO3-![]() Fe3+ + NO↑+ 2H2O
Fe3+ + NO↑+ 2H2O
C. 水垢上滴入CH3COOH溶液有气泡产生:CaCO3+2H+ ![]() Ca2++CO2↑+ H2O
Ca2++CO2↑+ H2O
D. SO2通入漂白粉溶液中产生白色浑浊:SO2+Ca2++2ClO-+H2O ![]() CaSO3↓+2HClO
CaSO3↓+2HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、铬、锰统称为黑色金属,它们的单质、合金及其化合物在科研和生产中有着重要用途。
请回答下列问题:
(1)基态铁原子的价电子轨道表示式为__。铁、铬、锰属于周期表中的___区元素。
(2)基态铬原子和基态锰原子中第一电离能较大的是___(填元素符号),原因为___。
(3)化学式为CrC13·6H2O的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色,已知Cr3+的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量AgNO3溶液,所得AgC1沉淀的物质的量之比为3:2:1。
①呈暗绿色的配合物内界的化学式为___。
②H2O分子的VSEPR模型为___。
(4)MnF2和MnCl2均为离子化合物,MnF2的熔点高于MnCl2熔点的原因为___。
(5)一氧化锰在医药、冶炼上用途广泛,其立方晶胞结构如图所示。
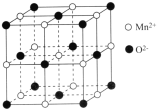
①该晶胞中由O2-形成的正八面体空隙数目为__。
②设NA为阿伏加德罗常数的值,晶胞中距离最近的两个O2-之间的距离为apm,则MnO晶体的密度ρ=____g·cm-3。(用含a、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
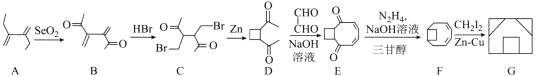
【题目】囧烷(G)是一种重要的烃,一种合成囧烷的路线如图所示:
已知: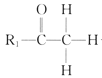 +R2—CHO
+R2—CHO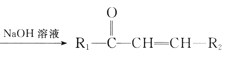 +H2O。
+H2O。
请回答下列问题:
(1)A的化学名称为___;G的分子式为__。
(2)B→C的反应类型为___;C中所含官能团的名称为__。
(3)D→E的化学方程式为___。
(4)同时满足下列条件的B的同分异构体有__种(不考虑立体异构);其中核磁共振氢谱有5组峰的结构简式为___。
①属于芳香族化合物且苯环上连有3个取代基。
②与FeC13溶液发生显色反应。
(5)参照上述合成路线和信息,以![]() 为原料(其他试剂任选),设计制备
为原料(其他试剂任选),设计制备![]() 的合成路线:___。
的合成路线:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,要使溶液中
CH3COO-+H+,要使溶液中![]() 值增大,可以采取的措施是
值增大,可以采取的措施是
A.加少量烧碱B.降低温度C.加少量冰醋酸D.加水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应)。请回答下列问题:

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34![]() C8H18+甲,甲
C8H18+甲,甲![]() 4乙,则甲的分子式为________,乙的结构简式为____________________________________。
4乙,则甲的分子式为________,乙的结构简式为____________________________________。
(2)B装置中的实验现象可能是________,写出反应的化学方程式:__________,其反应类型是________。
(3)C装置中可观察到的现象是____________,反应类型是________。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_____(填字母)中的实验现象可判断该资料是否真实。为了探究溴与乙烯反应是加成反应而不是取代反应,可以测定装置B中溶液在反应前后的酸碱性,简述其理由: __________________。
(5)通过上述实验探究,检验甲烷和乙烯的方法是________(选填字母,下同);除去甲烷中乙烯的方法是________。
A.气体通入水中 B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,甲烷火焰明亮而乙烯产生少量黑烟,原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一种瓦斯分析仪(下图甲)能够在煤矿巷道中的甲烷达到一定浓度时,通过传感器显示出来。该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如下图乙所示,其中的固体电解质是Y2O3-Na2O,O2-可以在其中自由移动。下列有关叙述正确的的是( )
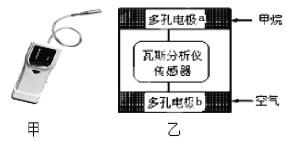
A. 瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a
B. 电极a的反应式为:CH4+5O2-―8e-=CO32- +2H2O
C. 电极b是正极, O2-由电极a流向电极b
D. 当固体电解质中有1 mol O2-通过时,电子转移4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学自酿米酒,具体步骤如下:
![]()
定时监测获得的实验数据图如下:
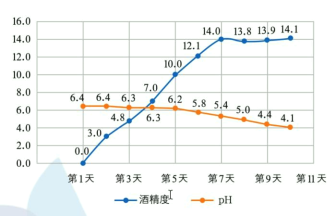
下列说法不正确的是
A.糯米中淀粉在酒曲中糖化酶作用下水解为葡萄糖,葡萄糖在酒化酶作用下转化为乙醇
B.酿造过程中米酒 pH 逐渐下降,可能是因为部分乙醇被空气氧化为乙酸
C.从第 7 天开始米酒的酒精度近乎不变,说明溶液中的葡萄糖已经完全反应
D.该小组最终酿出的米酒酒精度不高,可采用蒸馏法提高酒精度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com