
| A. | 放电时,Co元素的化合价升高 | |
| B. | 放电时,正极的电极反应式为Lil-xCoO2+xe-+xLi+=LiCoO2 | |
| C. | 充电时,Li+在电解质中由阳极向阴极迁移 | |
| D. | 充电时,阴极的电极反应式为C6+xLi++xe-=LixC6 |
分析 放电时的反应为Li1-xCoO2+LixC6═LiCoO2+C6,Co元素的化合价降低,Co得到电子,则Li1-xCoO2为正极,LixC6为负极,LixC6失去电子得到Li+,结合原电池中负极发生氧化反应,正极发生还原反应,充电是放电的逆过程,据此解答.
解答 解:A、放电时,Co元素的化合价降低,而不是升高,故A错误;
B、放电时,正极Lil-xCoO2发生还原反应,电极反应式为Lil-xCoO2+xe-+xLi+=LiCoO2,故B正确;
C、电解池中阳离子向阴极移动,所以充电时,Li+在电解质中由阳极向阴极迁移,故C正确;
D、充电时,阴极发生还原反应,电极反应式为:C6+xLi++xe-=LixC6,故D正确;
故选A.
点评 本题考查二次电池的充放电原理,明确电池反应中元素的化合价变化及原电池的工作原理即可解答,注意与氧化还原反应的结合,在写电极反应式时注意装置中有自由移动的Li+,C选项考查学生的仔细程度,难度适中.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 2.8 g铁粉与50 mL 4 mol•L-1盐酸反应转移电子的数目为0.15NA | |
| B. | 常温下1 L pH=13的氢氧化钠溶液中由水电离出的H+的数目为0.1NA | |
| C. | 标准状况下,8.96 L氢气、一氧化碳的混合气体完全燃烧,消耗氧分子的数目为0.2NA | |
| D. | 1.2 g金刚石与石墨混合物中含有碳碳单键的数目为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| ①中的反应物 | ②中的现象 | 实验结论 | 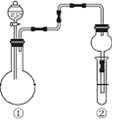 | |
| A | 纯碱、稀硫酸 | 硅酸钠溶液中出现白色沉淀 | 酸性:硫酸>碳酸>硅酸 | |
| B | MnO2、浓盐酸 | 淀粉KI溶液变蓝 | Cl2有氧化性 | |
| C | Na2SO3、硫酸 | 溴水褪色 | SO2有漂白性 | |
| D | Cu、硝酸 | 红棕色气体 | ①中硝酸为浓硝酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中c(SO42-)=0.2mol/L | |
| B. | 该溶液中c(SO42-)=2c(Al3+) | |
| C. | 该溶液中:3c(Al3+)+c(K+)+c(H+)=2c(SO42-) | |
| D. | 向该溶液中加入2L0.1mol/LBa(OH)2溶液,生成的沉淀为BaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验Fe(NO3)2样品已被氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 |
| B | 提取碘水中碘 | 将碘水倒入分液漏斗,加入适量乙醇,振荡后静置 |
| C | 验证Mg(OH)2沉淀可以转化为 Fe(OH)3沉淀 | 向 2mL1mol•L-1NaOH 溶液中加入2~3 滴 lmol•L-1MgCl2溶液,生成白色沉淀,再加入2~3滴lmol•L-1FeCl3溶液 |
| D | 比较碳和硅的非金属性强弱 | 向饱和的Na2SiO3溶液中通人CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 溶液中c(H+)>c(OH-) | |
| B. | NH4+水解是微弱的 | |
| C. | NH3•H2O是弱碱 | |
| D. | 由H2O电离出的c(H+)<10-7 mol/L | |
| E. | 物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  配制0.1mol/L的NaNO3溶液 | B. |  检查装置气密性 | ||
| C. | 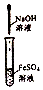 制取Fe(OH)2沉淀 | D. | 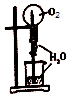 进行喷泉实验 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com