
��NAΪ����٤����������ֵ��������˵���У���ȷ����
A�������£�0��1 mol̼���ƾ����к���CO2—3�ĸ���Ϊ0.1 NA
B����״����22��4LH2O����������ΪNA
C��1 L0��5 mol·L-1 CH3COOH��Һ�У�CH3COO—���ӵĸ���Ϊ0��5 NA
D����NO��NO2�Ļ������22��4L�У����еĵ�ԭ����ΪNA��
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��.��֪��4Al(s)+3O2(g) = 2Al2O3(s) ��H=��2834.9KJ•mol��1
Fe2O3(s)+ C(s)=
C(s)= CO2(g)+2Fe(s) ��H=+234.1KJ•mol��1
CO2(g)+2Fe(s) ��H=+234.1KJ•mol��1
C(s)+O2(g)= CO2(g) ��H=��393.5KJ•mol��1
д�������������������ȷ�Ӧ���Ȼ�ѧ����ʽ______________ ��
��.��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO(g)+O2(g)  2NO2(g) ��H��0 ��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g) ��H��0 ��ϵ�У�n(NO)��ʱ��ı仯�����
| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1) д���÷�Ӧ��ƽ�ⳣ������ʽ��K= �� ��O2��ʾ��0~2s�ڸ÷�Ӧ��ƽ�����ʦͣ�O2��= ��
(2) �����о�Ŀ�ĺ�ʾ��ͼ������� ��
| A | B | C | D | |
| �о�Ŀ�� | ѹǿ�Է�Ӧ��Ӱ�죨P1>P2�� | �¶ȶԷ�Ӧ��Ӱ�� | ƽ����ϵ����O2�Է�Ӧ��Ӱ�� | �����Է�Ӧ��Ӱ�� |
| ͼʾ |
|
|
|
|
III.��ѧ�������һ��ʹ�ù������ʵĸ�Чȼ�ϵ�ء�һ���缫ͨ���������һ���缫ͨ��ȼ�����������й��������Dz�����Y2O3 ��ZrO2���壬���ڸ������ܴ���O2�����ӣ�����������Ӧ������ȫ�����Ա��飨C3H8������ȼ�ϡ�
(1)����صĸ�����ӦʽΪ________________��
(2)���ŵ�ʱ�����������O2��������____���ƶ����������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ͨ��һ���¶ȵ�����������Һ�У��õ����д�����ء�����غ��Ȼ��ص���Һ.��ø���Һ��c��ClO������c��ClO3����= 2��1������Һ��KCl��KClO�����ʵ���֮��Ϊ �� ��
A. 1��1 B. 2��5 C. 7��2 D. 5��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�ʵ���������ȷ����
A.�ζ���ϴ����ֱ��ע���Һ���еζ�
B.ij��Һ�ȼ���ϡ���������������ټ���BaCl2��Һ������ɫ������˵��ԭ��Һ�к���SO42��
C.����һ�����ʵ���Ũ�ȵ�ϡ����ʱ��������ƿ�м���������ˮ���ٻ���ע��������ȡ��Ũ����
D.ij������ʹʪ�����ɫʯ����ֽ��Ϊ��ɫ���������Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ж�ijЩ�������ʶ��ȷ����
A��Ư�ۺ�����������������ˮ�Ĵ��������ߵ�����ԭ������ͬ��
B���ڴ�����Ƕп��ͽ��������Դ�������������߷����ķ�������Ϊ�����籣����
C�������ô��������IJ���ƿ����ʽ�ζ���ʢȡ��Һ�����ߵ�ԭ������ͬ��
D��12C��14C ��O2��O3���������ʵ����ϵ����ͬ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���������У���ȷ����
A���Ȼ�����Һ�м��������ˮ��Ӧʵ���ǣ�
B���ڼ��������ܷų���������Һ�У�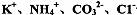 һ���ܹ���������
һ���ܹ���������
C��þ���Ͻ�ȿ���ȫ���ڹ��������ֿ���ȫ���ڹ���NaOH��Һ
D���������ȷ�Ӧԭ�����ܷ�����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
﮵��ؿ��������������ĵ�Դ���õ�ط�ӦΪ��
��֪��

���н����У�����ȷ����
A����ط�Ӧ2Li��s��+I2��s��=2LiI��s�� ��H= -105 kJ·mol-1
B�����������ӦLi-e—=Li+
C������14 gLi����ʱ�������ϻ��ͷ�2mol e—�ĵ���
D���õ�طŵ���ϵ�ص����������ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ�У�����Ũ�ȵĹ�ϵһ����ȷ����
A����ˮ����μ�������õ�������Һ��c��Cl-��>c��NH4+��>c��H+��>c��OH-��
B��pH��ͬ��CH3COONa��Һ��Ba��OH��2��Һ��KHCO3��Һ��c��K+��>c��Na+��>c��Ba2+��
C�����ʵ���Ũ�����Na2CO3��NaHCO3��Һ�������ϣ�
c��Na+��>c��HCO3-��>c��CO32-��>c��OH-��>c��H+��
D���������ʵ�����KHC2O4��H2C2O4����ˮ�����Һ��2c��K+��=c��HC2O4-��+c��H2C2O4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij���Ļ�ѧʽΪC4Hm�����й���C4Hm��˵������ȷ����
A����m��8ʱ������һ������ϩ��Ϊͬϵ��
B����m��4ʱ������һ������̼̼˫��
C������������ͬʱ����̼̼˫����̼̼����
D��1mol C4Hm��ȫȼ�գ�����������3.5mol H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com