
| 实验过程 | 实验现象 |
| 实验1:分别将①、②、③取样于三支试管中,再分别加入溶液④ | ①②无明显变化,③有气泡产生 |
| 实验2:分别将②、③、④取样于三支试管中,再分别加入溶液① | ③、④无明显变化,②溶液变红 |
| 实验3:分别向实验2的三支试管中,继续滴加入足量溶液④ | ④无明显变化,②溶液变红变为无色,③中先无明显现象,之后有气泡产生 |
分析 实验室有四瓶失去标签的无色透明液体,它们分别是稀硫酸、NaOH溶液、Na2CO3溶液和酚酞溶液;
实验1:分别将①、②、③取样于三支试管中,再分别加入溶液④,①②无明显变化,③有气泡产生,则③④分别为稀硫酸和Na2CO3溶液中的一种;
实验2:分别将②、③、④取样于三支试管中,再分别加入溶液①,③、④无明显变化,②溶液变红,则②为酚酞溶液,①为NaOH溶液;
实验3:分别向实验2的三支试管中,继续滴加入足量溶液④,④无明显变化,②溶液变红变为无色,③中先无明显现象,之后有气泡产生,则④为稀硫酸,③为Na2CO3溶液;
综上可知:①为NaOH溶液、②为酚酞溶液、④为稀硫酸、③为Na2CO3溶液;据此分析.
解答 解:实验室有四瓶失去标签的无色透明液体,它们分别是稀硫酸、NaOH溶液、Na2CO3溶液和酚酞溶液;
实验1:分别将①、②、③取样于三支试管中,再分别加入溶液④,①②无明显变化,③有气泡产生,则③④分别为稀硫酸和Na2CO3溶液中的一种;
实验2:分别将②、③、④取样于三支试管中,再分别加入溶液①,③、④无明显变化,②溶液变红,则②为酚酞溶液,①为NaOH溶液;
实验3:分别向实验2的三支试管中,继续滴加入足量溶液④,④无明显变化,②溶液变红变为无色,③中先无明显现象,之后有气泡产生,则④为稀硫酸,③为Na2CO3溶液;
综上可知:①为NaOH溶液、②为酚酞溶液、④为稀硫酸、③为Na2CO3溶液;
(1)实验1中,③中稀硫酸与碳酸钠溶液反应生成二氧化碳气体,其反应方程式为:Na2CO3+H2SO4=Na2SO4+CO2↑+H2O;
故答案为:Na2CO3+H2SO4=Na2SO4+CO2↑+H2O;
(2)由分析可知:①为NaOH溶液、②为酚酞溶液、④为稀H2SO4、③为Na2CO3溶液;
故答案为:NaOH;酚酞;稀H2SO4;
(3)②中为NaOH溶液和酚酞的混合溶液,加硫酸,硫酸与NaOH反应,所以溶液的颜色由“红色变为无色”;
③为NaOH和Na2CO3的混合溶液,加稀硫酸,先与NaOH反应,然后再与Na2CO3溶液反应,所以加稀硫酸时“先无明显现象,之后有气泡产生”;
故答案为:稀硫酸中和NaOH溶液;稀硫酸先与NaOH反应,然后再与Na2CO3溶液反应.
点评 本题考查了物质的检验与鉴别,题目难度不大,侧重于考查学生的分析能力和实验探究能力,注意把握各物质之间的反应以及反应现象.


科目:高中化学 来源: 题型:推断题
| A | ①能使溴的四氯化碳溶液褪色;②比例模型为 ;③能与水在一定条件下反应生成C ;③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成;②球棍模型为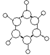 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与E反应生成相对分子质量为100的酯 |
| D | ①相对分子质量比C少2;②能由C氧化而成 |
| E | ①由C、H、O三种元素组成;②球棍模型为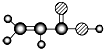 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
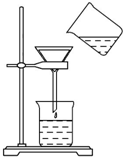 将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:
将含有少量氯化钾的硝酸钾固体提纯,某学生进行如图所示实验操作.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用硫酸铜溶液除去铁粉中混有的铜粉 | |
| B. | 用碳酸钙除去氯化钙溶液中混有的稀盐酸 | |
| C. | 用稀硫酸除去氯化钠中混有的碳酸钠 | |
| D. | 用点燃方法除去二氧化碳中混有的一氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| Zn的质量/g | Zn的形状 | 温度/℃ | 溶于酸的时间/s | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 45 | 25 |
| E | 2 | 薄片 | 45 | 25 |
| F | 2 | 薄片 | 15 | 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com