
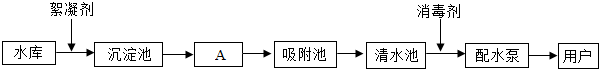
分析 (1)根据水库中水的组成分析其类别;
(2)①分离出液体和不溶物的操作方法为过滤;
②根据化合价原则、质量守恒定律分析回答;
③需要利用pH计测定溶液的酸碱度;
(3)根据氯离子的检验方法及水垢的成分分析回答;
(4)根据蒸馏的原理及注意的事项分析;
(5)对临时水源的水进行处理的方法为:先需要自然沉降、过滤,然后对过滤后的水进行消毒,最后加热煮沸后才能饮用.
解答 解:(1)由于水库中的水处于敞开的环境中,混入了一些物质,所以水库中的水属于混合物,
故答案为:混合物;
(2)①)A池中通过过滤除去水中的固体杂质,
故答案为:过滤;
②在二氧化氯(ClO2)中,由氧-2价,则氯的化合价是+4价;在Cl2+2NaClO2═2ClO2+2X方程式中左边有:氯原子、钠原子、氧原子的数目分别是4、2、2,在右边有氯原子、氧原子的数目分别是2、2、由质量守恒定律反应前后原子的种类及数目不变可知,X的化学式是NaCl,
故答案为:+4;NaCl;
③为了准确测定家用自来水的酸碱度,应用pH计来进行检测,
故答案为:pH计;
(3)自来水中通常都含有Cl-,可以在水样中滴加少量稀硝酸和硝酸银检验,若出现白色沉淀现象,说明水中含有Cl-;水中的Ca2+,Mg2+受热后转化为沉淀,即通常所说的水垢,水垢的主要成分为碳酸钙和氢氧化镁,
故答案为:硝酸银;白色沉淀;碳酸钙和氢氧化镁;
(4)可以利用沸点不同通过蒸馏的方法把自来水进一步净化为蒸馏水;蒸馏操作中通常加入碎瓷片或沸石,其目的是防止暴沸,
故答案为:蒸馏;防止暴沸;
(5)A.加热煮沸,通过加热除去水残留的消毒剂并降低水的硬度;B.消毒,加入消毒剂,杀灭水的病毒过;C.过滤,把水中不溶性固体杂质从水中除去;D.自然沉降,通过静置的方法使水中固体杂质沉至水底部,综上所述对临时水源的水进行处理的合理顺序是D、C、B、A,
故答案为:DCBA.
点评 本题考查了三废处理及环境保护、水的净化原理,题目难度中等,明确氧化还原反应原理、水的净化原理为解答关键,试题知识点较多、综合性较强,充分考查学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 推广使用燃煤脱硫技术,在燃煤中加入适量石灰石,可减少废气中的SO2 | |
| B. | 实施绿化工程,防治扬尘污染 | |
| C. | 研制开发燃料电池汽车,消除机动车尾气污染 | |
| D. | 加高工厂的烟囱,使烟尘和废气远离地表 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将2mol/L NaAlO2溶液和3mol/L的HCl溶液等体积互相均匀混合:6AlO2-+9H++3H2O═5Al(OH)3↓+Al3+ | |
| B. | 向1mol/L明矾溶液50mL中滴入数滴0.1mol/L Ba(OH)2溶液:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 | |
| D. | NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+═2Mn2++5NO3-+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 瘦肉精(Clenbuterol)是一种非常廉价的药品,对于减少脂肪增加瘦肉 (Lean Mass)作用非常好.但它有很危险的副作用,轻则导致心律不整,严重一点就会导致心脏病.瘦肉精是白色或类白色的结晶粉末,其结构简式如图,关于瘦肉精下列说法不正确的是( )
瘦肉精(Clenbuterol)是一种非常廉价的药品,对于减少脂肪增加瘦肉 (Lean Mass)作用非常好.但它有很危险的副作用,轻则导致心律不整,严重一点就会导致心脏病.瘦肉精是白色或类白色的结晶粉末,其结构简式如图,关于瘦肉精下列说法不正确的是( )| A. | 分子式为C12H18Cl2N2O | |
| B. | 该有机物含羟基、氯原子、氨基、肽键四种官能团 | |
| C. | 该有机物能发生催化氧化反应 | |
| D. | 该有机物核磁共振氢谱有7种类型氢原子的吸收峰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com