
【题目】已知六种物质:①H2O ②氨水③ Mg ④ HNO3 ⑤Ba(OH)2 ⑥CuSO4·5H2O
根据上述提供的物质,回答下列问题:
(1)属于电解质的是________(填序号,下同)。
(2)上述物质中④与⑤反应的离子方程式为_________。
(3)实验室配制900mL 0.1mol/L硫酸铜溶液,需要称取的溶质(从上述物质中选取)的质量为________g。在配制过程中,若其它操作均正确,则下列操作会使所配溶液物质的量浓度偏低的是_________(填字母序号)。
A 溶解后小烧杯、玻璃棒没有洗涤
B 所用容量瓶中,已有少量蒸馏水
C 定容摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线
D 定容时俯视刻度线
【答案】①④⑤⑥ H+ + OH -= H2O 25.0 AC
【解析】
(1)水溶液中或熔融状态下导电的化合物为电解质;
(2)④ HNO3 ⑤Ba(OH)2发生中和反应生成硝酸钡和水;
(3)根据n=cv计算溶质CuSO4的物质的量,利用CuSO4·5H2O的物质的量等于CuSO4的物质的量,根据m=nM计算CuSO4·5H2O的质量;分析操作的溶质的物质的量和溶液体积的影响,依据c=![]() 进行误差分析;
进行误差分析;
(1)①H2O部分电离成氢离子和氢氧根离子,属于弱电解质; ②氨水属于混合物;③ Mg是单质; ④ HNO3 电离成氢离子和硝酸根离子,属于强电解质;⑤Ba(OH)2 电离成钡离子和氢氧根离子,属于强电解质;⑥CuSO4·5H2O电离出铜离子和硫酸根离子,属于强电解质,属于电解质的是 ①④⑤⑥;故答案为:①④⑤⑥;
(2)④ HNO3 ⑤Ba(OH)2发生中和反应生成硝酸钡和水,④与⑤反应的离子方程式为:H+ + OH -= H2O;故答案为:H+ + OH -= H2O;
(3)配制溶液的体积为900ml,而容量瓶的规格没有900ml,只能选用1000ml容量瓶,CuSO4的物质的量n=cV=1.0L×0.1mol·L-1=0.1mol,CuSO4·5H2O的物质的量等于CuSO4的物质的量,所以CuSO4·5H2O的质量0.1mol×250g·mol-1=25.0g,故答案为:25.0g;
A.溶解后小烧杯、玻璃棒没有洗涤,导致部分溶质损耗,溶质的物质的量偏小,溶液浓度偏低,故A选;
B.所用容量瓶中,已有少量蒸馏水,对溶质的物质的量和溶液体积都不产生影响,溶液浓度不变,故B不选;
C.定容、加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度线,导致溶液体积偏大,溶液浓度偏低,故C选;
D.定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故D不选;
故选:AC;


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】恒温下,将a mol N2与b mol H2的混合气体通入一定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,
计算a=_______。
(2)反应达到平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的百分含量(体积分数)为25%。计算:平衡时NH3的物质的量为_____________。
(3)原混合气体与平衡混合气体的总物质的量之比
n(始): n(平)=____________。
(4)原混合气体中a : b=_______________。
(5)达到平衡时,N2和H2的转化率![]() (N2):
(N2):![]() (H2)=______________。
(H2)=______________。
(6)平衡混合气体中n(N2): n(H2): n(NH3)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11,若体积可以加和,则V (Ba(OH)2):V( NaHSO4)为( )
A.1:1B.1:4C.2:1D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国人自古就有泡药酒的习惯。药酒多选用50-60度的白酒,将中药材浸泡在酒中,经过一段时间,中药材中的有效成分(主要是有机物)溶解在酒中,此时即可过滤去渣后饮用。泡药酒的原理属于

A.萃取B.结晶C.干燥D.置换
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图示,下列与此原理有关说法错误的是
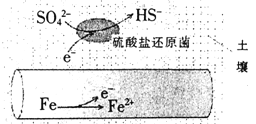
A. 正极反应为:SO42-+5H2O+8e-=HS-+9OH-
B. 输送暖气的管道不易发生此类腐蚀
C. 这种情况下,Fe腐蚀的最终产物为Fe2O3·xH2O
D. 管道上刷富锌油漆可以延缓管道的腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图所示装置进行实验,填写有关现象及化学方程式。
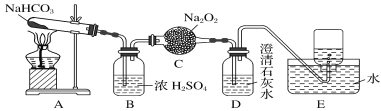
(1) D装置的作用是________,E中收集的气体是___________ (填名称)。
(2) 浓硫酸的作用是 _____________。
(3) A中发生反应的化学方程式为____________。
(4) C中发生反应的化学方程式为_________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家在 20℃时,将水置于足够强的电场中,水分子瞬间凝固成“暖冰”。对“暖冰”与其它物质比较正确的是( )
A.与Na2O 晶体类型相同B.与![]() 化学键类型相同
化学键类型相同
C.与CO2 分子构型相同D.与 CH4 分子极性相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知单质铜与稀硝酸的反应为3Cu+8HNO3===2NO↑+4H2O+3Cu(NO3)2(Cu的相对原子质量为64)。现把19.2 g Cu放入200 mL 5 mol·L-1硝酸中,充分反应,问:
(1)哪种物质过量?______
(2)参加反应的硝酸的物质的量为多少?______
(3)在标准状况下产生的气体的体积为多少?______
(4)生成水的分子数为多少?______
(5)若反应前后溶液的体积不变,则生成Cu(NO3)2的物质的量浓度为多少?______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下的一密闭容器中事先放入1.56g过氧化钠,然后再通入乙烷与氧气的混合气体,用电火花引爆,直至反应完全为止,恢复到原温度,容器内压强近似为零。
(1)相同条件下,通入的气体氧气和乙烷的体积比是多少?_____
(2)通入氧气的质量最大应是多少?_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com