
| A��Na2O2�ڷ�Ӧ��ֻ�������� |
| B��Na2FeO4�������������ǻ�ԭ���� |
| C��O2�ǻ�ԭ���� |
| D��2molFeSO4������Ӧʱ����Ӧ�й���8mol����ת�� |

 ʱ�����ڿ����У����桰���ơ������û�ѧ����ʽ��ʾԭ�� ��
ʱ�����ڿ����У����桰���ơ������û�ѧ����ʽ��ʾԭ�� �� �Լ�������ʳ�����ȫ����Ҫ��pH= ��Ҫ����2λ��Ч���֣�����֪��Һ������Ũ��С��10-5mol/Lʱ�������ӿɿ���������ȫ��lg2=0.3��
�Լ�������ʳ�����ȫ����Ҫ��pH= ��Ҫ����2λ��Ч���֣�����֪��Һ������Ũ��С��10-5mol/Lʱ�������ӿɿ���������ȫ��lg2=0.3�� ���100��1�ž�ϵ�д�
���100��1�ž�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
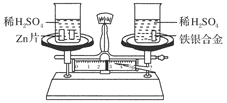
| A��65 ��56 | B��56 ��108 |
| C��56 ��9 | D��65 ��9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
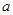 g����ͭ��Һ
g����ͭ��Һ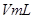 ������Һ������
������Һ������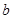 gˮ��ָ���20��C��ǡ��ȫ����������ͭ����
gˮ��ָ���20��C��ǡ��ȫ����������ͭ����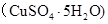 �������й�ϵʽ�������
�������й�ϵʽ�������A��ԭ����ͭ��Һ���ܶ�Ϊ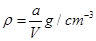 |
B��ԭ����ͭ��Һ�����ʵ���Ũ��Ϊ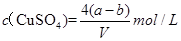 |
C��ԭ����ͭ��Һ��������������Ϊ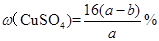 |
D����������ͭ��������ʵ���Ϊ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
 eCO3��ijѧϰС����������ʵ�飺
eCO3��ijѧϰС����������ʵ�飺 ��������ʲô��
��������ʲô���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ͭ��������Һ����Cu2+��Fe2+��Fe3+���� |
| B������ͭ��������Һ����Cu2+��Fe2+���ӣ�Ҳ������Fe3+���� |
| C������ͭ��������Һ����Fe2+���ӣ�û��Cu2+��Fe3+���� |
| D������ͭ��������Һ����Fe2+���ӣ�������Cu2+���ӣ�Ҳ������Fe3+���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NO3�� | B��Fe3�� | C��SO42�� | D��Mg2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ʵ���ҽϳ�ʱ�䱣��FeSO4��Һ�����Լ�����ϡ��������� |
| B��������Һ�е�Fe2+���ȼ���KSCN��Һ���ټ�����ˮ |
| C����ҵ��ʴͭ��ӡˢ��·��ʱ�����Ļ�ѧ��Ӧ��Fe+Cu2+=Fe2++Cu |
| D����ȥFeCl2��Һ�е�FeCl3����ȥFeSO4��Һ�е�Fe2(SO4)3�������Լ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com