
下列有关物质的性质和该性质的应用均正确的是
A.NH3溶于水后显碱性,在FeCl3饱和溶液中通入足量NH3可制取Fe(OH)3胶体
B.NaHCO3能与碱反应,食品工业上用作焙制糕点的膨松剂
C.Mg(OH)2分解吸热且生成高熔点固体,可用作阻燃剂
D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
科目:高中化学 来源:2015-2016学年广西钦州港经济开发区中学高一上12月月考化学试卷(解析版) 题型:选择题
有温度和容积均相同的两容器Ⅰ、Ⅱ,向Ⅰ中加入1 mol NO 2 ,Ⅱ中加入2 mol NO 2 ,都将发生反应2 NO 2 (g) N 2 O 4 (g),反应达到平衡时,测得Ⅰ中NO 2 的转化率为a%,Ⅱ中NO 2 的转化率为b%,则a、b的关系为
N 2 O 4 (g),反应达到平衡时,测得Ⅰ中NO 2 的转化率为a%,Ⅱ中NO 2 的转化率为b%,则a、b的关系为
A.a<b B.a>b C.a=b D.无法确定
查看答案和解析>>
科目:高中化学 来源:2016届广东省顺德市高三上第四次月考理综化学试卷(解析版) 题型:选择题
部分弱电解质的电离平衡常数如下表:
弱电解质 | HCOOH | HCN | H2CO3 | NH3·H2O |
电离平衡常数 (25 ℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Kb=1.8×10-5 |
下列说法不正确的是
A.结合H+的能力:CO32->CN->HCO3->HCOO-
B.0.1mol/L的HCOONH4溶液中:c(HCOO-)>c(NH4+)>c(H+)>c(OH-)
C.25 ℃时,pH=3的盐酸与pH=11的氨水混合,若溶液显中性,则二者消耗的体积是:V(盐酸)>V(氨水)
D.HCN + HCOONa = NaCN + HCOOH
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上12月月考化学试卷(解析版) 题型:选择题
下列各组离子在指定溶液中可能大量共存的是
①无色透明溶液中:K+、Ca2+、MnO4-、SO42-
②pH=11的溶液中:CO32-、Na+、 [Al(OH)]4-、NO3-
③加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+
④由水电离出的c(OH-) =10-4mol·L-1的溶液中:NH4+、Al3+、Cl-、Br-
⑤有较多Fe3+的溶液中:Na+、NH4+、SCN-、Cl-
⑥酸性溶液中:Fe2+、Al3+、NO3-、I-、Cl-
A.①②④ B.③⑥ C.②④ D.①③⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016届浙江省金丽衢十二校高三上学期第一次联考化学试卷(解析版) 题型:填空题
中科院大连化学物理研究所的“煤基甲醇制取低碳烯烃技术(简称DMTO)”荣获2014年度国家技术发明一等奖。DMTO技术主要包括煤的气化、液化、烯烃化三个阶段,相关反应的热化学方程式如下:
(i)煤气化制合成气:C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
(ii)煤液化制甲醇:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
(iii)甲醇制取低碳烯烃:2CH3OH(g) C2H4(g)+2H2O(g) ΔH= -11.72kJ·mol-1……(a)
C2H4(g)+2H2O(g) ΔH= -11.72kJ·mol-1……(a)
3CH3OH(g) C3H6(g)+3H2O(g) ΔH= -30.98kJ·mol-1……(b)
C3H6(g)+3H2O(g) ΔH= -30.98kJ·mol-1……(b)
回答下列问题:
(1)已知:C(s)+CO2(g)=2CO(g) ΔH= +172.5kJ·mol-1,
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH= -41.0kJ·mol-1
反应(i)能自发进行的条件是 (填“高温”、“低温”或“任何温度”)。
(2)反应(ii)中以氢碳[n(H2)∶n(CO)]投料比为2制取甲醇,温度、压强与CO的平衡转化率关系如下图1。
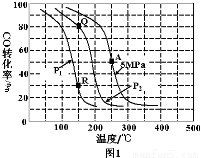
①对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度c(B),则A点时反应(ii)的Kp= (保留两位有效数字,分压=总压×物质的量分数)。
②比较P1 P2,Kp(Q) Kp(R)(填“大于”、“小于”或“等于”)。
③工业上常以铜基催化剂,压强5MPa,温度275℃下发生反应(ii),CO转化率可达到40%左右。为提高CO转化率除了可以适当改变反应温度和压强外,还可以采取的措施有 (写出2个)。
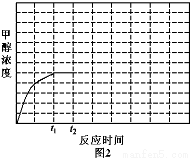
④若反应(ii)在恒容密闭容器内进行,T1温度下甲醇浓度随时间变化曲线如图2所示;不改变其他条件,假定t2时刻迅速降温到T2,t3时刻体系重新达到平衡。试在图中画出t2时刻后甲醇浓度随时间变化趋势图(在图中标出t3)。
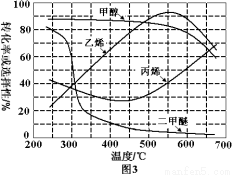
(3)烯烃化阶段:在常压和某催化剂作用下,甲醇的平衡转化率及乙烯、丙烯等物质的选择性(指除了水蒸气以外的产物中乙烯、丙烯等物质的物质的量分数)与反应温度之间的关系如图3。为尽可能多地获得乙烯,控制反应温度为550℃的理由是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高一上第二次月考化学试卷(解析版) 题型:选择题
硫酸铁和硫酸亚铁的混合物中,若其中铁元素的质量分数为a%,则其中硫元素的质量分数为
A.(100-3a)% B.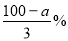 C.
C.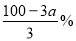 D.
D.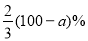
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三上学期月考化学试卷(解析版) 题型:选择题
下列说法正确的是
① 标准状况下,6.02×1023个分子所占的体积约是22.4L
②0.5molH2所占体积为11.2L
③标准状况下,1molH2O的体积为22.4L
④标准状况下,28gCO与N2的混合气体的体积约为22.4L
⑤各种气体的气体摩尔体积都约为22.4L/mol
⑥标准状况下,体积相同的气体的分子数相同
A.①③⑤ B.④⑥ C.③④⑥ D.①④⑥
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南省高二上第三次月考化学试卷(解析版) 题型:选择题
某温度下,对于反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是
2NH3(g) ΔH=-92.4kJ/mol。N2的平衡转化率(α)与体系总压强(p)的关系如图所示。下列说法正确的是
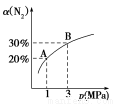
A.将1 mol氮气、3 mol氢气,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ
B.平衡状态由A变到B时,平衡常数K(A)<K(B)
C.上述反应在达到平衡后,增大压强,H2的转化率增大
D.升高温度,平衡向逆反应方向移动,说明逆反应速率增大,正反应速率减小
查看答案和解析>>
科目:高中化学 来源:2016届山东省北校高三上学期第二次单元测试化学试卷(解析版) 题型:实验题
(一)如图所示,甲、乙是电化学实验装置,请回答下列问题:
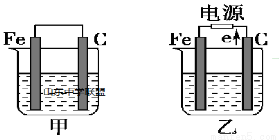
若甲、乙两个烧杯中均盛放饱和NaCl溶液。
①甲中石墨棒上的电极反应式是_________________________________
②乙中总反应的离子方程式为___________________________________
③若乙中含有0.10 mol·L-1NaCl溶液400mL,当阳极产生的气体为560mL(标准状况下)时,溶液的pH=_____________(2分)(假设溶液体积变化忽略不计),转移电子的个数为____________
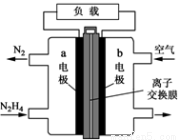
(二)肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景。其工作原理如上图所示,回答下列问题:
①该燃料电池中正极通入的物质是__________;
负极发生的反应式为:__________________________
②电池工作时,OH- 移向极________(“a”或“b”)
③当电池放电转移5mol电子时,至少消耗燃料肼________g
(三)全钒液流电池的结构如图所示,其电解液中含有钒的不同价态的离子、H+和SO42﹣.电池放电时,负极的电极反应为:V2+﹣e﹣=V3+.
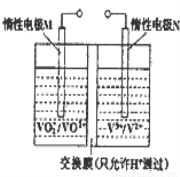
①电池放电时的总反应方程式为___________________________
充电时,电极M应接电源的_________ 极
②若电池初始时左、右两槽内均以VOSO4和H2SO4的混合液为电解液,使用前 需先充电激活,充电过程阴极区的反应分两步完成:第一步VO2+转化为V3+;第二步V3+转化为V2+.则第一步反应过程中阴极区溶液n(H+)_________ _(填“增大”、“不变”或“减小”) (1分),阳极的电极反应式为_________________________
_(填“增大”、“不变”或“减小”) (1分),阳极的电极反应式为_________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com