


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 |
| B、用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度 |
| C、石油的分馏是物理变化,而煤的干馏是化学变化 |
| D、将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
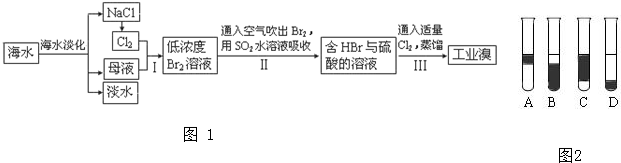
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)铁、铝、铜是人类使用广泛的三种金属.
(1)铁、铝、铜是人类使用广泛的三种金属.| 原料 | 杂木屑 | 麦麸 | 生石灰(粉) | 过磷酸钙 |
| 质量(kg) | 200 | 50 | 2.5 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元 素 | Mn | Fe | |
| 电离能 /kJ?mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
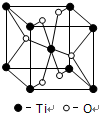
查看答案和解析>>
科目:高中化学 来源: 题型:
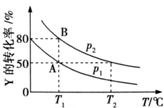 在一固定容积的密闭容器中加入X、Y、Z三种气体,保持一定温度,不同时刻测得X、Y、Z三种物质的物质的量如表所示.
在一固定容积的密闭容器中加入X、Y、Z三种气体,保持一定温度,不同时刻测得X、Y、Z三种物质的物质的量如表所示.| 测定时间/s | t1 | t2 | t3 | t4 |
| n(X)/mol | 7 | 3 | 1 | 1 |
| n(Y)/mol | 5 | 3 | 2 | 2 |
| n(Z)/mol | 1 | 3 | 4 | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com