
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年广东省高二上期中测试化学试卷(解析版) 题型:选择题
工业上制备纯硅的热化学方程式如下:SiCl4(g)+2H2(g)=Si(s)+4HCl(g) ΔH=+Q KJ·mol-1(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行反应,下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1 mol,则在平衡时,吸收热量为Q kJ
C.将反应的温度由T1升高至T2,则对应温度下的平衡常数K1> K2
D.当反应吸收热量为0.25 Q kJ时,生成的HCl恰好与1 mol NaOH反应
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省高三上学期期中测试化学试卷(解析版) 题型:选择题
混合下列各组物质使之充分反应,加热蒸干产物并高温下灼烧至质量不变,最终残留固体为纯净物的是( )
A.向CuSO4溶液中加入适量铁粉
B.等物质的量浓度、等体积的FeCl3与KI溶液混合
C.物质的量之比为2:1的NaHCO3与Na2O2溶于水
D.在Na2SiO3溶液中通入过量CO2气体
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高一上半期测试化学试卷(解析版) 题型:选择题
某反应可用下式表示: xR2+ + yH+ + O2 == mR3+ + nH2O 。 则m的值为
A.2x B.4 C.y/2 D.7
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高一上12月段考化学试卷(解析版) 题型:推断题
有一包白色粉末,其中可能含有Ba(NO3)2、CaCl2、K2CO3,现做以下实验:
(1)将部分粉末加水中,振荡,有白色沉淀生成;
(2)向(1)的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
(3)取少量(2)的溶液滴入AgNO3溶液,有白色沉淀生成。
根据上述实验现象,判断原白色粉末中肯定含有什么物质,可能含有什么物质,写出各步反应的离子方程式。肯定有____________;可能含有____________
离子方程式:
(1)____________________________
(2)____________________________
(3)____________________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.离子晶体中,只存在离子键,不可能存在其它化学键
B.氧族元素(O、S、Se、Te)的氢化物的沸点依次升高
C.NaHSO4、Na2O2晶体中的阴阳离子个数比均为1∶1
D.晶体的硬度:金刚石>碳化硅>石英
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
下列对晶体类型判断正确的是( )
选项 | Na2B2O7 | CaF2 | H3BO3 | NH3 |
A | 原子晶体 | 金属晶体 | 原子晶体 | 分子晶体 |
B | 离子晶体 | 分子晶体 | 离子晶体 | 分子晶体 |
C | 离子晶体 | 离子晶体 | 分子晶体 | 分子晶体 |
D | 分子晶体 | 离子晶体 | 分子晶体 | 离子晶体 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上第二次质检化学试卷(解析版) 题型:选择题
实验室制取下列气体时,不能用排气法收集,而只能用排水法收集的是
A.NH3 B.Cl2 C.CO2 D.NO
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上12月月考化学试卷(解析版) 题型:填空题
碳和氮的化合物与人类生产、生活密切相关。
(1)在一恒温、恒容密闭容器中发生反应:Ni(s)+4CO(g) 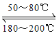 Ni(CO)4(g),△H<0;
Ni(CO)4(g),△H<0;
利用该反应可以将粗镍转化为纯度达99.9%的高纯镍。下列说法正确的是_______(填字母编号)。
A.增加Ni的量可提高CO的转化率,Ni的转化率降低
B.缩小容器容积,平衡右移,△H减小
C.反应达到平衡后,充入CO再次达到平衡时,CO的体积分数降低
D.当4v正[Ni(CO)4]=v正(CO)时或容器中混合气体密度不变时,都可说明反应已达化学平衡状态
(2)CO与镍反应会造成含镍催化剂的中毒.为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫.
已知:CO(g)+ 1/2O2(g)=CO2(g) △H=-Q1 kJ•mol-1
S(s) +O2(g) =SO2(g) △H=-Q2 kJ•mol-1
则SO2(g) +2CO(g) =S(s) +2CO2(g) △H=________________;
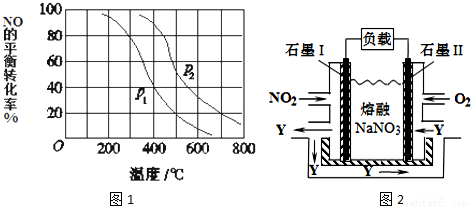
(3)对于反应:2NO(g)+O2═2NO2(g),向某容器中充入10mol的NO和10mol的O2,在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下随温度变化的曲线(如图1).
①比较P1、P2的大小关系_______________;
②700℃时,在压强为P2时,假设容器为1L,则在该条件平衡常数的数值为_______(最简分数形式);
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图2所示.该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为_______________;若该燃料电池使用一段时间后,共收集到20mol Y,则理论上需要消耗标准状况下氧气的体积为________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com