
【题目】根据要求完成下列问题:
(1)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,试回答:
该元素价电子排布式_____________________。
(2)外围电子排布式为3d54s2的原子,其原子结构示意图为____________,其最高正价为________;其在元素周期表中的位置为:___________________。
(3)下列分子中是否有手性原子:_________(填“有”或“无”,若有请在图中碳原子下方用“*”标出)
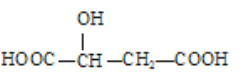
(4)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧、PCl3中,属于非极性分子的是(填番号)________________。
(5) 试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):
HClO3________HClO4; H3PO4________H3PO3。
【答案】 3d14s2  +7 第4周期VIIB族 有;
+7 第4周期VIIB族 有;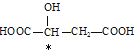 ①③④⑦ < >
①③④⑦ < >
【解析】(1)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,则该元素的核外电子数是18+1+2=21,所以该元素价电子排布式为3d14s2;(2)外围电子排布式为3d54s2的原子是Mn,其原子结构示意图为 ,其最高正价为+7价;其在元素周期表中的位置为第4周期VIIB族;(3)与羟基相连的碳原子连接的4个基团均不相同,属于手性碳原子;(4)①CO2直线形结构,属于非极性分子;②NH3是三角锥形,是极性分子;③CCl4是正四面体型,是非极性分子;④BF3是平面三角形,是非极性分子;⑤H2O是V形,是极性分子;⑥SO2是V形,是极性分子;⑦SO3是平面三角形,是非极性分子;⑧PCl3是三角锥形,是极性分子,因此属于非极性分子的是①③④⑦;(5) 氯酸分子中非羟基氧原子个数小于高氯酸中非羟基氧原子个数,因此氯酸的酸性小于高氯酸;同样磷酸的酸性强于亚磷酸。
,其最高正价为+7价;其在元素周期表中的位置为第4周期VIIB族;(3)与羟基相连的碳原子连接的4个基团均不相同,属于手性碳原子;(4)①CO2直线形结构,属于非极性分子;②NH3是三角锥形,是极性分子;③CCl4是正四面体型,是非极性分子;④BF3是平面三角形,是非极性分子;⑤H2O是V形,是极性分子;⑥SO2是V形,是极性分子;⑦SO3是平面三角形,是非极性分子;⑧PCl3是三角锥形,是极性分子,因此属于非极性分子的是①③④⑦;(5) 氯酸分子中非羟基氧原子个数小于高氯酸中非羟基氧原子个数,因此氯酸的酸性小于高氯酸;同样磷酸的酸性强于亚磷酸。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】黄铜灰渣(含有Cu、Zn、CuO、ZnO及少量的FeO、Fe2O3)生产氯化铜晶体的流程如下:
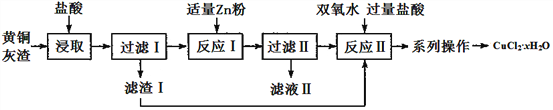
(1)反应Ⅰ中所加Zn粉不能过量的原因是______________________
(2)滤液Ⅱ中含有的主要金属阳离子是___________________
(3)写出反应Ⅱ的化学方程式_________________________
(4)“系列操作”包括蒸发浓缩、冷却结晶、过滤、__________、___________。
(5)在空气中直接加热CuCl2·xH2O晶体得不到纯的无水CuCl2,原因是____________________(用化学方程式表示)
(6)CuCl2·xH2O晶体中x值的测定:称取3.420g产品溶解于适量水中,向其中加入含AgNO3 4.400×10-2mol的AgNO3溶液(溶液中除Cl- 外,不含其它与Ag+反应的离子),待Cl- 完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol·L-1的KSCN标准溶液滴定剩余的AgNO3。使剩余的Ag+以AgSCN白色沉淀的形式析出。
①滴定终点的现象是______________________。
②若滴定过程用去上述浓度的KSCN标准溶液20.00mL,则CuCl2·xH2O 中x值为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取100 mL 1.0mol·L-1和200 mL 2.0 mol·L-1的盐酸混合后,全部注入500 mL的容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是( )
A.0.5 mol·L-1 B.1.0 mol·L-1 C.1.5. mol·L-1 D.2.0 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素互化物与卤素单质性质相似。已知CH2=CH—CH=CH2(1,3-丁二烯)与氯气发生1:1加成产物有两种:
①CH2Cl—CHCl—CH=CH2 (1,2-加成)
②CH2Cl—CH=CH—CH2Cl (1,4-加成)
据此推测CH2=C(CH3)—CH=CH2(异戊二烯)与卤素互化物BrCl的1:1加成产物有(不考虑顺反异构和镜像异构)
A. 6种B. 7种C. 8种D. 9种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题(用化学用语表示):
![]()
(1)在这些元素中,化学性质最不活泼的是____________,其原子结构示意图为____________。元素K是____________,在周期表中的位置是__________________。
(2)最高价氧化物对应水化物中碱性最强的化合物是______________。
(3)某元素二价阳离子的核外有10个电子,该元素是__________。
(4)G、H、I形成的简单气态氢化物稳定性由强到弱的顺序是______________________________。
(5)F、H、J的最高价氧化物对应水化物的酸性由强到弱的顺序是______________________。
(6)I、J、K三种元素形成的离子,离子半径由大到小的顺序是________________________。
(7)元素I的氢化物的结构式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷和氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下图所示:

根据要求填空:
(1)B装置有三种功能:①控制气流速度;②干燥混合气体;③________________。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应____________。
(3)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:____________________________________。
(4)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为___________。该装置的主要缺陷是 。
(5)已知丁烷与氯气的取代反应的产物之一为C4H8Cl2,其有 种同分异构体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用试纸检验气体是一种重要的实验方法.下列试纸的选用以及对应的现象、结论都正确的一项是( )
A.用干燥的pH试纸检验CO2
B.用干燥的红色石蕊试纸检验NH3
C.SO2能使湿润的品红试纸褪色
D.能使湿润的淀粉碘化钾试纸变蓝的气体一定是氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作正确的是
A.蒸馏实验中温度计的水银球应插入液态混合物中
B.用酒精萃取碘水中的碘
C.分液时,打开旋塞,使下层液体从下口流出,上层液体从上口倒出
D.开始蒸馏时,应该先加热,再开冷凝水;蒸馏完毕,应先关冷凝水再撤酒精灯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com