
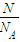 计算H2SO4分子的物质的量,根据m=nM计算H2SO4的质量;
计算H2SO4分子的物质的量,根据m=nM计算H2SO4的质量;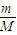 计算1.7g氨气的物质的量,利用V=nVm计算氨气体积;氨气中H原子的物质的量为氨气的3倍,计算出H原子物质的量,H2S中H原子物质的量为H2S的2倍,所以2n(H2S)=3n(NH3),据此计算n(H2S),再利用V=nVm计算H2S体积;
计算1.7g氨气的物质的量,利用V=nVm计算氨气体积;氨气中H原子的物质的量为氨气的3倍,计算出H原子物质的量,H2S中H原子物质的量为H2S的2倍,所以2n(H2S)=3n(NH3),据此计算n(H2S),再利用V=nVm计算H2S体积;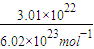 =0.05mol,质量为0.05mol×98g/mol=4.9g,
=0.05mol,质量为0.05mol×98g/mol=4.9g,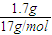 =0.1mol,标准状况下,1.7g氨气所占的体积为0.1mol×22.4L/mol=2.24L,
=0.1mol,标准状况下,1.7g氨气所占的体积为0.1mol×22.4L/mol=2.24L, n(NH3)=
n(NH3)= ×0.1mol=0.15mol,所以V(H2S)=0.15mol×22.4L/mol=3.36L,
×0.1mol=0.15mol,所以V(H2S)=0.15mol×22.4L/mol=3.36L,

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(08皖南八校模拟)已知2SO![]() (g)+O
(g)+O![]() (g)
(g)![]() 2SO
2SO![]() (g);△H=-197kJ/mol,同温下,往相同体积的密闭容器甲、乙中分别充入2molSO
(g);△H=-197kJ/mol,同温下,往相同体积的密闭容器甲、乙中分别充入2molSO![]() 、1molO
、1molO![]() 和1molSO
和1molSO![]() 、1molSO
、1molSO![]() 、0.5molO
、0.5molO![]() ,当它们分别达到平衡时放出的热量为Q
,当它们分别达到平衡时放出的热量为Q![]() kJ和Q
kJ和Q![]() KJ,则下列比较正确的是:()
KJ,则下列比较正确的是:()
A.Q![]() <1/2Q
<1/2Q![]() <98.5 B.Q
<98.5 B.Q![]() <1/2Q
<1/2Q![]() <=98.5
<=98.5
C.1/2Q![]() <Q
<Q![]() <98.5 D.Q
<98.5 D.Q![]() =1/2Q
=1/2Q![]() <98.5
<98.5
查看答案和解析>>
科目:高中化学 来源: 题型:
(08皖南八校模拟)已知2SO![]() (g)+O
(g)+O![]() (g)
(g)![]() 2SO
2SO![]() (g);△H=-197kJ/mol,同温下,往相同体积的密闭容器甲、乙中分别充入2molSO
(g);△H=-197kJ/mol,同温下,往相同体积的密闭容器甲、乙中分别充入2molSO![]() 、1molO
、1molO![]() 和1molSO
和1molSO![]() 、1molSO
、1molSO![]() 、0.5molO
、0.5molO![]() ,当它们分别达到平衡时放出的热量为Q
,当它们分别达到平衡时放出的热量为Q![]() kJ和Q
kJ和Q![]() KJ,则下列比较正确的是:()
KJ,则下列比较正确的是:()
A.Q![]() <1/2Q
<1/2Q![]() <98.5 B.Q
<98.5 B.Q![]() <1/2Q
<1/2Q![]() <=98.5
<=98.5
C.1/2Q![]() <Q
<Q![]() <98.5 D.Q
<98.5 D.Q![]() =1/2Q
=1/2Q![]() <98.5
<98.5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com