
| ������ | Na+ H+ Ba2+ |
| ������ | OH- CO32-SO42- |


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѹǿ/MPa ת����/% �¶�/�� | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
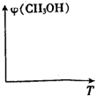 ��ҵ���ںϳ����в������з�Ӧ�ϳɼ״���CO��g��+2H2��g��?CH3OH��g����H=QkJ/mol
��ҵ���ںϳ����в������з�Ӧ�ϳɼ״���CO��g��+2H2��g��?CH3OH��g����H=QkJ/mol| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
| ���� | �� | �� | �� | |
| ��Ӧ��Ͷ���� | 1mol CO 2mol H2 | 1mol CH3OH | 2mol CH3OH | |
| ƽ �� ʱ �� �� | CH3OH��Ũ�ȣ�mol?L-1�� | c1 | c2 | c3 |
| ��Ӧ���ջ�ų���������KJ�� | a | b | c | |
| ��ϵѹǿ��Pa�� | P1 | P2 | P3 | |
| ��Ӧ��ת���� | ��1 | ��2 | ��3 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| N | F | |||||
| Mg | Al | S | Cl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ѡ�� | ʵ����� | ʵ������ | ���� |
| A | ���������Һ�еμ�1�η�̪��Ȼ����μ���ϡ��������ɫ��ȥ | 2min���Թ���������� | ���ԣ�������� |
| B | �ھƾ����ϼ������� | �����ۻ��������� | �۵㣺���������� |
| C | �����£���Ũ������Ͷ����Ƭ | ��Ƭ���ܽ� | �����£�������Ũ���ᷴӦ |
| D | ��ij��Һ���ȵμ�KSCN��Һ���ٵμ�������ˮ | ��������������Һ���Ѫ��ɫ | ��Һ�к���Fe2+��û��Fe3+ |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��N2��O2��CO2��H2 |
| B��N2��H2��H2O��g����CO |
| C��NH3��Cl2��HCl��H2 |
| D��CO��CO2��O2��HCl |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com