
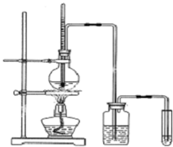
 如图是实验室制乙烯并检验其性质的装置图,请回答:
如图是实验室制乙烯并检验其性质的装置图,请回答:分析 实验室制备乙烯所用的原料为乙醇,在浓硫酸作用下,乙醇发生消去反应生成乙烯,乙烯含有碳碳双键,可发生加成、氧化反应,以此解答该题.
解答 解:(1)利用乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,反应为CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;
(2)高锰酸钾具有强氧化性,乙烯含有不饱和键,C=C双键,能被高锰酸钾溶液氧化,C=C双键,能卤素单质发生加成反应,乙烯易和溴加成生成1,2-二溴乙烷,
故答案为:高锰酸钾溶液(或溴的四氯化碳溶液).
点评 本题考查了乙烯的实验室制法并检验乙烯性质,为高频考点,侧重于学生的分析、实验能力的考查,掌握反应的原理和乙烯的化学性质以及以及有关实验操作是解答本题的关键,题目较简单.


 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:高中化学 来源: 题型:选择题
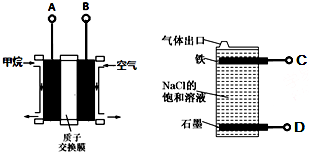
| A. | 燃料电池的A极连接电解池的C极 | |
| B. | 燃料电池工作时当0.2 NA个H+通过质子交换膜移向右边,饱和食盐水中可产生2.24L气体 | |
| C. | A电极的电极反应式为:CH4-8e-+2H2O═CO2+8H+ | |
| D. | 电解池总反应式为NaCl+H2O$\frac{\underline{\;电解\;}}{\;}$NaClO+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表是按相对原子质量逐渐增大的顺序从左到右排列的 | |
| B. | 最外层电子数相同的元素一定属于同一族 | |
| C. | 非金属元素的最外层电子数都大于或等于4 | |
| D. | 同周期元素的电子层数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在平衡常数表达式中,反应物浓度用起始浓度表示,生成物浓度用平衡浓度表示 | |
| B. | 平衡常数越大,表示化学反应速率越大 | |
| C. | 可以用化学平衡常数来定量描述化学反应的限度 | |
| D. | 平衡常数的大小与温度、浓度、压强、催化剂有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2与O3互为同位素 | |
| B. | O2与O3的相互转化是物理变化 | |
| C. | 等质量的O2与O3含有相同的质子数 | |
| D. | 在相同的温度与压强条件下,等体积的O2与O3含有相同的原子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com