
| A. | 铁粉作食品袋内的脱氧剂 | B. | 用生石灰做干燥剂 | ||
| C. | 漂粉精作消毒剂 | D. | 明矾作净水剂 |
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 沸腾炉 | B. | 吸收塔 | C. | 高炉 | D. | 接触室 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行实验并得到下表实验结果:
某研究性学习小组欲探究原电池的形成条件,按如图所示装置进行实验并得到下表实验结果:
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
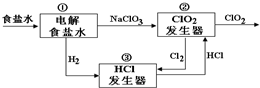 利用食盐水制取ClO2的工业流程如图所示,装置①中的反应:NaCl+3H2O$\frac{\underline{\;电解\;}}{\;}$NaClO3+3H2↑;装置②中的反应:2NaClO3+4HCl$\frac{\underline{\;电解\;}}{\;}$ClO2+Cl2↑+2NaCl+2H2O.下列关于该流程说法不正确的是( )
利用食盐水制取ClO2的工业流程如图所示,装置①中的反应:NaCl+3H2O$\frac{\underline{\;电解\;}}{\;}$NaClO3+3H2↑;装置②中的反应:2NaClO3+4HCl$\frac{\underline{\;电解\;}}{\;}$ClO2+Cl2↑+2NaCl+2H2O.下列关于该流程说法不正确的是( )| A. | 该流程中Cl2、NaCl都可以循环利用 | |
| B. | 装置①中H2是阴极产物 | |
| C. | 装置②发生的反应中,Cl2是氧化产物,NaCl是还原产物 | |
| D. | 为了使H2完全转化为HCl,需要向装置③中补充Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{1.5}{n}$ | B. | $\frac{n}{1.5}$ | C. | 1.5n | D. | $\frac{3}{n}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 弱电解质 | HCl | CH3COOH | HClO | Ca(OH)2 |
| 强电解质 | H3PO4 | FeCl3 | BaSO4 | HNO3 |
| 非电解质 | CH4 | Cu | C2H5OH | H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6 g铁与足量的氯气反应失去的电子为0.2 mol | |
| B. | 25℃、pH=0的溶液中,Al3+、NH4+、NO3-、Fe2+可以大量共存 | |
| C. | 2Fe3++Fe═3Fe2+成立说明氧化性:Fe3+>Fe2+ | |
| D. | 硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+═Fe3++4H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com