
ЁОЬтФПЁПФГбЇЯАаЫШЄаЁзщЯыРћгУИпСыЭСЃЈЦфжївЊГЩЗжЪЧAl2O32SiO22H2OЃЉжЦБИаТаЭЕФОЛЫЎМСЃЎЪЕбщСїГЬШчЭМЃК 
ЦфжаТЫвКCОЭЪЧгћжЦБИЕФОЛЫЎМСЃЎЪдЭъГЩЯТСаЮЪЬтЃК
ЃЈ1ЃЉЛьКЯЮяAЁЂBЃЌТЫвКCЁЂГСЕэDЕФжївЊГЩЗжЃКAЃЛBЃЛCD ЃЎ
ЃЈ2ЃЉаДГіИпСыЭСгыДПМюМгШШШлШкЕФСНИіЛЏбЇЗНГЬЪНЃКЁЂ
ЃЈ3ЃЉИУЪЕбщжаЃЌШлШкИпСыЭСЁЂДПМюЕФЛьКЯЮяПЩвдбЁгУЕФлсліга ЃЎ
A.ВЃСЇлслі
B.ДЩлслі
C.бѕЛЏТСлслі
D.ЬњлсліЃЎ
ЁОД№АИЁП
ЃЈ1ЃЉNaAlO2КЭNa2SiO3ЃЛAlCl3КЭH2SiO3ЃЛAlCl3ЃЛH2SiO3
ЃЈ2ЃЉNa2CO3+Al2O3 ![]() ?2NaAlO2+CO2ЁќЃЛNa2CO3+SiO2
?2NaAlO2+CO2ЁќЃЛNa2CO3+SiO2 ![]() ?Na2SiO3+CO2Ёќ
?Na2SiO3+CO2Ёќ
ЃЈ3ЃЉD
ЁОНтЮіЁПНтЃКЃЈ1ЃЉбѕЛЏТСКЭЖўбѕЛЏЙшдкИпЮТШлШкзДЬЌЯТгыДПМюЗДгІЩњГЩAГЩЗжЮЊЙшЫсФЦКЭЦЋТСЫсФЦЃЌAжаМгЫЎШмНтВЂЙ§ТЫКѓЕУЕНЕФжївЊЪЧЙшЫсФЦгыЦЋТСЫсФЦЕФЛьКЯвКЃЌAЮЊNaAlO2КЭNa2SiO3 ЃЌ ЕЮМгЙ§СПбЮЫсЛсЩњГЩЙшЫсГСЕэКЭТШЛЏТСШмвКЃЌBЮЊAlCl3КЭH2SiO3ЕФЛьКЯЮяЃЌЙ§ТЫКѓЕФВЛШмЮяГСЕэDЮЊH2SiO3 ЃЌ ТЫвКCЮЊAlCl3ШмвКЃЌ ЫљвдД№АИЪЧЃКNaAlO2КЭNa2SiO3ЃЛAlCl3КЭH2SiO3ЃЛAlCl3ЃЛH2SiO3ЃЛЃЈ2ЃЉбѕЛЏТСвдМАЖўбѕЛЏЙшгыЬМЫсФЦЕФЗДгІЮЊЃКNa2CO3+Al2O3 ![]() 2NaAlO2+CO2ЁќЁЂNa2CO3+SiO2
2NaAlO2+CO2ЁќЁЂNa2CO3+SiO2 ![]() Na2SiO3+CO2ЁќЃЌ
Na2SiO3+CO2ЁќЃЌ
ЫљвдД№АИЪЧЃКNa2CO3+Al2O3 ![]() 2NaAlO2+CO2ЁќЁЂNa2CO3+SiO2
2NaAlO2+CO2ЁќЁЂNa2CO3+SiO2 ![]() Na2SiO3+CO2ЁќЃЛЃЈ3ЃЉДЩлсліЁЂВЃСЇлсліЕФГЩЗжжаКЌгаЖўбѕЛЏЙшЃЌФмКЭДПМюЗЂЩњЗДгІЃЌбѕЛЏТСлслівВФмКЭДПМюЗЂЩњЗДгІЃЌдкМгШШЪБЗДгІвзЪЙлсліеЈСбЃЌдђгІбЁдёЬњлсліЃЌ
Na2SiO3+CO2ЁќЃЛЃЈ3ЃЉДЩлсліЁЂВЃСЇлсліЕФГЩЗжжаКЌгаЖўбѕЛЏЙшЃЌФмКЭДПМюЗЂЩњЗДгІЃЌбѕЛЏТСлслівВФмКЭДПМюЗЂЩњЗДгІЃЌдкМгШШЪБЗДгІвзЪЙлсліеЈСбЃЌдђгІбЁдёЬњлсліЃЌ
ЫљвдД№АИЪЧЃКDЃЎ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪвЮТЯТЃЌНЋЬМЫсФЦШмвКМгШШжС70ЁцЃЌЦфНсЙћЪЧ(ЁЁЁЁ)
A. ШмвКжаc(CO32-)діДѓ B. ЫЎЕФЕчРыГЬЖШВЛБф
C. ШмвКЕФpHНЋБфаЁ D. ШмвКЕФМюаддіЧП
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЭМЪОжаЮяжЪзЊЛЏзюжеЩњГЩввЫсКЭИпЗжзгЭПСЯНК№ЄМСYЕФКЯГЩТЗЯпШчЯТЃЈВПЗжЗДгІЬѕМўвбЪЁТдЃЉЃК
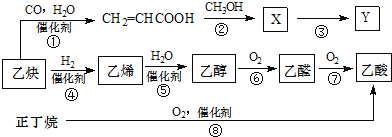
ЃЈ1ЃЉЛЏКЯЮяCH2ЈTCHCOOHжаЫљКЌЙйФмЭХУћГЦЮЊ_____________КЭ____________ЃЛ
ЃЈ2ЃЉе§ЖЁЭщЕФвЛжжЭЌЗжвьЙЙЬхЕФНсЙЙМђЪНЮЊ_____________ЃЛYЕФНсЙЙМђЪНЮЊ_____________ЃЛ
ЃЈ3ЃЉЭМжа8ВНЗДгІжаЃЌдзгРћгУТЪУЛгаДяЕН100%ЕФЮЊ_____________ЃЈЬюађКХЃЉЁЃ
ЃЈ4ЃЉаДГіЯТСаЗДгІЕФЛЏбЇЗНГЬЪНЃЈзЂУїЗДгІЬѕМўЃЉЃКЗДгІЂо__________________________ЃЛЗДгІЂрЮЊЃЈЭЌЪБгаЫЎЩњГЩЃЉ_______________________________________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЭљКЌ0.2mol NaOHКЭ0.1mol CaЃЈOHЃЉ2ЕФШмвКжаГжајЮШЖЈЕиЭЈШыCO2ЦјЬхЃЌЕБЭЈШыЦјЬхЮЊ6.72LЃЈSЃЎTЃЎPЃЉЪБСЂМДЭЃжЙЃЌдђетвЛЙ§ГЬжаЃЌШмвКжаРызгЕФЮяжЪЕФСПКЭЭЈШыCO2ЦјЬхЕФЬхЛ§ЙиЯЕе§ШЗЕФЭМЯѓЪЧЃЈЦјЬхЕФШмНтКіТдВЛМЦЃЉЃЈ ЃЉ
A.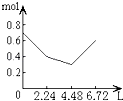
B.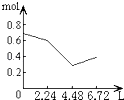
C.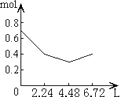
D.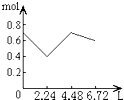
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПPCl3КЭPCl5ЖМЪЧживЊЕФЛЏЙЄдСЯЁЃНЋPCl3(g)КЭCl2(g)ГфШыЬхЛ§ВЛБфЕФ2 LУмБеШнЦїжаЃЌдквЛЖЈЬѕМўЯТЗЂЩњЯТЪіЗДгІЃЌ10 minЪБДяЕНЦНКтЃКPCl3(g) + Cl2(g)![]() PCl5(g)гаЙиЪ§ОнШчЯТЃЌЯТСаХаЖЯВЛе§ШЗЕФЪЧ
PCl5(g)гаЙиЪ§ОнШчЯТЃЌЯТСаХаЖЯВЛе§ШЗЕФЪЧ
PCl3(g) | Cl2(g) | PCl5(g) | |
ГѕЪМХЈЖШ(mol/L) | 2.0 | 1.0 | 0 |
ЦНКтХЈЖШ(mol/L) | c1 | c2 | 0.4 |
A. 10 minФкЃЌv(Cl2) = 0.04 mol/(LЁЄmin)
B. ЕБШнЦїжаCl2ЮЊ1.2 molЪБЃЌЗДгІДяЕНЦНКт
C. ШєЩ§ИпЮТЖШ(T1ЃМT2)ЪБЃЌИУЗДгІЦНКтГЃЪ§МѕаЁЃЌдђЦНКтЪБPCl3ЕФ![]()
D. ЦНКтКѓвЦзп2.0 mol PCl3КЭ1.0 molCl2ЃЌдкЯрЭЌЬѕМўЯТдйДяЦНКтЪБЃЌc(PCl5)ЃМ0.2 mol/L
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПФГПЮЭтЛюЖЏаЁзщЕФЭЌбЇЃЌдкЪЕбщЪвзіаПгыХЈСђЫсЗДгІЕФЪЕбщжаЃЌМзЭЌбЇШЯЮЊВњЩњЕФЦјЬхЪЧЖўбѕЛЏСђЃЌЖјввЭЌбЇШЯЮЊГ§ЖўбѕЛЏСђЦјЬхЭтЃЌЛЙПЩФмВњЩњЧтЦјЃЎЮЊСЫбщжЄФФЮЛЭЌбЇЕФХаЖЯе§ШЗЃЌБћЭЌбЇЩшМЦСЫШчЭМ1ЫљЪОЪЕбщзАжУЃЈаПгыХЈСђЫсЙВШШЪБВњЩњЕФЦјЬхЮЊXЃЌЦјЬхЗЂЩњзАжУТдШЅЃЉЃЎЪдЛиД№ЃК 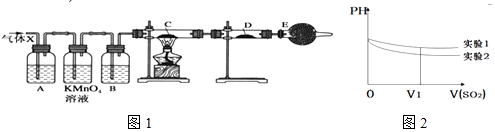
ЃЈ1ЃЉЩЯЪіЗДгІжаЩњГЩЖўбѕЛЏСђЕФЛЏбЇЗНГЬЪНЮЊ ЃЎ
ЃЈ2ЃЉввЭЌбЇШЯЮЊЛЙПЩФмВњЩњЧтЦјЕФРэгЩЪЧ ЃЎ
ЃЈ3ЃЉAжаМгШыЕФЪдМСПЩФмЪЧ ЃЌ зїгУЪЧЃЛBжаМгШыЕФЪдМСПЩФмЪЧ ЃЌ зїгУЪЧЃЛ
ЃЈ4ЃЉПЩвджЄУїЦјЬхXжаКЌгаЧтЦјЕФЪЕбщЯжЯѓЪЧЃКCжаЃК ЃЌ DжаЃК ЃЎ
ЃЈ5ЃЉIIЃЎИУаЁзщЭЌбЇНЋЪеМЏЕФSO2ЦјЬхЭЈШы0.1molLЉ1ЕФBaЃЈNO3ЃЉ2ШмвКжаЃЌЕУЕНСЫBaSO4ГСЕэЃЌЮЊЬНОПЩЯЪіШмвКжаКЮжжЮЂСЃФмбѕЛЏЭЈШыЕФSO2 ЃЌ ИУаЁзщЬсГіСЫШчЯТМйЩшЃК МйЩшвЛЃКШмвКжаЕФNO3Љ
МйЩшЖўЃКШмвКжаШмНтЕФO2
ИУаЁзщЩшМЦЪЕбщбщжЄСЫМйЩшвЛЃЌ
ЧыдкЯТБэПеАзДІЬюаДЯрЙиЪЕбщЯжЯѓ
ЪЕбщВНжш | ЪЕбщЯжЯѓ | НсТл |
ЪЕбщ1ЃКдкЪЂгаВЛКЌO2ЕФ25ml0.1mol/LBaCl2ШмвКЕФЩеБжаЃЌЛКТ§ЭЈШыДПОЛЕФSO2ЦјЬх | МйЩшвЛГЩСЂ | |
ЪЕбщ2ЃКдкЪЂгаВЛКЌO2ЕФ25ml0.1mol/LBaЃЈNO3ЃЉ2ШмвКЕФЩеБжаЃЌЛКТ§ЭЈШыДПОЛЕФSO2ЦјЬх |
ЃЈ6ЃЉЮЊЩюШыбаОПИУЗДгІЃЌИУаЁзщЛЙВтЕУЩЯЪіСНИіЪЕбщжаШмвКЕФpHЫцЭЈШыSO2ЬхЛ§ЕФБфЛЏЧњЯпШчЭМ2ЃЌЪЕбщ1жаШмвКpHБфаЁЕФдвђЪЧV1ЪБЃЌЪЕбщ2жаШмвКpHаЁгкЪЕбщ1ЕФдвђЪЧЃЈгУРызгЗНГЬЪНБэЪОЃЉ ЃЎ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСагаЙиЮяжЪЕФгУЭОжаЃЌдЫгУСЫЮяжЪЕФЛЏбЇаджЪЕФЪЧ
A. гУНКзДЧтбѕЛЏТСФ§ОлЫЎжаЕФаќИЁЮяНјааОЛЫЎ
B. гУКьзиЩЋбѕЛЏЬњжЦдьКьЩЋгЭЦс
C. ЧтбѕЛЏТСзїЮЊвНгУЕФЮИЫсжаКЭМС
D. гУбѕЛЏТСжЦдьФЭЛ№лсліКЭФЭЛ№Йм
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЪЕбщЪвгаЫФИівЉЦЗГїЃЌвбДцЗХШчЯТвЉЦЗЃК
Гї | МзГї | ввГї | БћГї | ЖЁГї |
вЉЦЗ | бЮЫсЁЂСђЫс | CCl4ЁЂC2H5OH | КьСзЁЂСђ | ЭЁЂаП |
ЪЕбщЪваТЙКНјвЛаЉЛюадЬПЃЌгІНЋЫќДцЗХдк
A. МзГї B. ввГї C. БћГї D. ЖЁГї
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаДыЪЉЛђЪТЪЕВЛФмгУРеЯФЬиСадРэНтЪЭЕФЪЧ
AЃЎаТжЦЕФТШЫЎдкЙтееЯТбеЩЋБфЧГ
BЃЎH2ЁЂI2ЁЂHIЦНКтЛьКЯЦјМгбЙКѓбеЩЋБфЩю
CЃЎЭљK2CrO4ШмвКжаМгЫсЃЌЪЙШмвКГШЩЋМгЩю
DЃЎFe(SCN)3ШмвКжаМгШыМИЕЮ6mol/L NaOHШмвККѓШмвКбеЩЋБфЧГ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com