
 pC(g)+qD(g)经5 min后达到平衡,测得此时A的浓度减少了a mol·L-1,而C的浓度增加了2/3a mol·L-1,又测得平均反应速率v(C)=2v(B),达到平衡后,若保持温度不变,给体系加压,平衡不移动,那么该反应可表示为( )
pC(g)+qD(g)经5 min后达到平衡,测得此时A的浓度减少了a mol·L-1,而C的浓度增加了2/3a mol·L-1,又测得平均反应速率v(C)=2v(B),达到平衡后,若保持温度不变,给体系加压,平衡不移动,那么该反应可表示为( ) 3C(g)+5D(g) B.3A(g)+B(g)
3C(g)+5D(g) B.3A(g)+B(g) 2C(g)+2D(g)
2C(g)+2D(g) 2C(g)+D(g) D.A(g)+3B(g)
2C(g)+D(g) D.A(g)+3B(g) 2C(g)+2D(g)
2C(g)+2D(g) 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源:不详 题型:判断题

 XeF4(g)+F2(g),其反应热ΔH0(填“>”“=”或“<”=。理由是__________________________。
XeF4(g)+F2(g),其反应热ΔH0(填“>”“=”或“<”=。理由是__________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 C(g)
C(g)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C达到平衡时,增大压强,C的量减少,则下列结论符合该平衡的是( )
2C达到平衡时,增大压强,C的量减少,则下列结论符合该平衡的是( )查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.-20 ℃ | B.-10 ℃ | C.0 ℃ | D.10 ℃ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SCl2(鲜红色液体);△H=+61.16kJ。
2SCl2(鲜红色液体);△H=+61.16kJ。| A.单位时间里生成n mol S2Cl2的同时也生成n molCl2 |
| B.达到平衡时,若升高温度,压强不变,反应混合溶液颜色变浅 |
| C.达到平衡时,单位时间里消耗n mol S2Cl2的同时也生成n molCl2 |
| D.加入氯气,平衡向正反应方向移动,氯气的转化率一定升高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3。下列有关说法正确的是( )
2NH3。下列有关说法正确的是( )| A.达到化学平衡时,正反应和逆反应的速率都为零 |
| B.当符合:3u正(N2)=u正(H2)时,反应达到平衡状态 |
| C.达到化学平衡时,单位时间消耗amolN2,同时生成3amolH2 |
| D.当N2、H2、NH3的分子数比为1∶3∶2,反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 PCl3(g)+Cl2(g),反应达到平衡后,PCl5的体积分数为M%,若在同一温度和同一容器中最初投入2 mol PCl5,反应达到平衡时,PCl5的体积分数为N%,则M和N的正确关系为( )
PCl3(g)+Cl2(g),反应达到平衡后,PCl5的体积分数为M%,若在同一温度和同一容器中最初投入2 mol PCl5,反应达到平衡时,PCl5的体积分数为N%,则M和N的正确关系为( )| A.M>N | B.N>M | C.M=N | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 FeO(s) + CO(g),其温度与平衡常数K的关系如下表:
FeO(s) + CO(g),其温度与平衡常数K的关系如下表:| T(K) | 938 | 1173 |
| K | 1.47 | 2.15 |
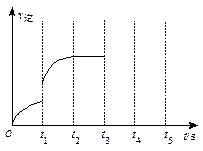
 画出t3~ t5时间段的v逆变化曲线。
画出t3~ t5时间段的v逆变化曲线。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com