
某班同学用如下实验探究Fe2+、Fe3+的性质。回答下列问题:
(1)甲组同学取2mL FeCl2溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,说明Cl2可将Fe2+氧化。FeCl2溶液与氯水反应的离子方程式为__ 。
(2)乙组同学认为甲组的实验不够严谨,该组同学在2mL FeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是 。
(3)丙组同学取10mL 0.1mol/L KI溶液,加入6mL 0.1mol/L FeCl3溶液混合。分别取2mL此溶液于3支试管中进行如下实验:
①第一支试管中加入1mLCCl4充分振荡、静置,CCl4层呈紫色;
②第二只试管中加入1滴K3[Fe(CN)6]溶液,生成蓝色沉淀;
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是 (填离子符号);实验①和③说明:在I-过量的情况下,溶液中仍含有 (填离子符号) ,由此可以证明该氧化还原反应为 反应(填“可逆”或“不可逆”)。
,由此可以证明该氧化还原反应为 反应(填“可逆”或“不可逆”)。
(4)丁组同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为 ;一段时间后.溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原因是 ;生成沉淀的原因是 (用平衡移动原理解释)。
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源:2017届海南省高三上学期月考三化学试卷(解析版) 题型:实验题
空气 吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
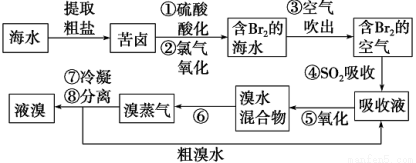
(1)步骤①中用硫酸酸化的目的是 ;
步骤②发生反应的离子方程式为 。
(2)步骤④利用了SO2的还原性,反应的离子方程式: 。
(3)步骤⑥的名称是 。
(4)从含Br2的海水中吹出的溴也可用纯碱吸收,纯碱吸收溴的主要反应是3Na2CO3+3Br2==NaBrO3+5NaBr+3CO2;吸收1 mol Br2时,转移的电子为_________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 夏季用空调时,把设定温度适当调高 | |
| B. | 让电视机长期待机 | |
| C. | 离开房间时,随手关灯 | |
| D. | 使用高效节能型的用电设备 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 集气瓶被誉为“万能瓶”,如下图装置是其中的一种.当被收集的气体从a口进入时,瓶内空气从b口排出,相当于向上排空气法收集气体.现若将被收集的气体从b口进入,则它可收集的气体为:①H2 ②O2 ③CO2( )
集气瓶被誉为“万能瓶”,如下图装置是其中的一种.当被收集的气体从a口进入时,瓶内空气从b口排出,相当于向上排空气法收集气体.现若将被收集的气体从b口进入,则它可收集的气体为:①H2 ②O2 ③CO2( )| A. | 只有① | B. | 只有②和③ | C. | 只有③ | D. | ①②③均可 |
查看答案和解析>>
科目:高中化学 来源:2017届海南省高三上学期月考三化学试卷(解析版) 题型:实验题
KAl(SO4)2·12H2O(明矾)是一种复盐,在造纸等方面应用广泛。实验室中,采用废易拉罐(主要成分为Al,含有少量的Fe、Mg杂质)制备明矾的过程如下图所示。回答下列问题:
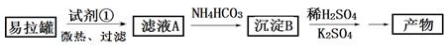
(1)为尽量少引入杂质,试剂①应选用 (填标号)。
A.HCl溶液 B.H2SO4溶液 C.氨水 D.NaOH溶液
(2)生成沉淀B的离子方程式为 ;明矾能用于净水,其原因是 ;往明矾溶液中滴加Ba(OH)2溶液,恰好使溶液中的SO42-完全沉淀的离子方程式为 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2017届广西桂林十八中高三上10月月考化学试卷(解析版) 题型:选择题
下列各组离子或分子能大量共存,当加入相应试剂后会发生化学变化,且发生反应的离子方程式书写可能正确的是
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Na+、Fe3+、Cl-、I- | NaOH溶液 | Fe3++3OH-=Fe(OH)3↓ |
B | Mg2+、HCO | 过量NaOH溶液 | Mg2++HCO H2O+Mg(OH)2↓+CO |
C | K+、NH3·H2O、CO | 通入少量CO2 | 2OH-+CO2=CO |
D | Na+、NO | NaHSO4溶液 | SO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com