
分析 根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$,结合摩尔质量与相对分子质量的关系以及分子的组成原子的原子结构计算.
解答 解:1.7g NH3的物质的量为$\frac{m}{M}$=$\frac{1.7g}{17g/mol}$=0.1mol;标准状况下的体积为V=nVm=0.1mol×22.4L/mol=2.24L;含有氢原子的物质的量为0.3mol,与氨气所含H原子数相同的H2S的物质的量为0.15mol,则其体积为0.15mol×22.4L/mol=3.36L,
故答案为:0.1mol;2.24L;3.36.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,题目难度不大,注意有关计算公式的运用和物质的结构和组成.


科目:高中化学 来源: 题型:选择题
| A. | 7 | B. | 6 | C. | 5 | D. | 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
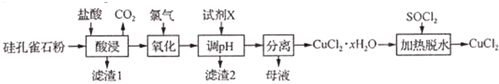
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
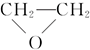 ③CH3CHO;④
③CH3CHO;④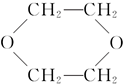 ⑤HO-CH2CH2OCH2CH2-OH.
⑤HO-CH2CH2OCH2CH2-OH.| A. | 只有① | B. | 只有①④ | C. | 只有①⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
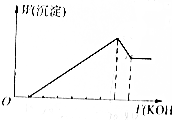 把镁铝合金用稀H2SO4溶液完全溶解后,在所得溶液中加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量比是( )
把镁铝合金用稀H2SO4溶液完全溶解后,在所得溶液中加入KOH溶液的体积与生成沉淀的质量关系如图所示,则合金中镁与铝的质量比是( )| A. | 1:1 | B. | 8:9 | C. | 4:3 | D. | 4:9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cl-、MnO4-、SO42- | B. | Na+、SiO32-、NO3-、CO32- | ||
| C. | Na+、NO3-、SO42-、HCO3- | D. | Mg2+、SO42-、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 该硫酸的物质的量浓度为18.4 mol/L | |
| B. | 1 mol Zn与足量的该硫酸反应产生2 g氢气 | |
| C. | 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50.0 mL | |
| D. | 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com