
【题目】下列有关化学反应与能量的叙述正确的是![]()
A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.己知![]() 白磷,
白磷,![]() 红磷,
红磷,![]() ,则白磷比红磷稳定
,则白磷比红磷稳定
C.对于某一化学反应,当生成物中化学键形成时所吸收的能量大于反应物中化学键断裂所释放的能量时,该反应为吸热反应,![]()
D.若![]() ,
,![]()
![]() ,则含
,则含![]() gNaOH的稀溶液与稀醋酸完全中和,放出的热量小于
gNaOH的稀溶液与稀醋酸完全中和,放出的热量小于![]() kJ
kJ
 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】某研究小组以乙烯和甲苯为主要原料,设计出医药中间体G的合成路线如下:
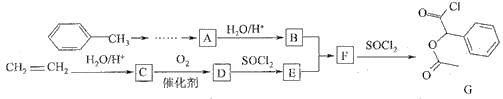
已知:![]()
RCOOH![]() RCOCl
RCOCl![]() RCOOR’
RCOOR’
(1)B的结构简式为________。
(2)从乙烯到化合物E的转化过程中,涉及的反应类型依次是________反应、________反应和________反应。
(3)F的分子式为________,M是F的某种能发生水解反应的同分异构体,经测定M的核磁共振氢谱为2组峰且峰面积之比为2:3,则M的结构简式可能为________![]() 仅写一列即可
仅写一列即可![]() 。写出M与足量NaOH溶液反应的作学方程式:________。
。写出M与足量NaOH溶液反应的作学方程式:________。
(4)A的同分异构体有多种,同时符合下列条件的A的同分异构体有________种。
①含有一![]() 和
和![]() 且都与苯环直接相连。
且都与苯环直接相连。
②有4个碳原子在同一条直线上。
(5)设计出以甲苯为原料制备A的合成路线_____________。(无机试剂任选,已知:RCHO
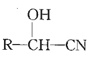 )合成路线常用的表示方式为:原料
)合成路线常用的表示方式为:原料 中间产物
中间产物 目标产物。
目标产物。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃时,pH=5的CH3COOH溶液中,由水电离出的氢离子浓度c(H+)=______
molL﹣1;往溶液中加入少量NaOH固体,则溶液中![]() _____(填“增大”、“减小”或“不变”),写出表示该混合溶液中所有离子浓度之间的一个等式:______。
_____(填“增大”、“减小”或“不变”),写出表示该混合溶液中所有离子浓度之间的一个等式:______。
(2)甲醇(CH3OH)是一种可再生能源,具有广阔的开发和应用前景。以甲醇、氧气和KOH溶液为原料,石墨为电极制造新型手机电池,甲醇在_____极反应(填“正”或“负”),电极反应式为_____。
(3)泡沫灭火器的原理:________________________(用离子反应方程式表示)。
(4)Na2CO3溶液中所有离子的大小关系是:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胆矾CuSO4·5H2O可写[Cu(H2O)4]SO4·H2O,其结构示意图如下:
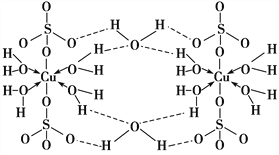
下列有关胆矾的说法正确的是( )
A. 所有氧原子都采取sp3杂化 B. 氧原子参与形成配位键和氢键两种化学键
C. Cu2+的价电子排布式为3d84s1 D. 胆矾中的水在不同温度下会分步失去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NaOH溶液分别加到HA、HB两种弱酸溶液中,两溶液中pH与粒子浓度比值的对数关系如图所示,已知![]() ,下列有关叙述错误的是( )
,下列有关叙述错误的是( )
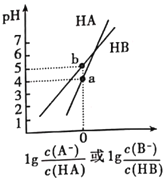
A.HA、HB两种酸中,HB的酸性弱于HA
B.b点时,![]()
C.同浓度同体积的NaA和NaB溶液中,阴离子总数相等
D.向HB溶液中加入NaOH溶液所得的混合溶液中,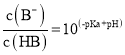
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取的乙烯中常混有少量的![]() ,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
,有人设计如图实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
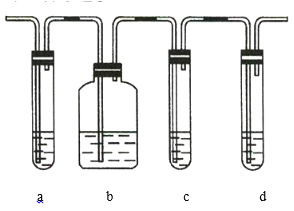
(1)图中a、b、c、d装置盛放的试剂依次是___________________(填序号)。
A.品红溶液 B.![]() 溶液 C.浓硫酸 D.酸性高锰酸钾溶液
溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明![]() 存在的实验现象是______________________________________。
存在的实验现象是______________________________________。
(3)使用装置b的目的是________________________。
(4)使用装置c的目的是________________________。
(5)能说明混合气体中含有乙烯的现象是____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 在工业、农业等方面有广泛的应用,工业上可由高铁菱锰矿(主要成分为
在工业、农业等方面有广泛的应用,工业上可由高铁菱锰矿(主要成分为![]() ,含有
,含有![]() 、
、![]() 、
、![]() 、
、![]() 等杂质)制备,部分工艺流程如图所示:
等杂质)制备,部分工艺流程如图所示:
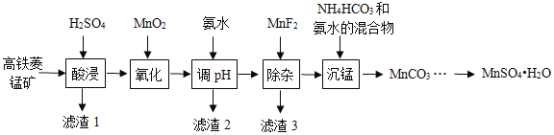
相关金属离子生成氢氧化物沉淀的![]() (开始沉淀的
(开始沉淀的![]() 按离子浓度为
按离子浓度为![]() 计算):
计算):
金属离子 |
|
|
|
|
|
开始沉淀的 | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 |
沉淀完全的 | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 |
(1)“氧化”时发生反应的离子方程式为______________。
(2)“调![]() ”范围至5~6,得到滤渣2的主要成分除
”范围至5~6,得到滤渣2的主要成分除![]() 外还有_____________。
外还有_____________。
(3)“除杂”过程中加入![]() 的目的是______。
的目的是______。
(4)“沉锰”过程中发生反应的化学方程式为______。
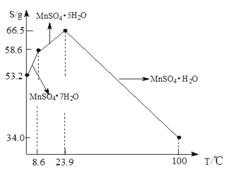
(5)![]() 在水中的溶解度与温度关系如图。由
在水中的溶解度与温度关系如图。由![]() 获得较纯净的
获得较纯净的![]() 晶体的方法是:将
晶体的方法是:将![]() 溶于适量的稀硫酸,控制温度在
溶于适量的稀硫酸,控制温度在![]() 之间蒸发结晶,______,得到
之间蒸发结晶,______,得到![]() 晶体,洗涤、烘干。晶体通常采用减压烘干的原因是______。
晶体,洗涤、烘干。晶体通常采用减压烘干的原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以海绵铜(主要成分为Cu和CuO)为原料制取CuCl的主要流程如图所示。
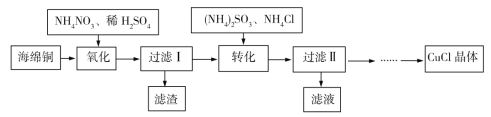
已知:①CuCl微溶于水,不溶于乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl露置于潮湿的空气中易被氧化。
回答下列问题。
(1)“氧化”时温度应控制在60℃~70℃,原因是___。
(2)写出“转化”过程中的离子方程式___。
(3)“过滤Ⅱ”所得滤液经蒸发浓缩、降温结晶、过滤等操作获得(NH4)2SO4晶体,可用作化学肥料。“过滤Ⅱ”所得滤渣主要成分为CuCl,用乙醇洗涤的优点是___。
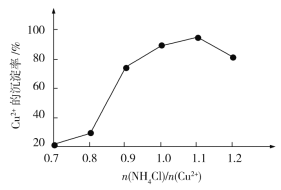
(4)氯化铵用量![]() 与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是___。
与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是___。
(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:___。(实验中可选试剂:0.1mol·L-1盐酸、10mol·L-1盐酸、蒸馏水、无水乙醇)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的是
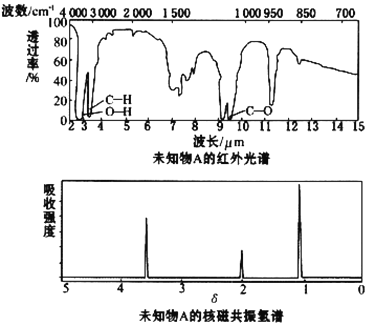
A.由红外光谱可知,该有机物中至少含有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子
C.仅由其核磁共振氢谱可知其分子中的氢原子总数
D.若A的化学式为C2H6O,则其结构简式为CH3CH2OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com