
| A. | 氧化铁俗名铁红,可用作红色涂料 | |
| B. | 氢氧化铝是两性氢氧化物,可用于治疗胃酸过多 | |
| C. | 铁是地壳中含量最多的金属元素 | |
| D. | 保存硫酸亚铁溶液常加铁粉防氧化 |
分析 A、氧化铁俗称铁红,根据其用途来回答;
B、根据胃酸的成分是盐酸,氢氧化铝与盐酸发生中和反应进行解答;
C.地壳中含量最多的金属元素是铝;
D.硫酸亚铁溶液中,亚铁离子具有较强还原性,容易被氧化成铁离子,所以保存硫酸亚铁溶液时,通常需要加入还原剂,防止亚铁离子氧化,为了不引进杂质,应该加入少量铁粉.
解答 解:A、氧化铁俗称铁红,可用作红色油漆和涂料,故A正确;
B、氢氧化铝可以和胃酸的成分盐酸发生中和反应,而且这种物质没有腐蚀性,所以氢氧化铝可用于治疗胃酸过多,故B正确;
C.地壳中含量最多的前五种元素:氧、硅、铝、铁、钙,汉字中带钅字旁(汞和金除外)的属于金属元素,所以地壳中含量最多的金属元素是铝,故C错误;
D.硫酸亚铁溶液中Fe2+容易被氧化成Fe3+,导致硫酸亚铁溶液变质,为了防止防止硫酸亚铁溶液变质,需要加入少量铁粉,反应的离子方程式为2Fe3++Fe═3Fe2+;由于锌粉、铜粉、镁粉都会引进杂质,所以选用铁粉,故D正确;
故选C.
点评 本题考查了铁及其化合物性质和应用,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CH3COOCH2CH3 | B. | HCOOH | C. | HOOCCOOH | D. | HCHO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
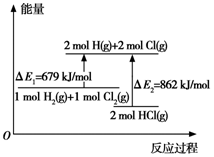
| A. | △E1是该反应的活化能 | B. | △E2是2 mol H-Cl键的总键能 | ||
| C. | 加入催化剂可以改变反应的焓变 | D. | 该反应是一个放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
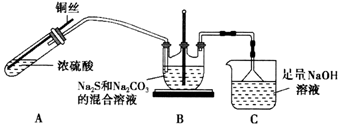
| 序号 | 操作及现象 | 结论 |
| ① | 取少量Al(OH)3粉末于试管中,滴加适量溶液,振荡,白色粉末溶解 | 溶质中一定含有NaOH |
| ② | 取2nL溶液于试管中,滴加足量氯水,氯水褪色丙有气泡产生,再滴加几滴Ba(NO3)2溶液,有白色沉淀产生 | 溶质为NaOH和 Na2CO3、Na2SO3 |
| 取2mL溶液于试管中,若 先加入足量稀硝酸,产生气泡,再滴入几滴Ba(NO3)2溶液,无沉淀产生 | 溶质为为NaOH和Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L水中含有水分子数为NA | |
| B. | 1mol Na2CO3 固体中含有的钠离子数为NA | |
| C. | 16g O2中含有的氧原子数为NA | |
| D. | 0.1mol/L的NaOH溶液中含有OH-的数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①④ | C. | ③④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
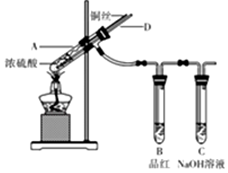 某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验,实验装置如图所示:
某实验小组同学为了探究铜与浓硫酸的反应,进行了如下系列实验,实验装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
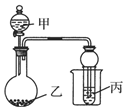 用如图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,能产生气体且丙中现象正确的是( )
用如图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,能产生气体且丙中现象正确的是( ) | 甲 | 乙 | 丙 | 试管中的现象 | |
| A | 浓氨水 | 生石灰 | Al(SO4)3溶液 | 先沉淀后消失 |
| B | 浓硫酸 | 亚硝酸钠 | 氢硫酸 | 溶液出现浑浊 |
| C | 浓硝酸 | 铜 | 淀粉KI溶液 | 试管口出现红棕色溶液仍为无色 |
| D | 浓盐酸 | 二氧化锰 | 含有KSCN的FeCl2溶液 | 溶液变红 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com