
| A、0.1mol N2与足量的H2反应,转移的电子数是0.6NA |
| B、常温下,0.1mol?L-1 NH4NO3溶液中含有的氮原子数是0.2NA |
| C、常温常压下,3.2g O2和3.2g O3所含氧原子数都是0.2NA |
| D、2.24L CO和CO2的混合气体中所含的碳原子数为0.1N A |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| B、能自发进行的化学反应,一定是△H<0、△S>0 |
| C、将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为氢氧化钠 |
| D、电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,SO2、NO2、Cl2均为有刺激性气味、有毒的气体 |
| B、Na2CO3粉末遇水生成含有结晶水的碳酸钠晶体,该晶体一定是Na2CO3?10H2O |
| C、人工合成的硅橡胶是目前最好的、既耐高温又耐低温的橡胶 |
| D、合金的硬度可以大于它的纯金属成分,合金的熔点也可以低于它的成分金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向1 mo1?L-l CH3COOH溶液中加入少量CH3COONa固体,由于CH3COONa水解显碱性,所以溶液的pH升高 | ||||||||||
B、25℃时,将a mol?L-l氨水与0.01mol?L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(Cl-),用含a的代数式表示反应完全时NH3?H2O的电离常数Kb=
| ||||||||||
C、根据表中数据可以计算出 (g)+3H2(g)→ (g)+3H2(g)→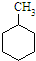 (g)的焓变 (g)的焓变
| ||||||||||
| D、已知298K时,MgCO3的Ksp=6.82×10-6,溶液中c(Mg2+)=0.0001mol?L-1,c(CO32-)=0.0001mol?L-1,此时Mg2+和CO32-不能共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水电离出的c(H+)?c(OH-)=10-22的溶液:K+、Na+、SO42-、S2O32- |
| B、澄清透明溶液:Mg2+、Cu2+、Cl-、SO42- |
| C、使酚酞变红色的溶液:NH4+、K+、AlO2-、NO3- |
| D、含0.1mol?L-1 KI的溶液:Fe3+、Na+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
| B、腐蚀法制作印刷线路板2Fe3++Cu═2Fe2++Cu2+ |
| C、碳酸氢铵溶液中加足量石灰水:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、用惰性电极电解熔融氯化钠:2Cl-+2H2O═Cl2↑+H2↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有①③ | B、只有①②③ |
| C、只有②③④ | D、有①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com