
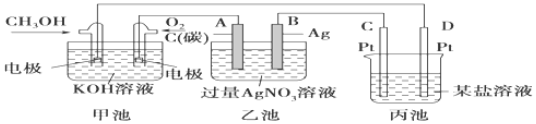
分析 (1)燃料电池属于原电池,原电池放电时,溶液中阳离子向正极移动,阴离子向负极移动;
(2)燃料电池中燃料失电子发生氧化反应,甲醇失电子和氢氧根离子反应生成碳酸根离子和水;
(3)电解硝酸银溶液时,银离子得电子生成银、水失电子生成氧气和氢离子,据此写出离子方程式;
(4)根据银和氢离子关系式计算氢离子浓度,从而确定溶液的pH,阴极上析出金属,则在金属活动性顺序表中金属元素处于H元素后,根据串联电池中转移电子数相等知,丙中析出金属元素需要的电子等于或小于乙池中转移电子数,据此确定含有的金属元素.
解答 解:(1)燃料电池中,投放燃料的电极是负极,投放氧化剂的电极是正极,原电池放电时,电解质溶液中氢氧根离子向负极移动,即向投放甲醇的电极移动,
故答案为:CH3OH;
(2)该燃料电池中,甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O,
故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;
(3)电解硝酸银溶液时,银离子得电子生成银、水失电子生成氧气和氢离子,离子方程式为4Ag++2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4H+,
故答案为:4Ag++2H2O$\frac{\underline{\;电解\;}}{\;}$4Ag+O2↑+4H+;
(4)当乙池中B(Ag)极的质量增加5.40g时,设氢离子浓度为xmol/L,
4Ag++2H2O=4Ag+O2↑+4H+;
432g 4mol
5.40g 0.5xmol
解得:x=0.1,所以溶液的pH=1,
阴极上析出金属,则在金属活动性顺序表中金属元素处于H元素后,根据串联电池中转移电子数相等知,丙中析出金属元素需要的电子等于或小于乙池中转移电子数,据此确定含有的金属元素,析出5.40g时转移电子是0.05mol,
A、硫酸镁中镁元素处于H元素前,所以阴极上不析出金属单质,故错误;
B、电解硫酸铜溶液时,阴极上析出1.60g铜需要转移电子0.05mol,故正确;
C、NaCl中钠元素处于氢元素前,所以阴极上不析出金属单质,故错误;
D、电解硝酸银溶液时,阴极上析出1.60g银需要转移电子0.0148mol<0.05mol,故正确;
故答案为:1;BD.
点评 本题考查了原电池和电解池原理的应用,题目难度中等,侧重于考查学生的分析能力和对基础知识的应用能力,注意(4)题中,丙中析出金属元素需要的电子等于或小于乙池中转移电子数,为易错点.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 试验操作 |
| A | 证明Mg的金属性强于Al | 分别向MgCl2、AlCl3溶液中加入足量的氨水 |
| B | 除去NH4Cl溶液中的Fe3+ | 加入氨水调节pH,过滤 |
| C | 检验Na2SO3是否已氧化变质 | 将Na2SO3样品溶于水中,滴加稀盐酸酸化的Ba(NO3)2溶液,观察是否有白色沉淀生成 |
| D | 检验碳单质与浓硫酸反应的产物 | 将生成的气体通过无水硫酸铜粉末、澄清石灰水、品红溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②③⑤⑦ | C. | ①②④⑥⑦ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
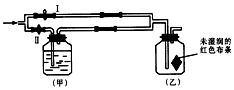 如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含有氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种
如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含有氯气的气体经过甲瓶后,通入乙瓶,布条不褪色;若关闭Ⅱ阀打开Ⅰ阀,再通入这种| A. | ② | B. | ②③ | C. | ①②④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 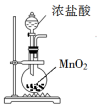 用装置制取氯气 | B. | 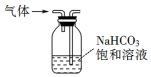 用装置除去CO2中的少量SO2气体 | ||
| C. | 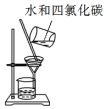 用装置分离水和四氯化碳的混合物 | D. | 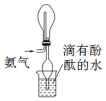 用装置收集氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 卤素原子、碳碳双键 | B. | 羟基、羧基 | ||
| C. | 醛基、酯基 | D. | 碳碳双键、酯基 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200mL 3mol•L-1 NaClO3溶液 | B. | 100mL 2mol•L-1 FeCl3溶液 | ||
| C. | 150mL 3mol•L-1 KCl溶液 | D. | 150mL 1mol•L-1 MgCl2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com