
【题目】I.2016年,我国研制的大型运输机运-20正式进入投产,标志着我国成为少数几个能生产大型军用运输机的国家之一。
(1)运-20的外壳大量使用了AM系列Mg-Al-Mn,铝的价电子排布图为_________________,第一电离能铝___________(填“大于”、“等于”或“小于”)镁
(2)为了减轻飞机的起飞重量并保持机身强度,运-20使用了大量的树脂材料,其中一种树脂材料的部分结构如图1所示,其中碳原子的杂化方式为___________,其个数比为___________


II.大型飞机的高推重比发动机被誉为航空工业皇冠上的“宝石”,采用大量的金属钨作为耐高温耐磨损材料
(3)钨元素位于第六周期第VIB族,价电子排布的能级与Cr相同,但排布方式与Cr有所不同,请写出钨原子的价层电子排布式___________
(4)图2为碳和钨形成的一种化合物的晶胞模型,碳原子和钨原子个数比为___________,其中一个钨原子周围距离最近且相等的碳原子有___________个。
【答案】 小于 sp2 、sp3 3:1 5d46s2 1:1 6
小于 sp2 、sp3 3:1 5d46s2 1:1 6
【解析】
(1)根据基态Al原子的核外电子排布式为1s22s22p63s23p1,确定铝原子的价电子排布图;镁、铝在元素周期表中位于同一周期,镁属于第ⅡA族元素,铝属于第ⅢA族元素,基态第ⅡA族元素的原子最外层电子填充的ns处于全充满,np处于全空,体系比较稳定,故基态第ⅡA族元素的原子的第一电离能比同周期相邻主族元素的第一电离能大;
(2)结合该物质的结构简式,根据价层电子对数确定该物质中碳原子的杂化方式;
(3)钨元素位于第六周期第VIB族,价电子排布的能级与Cr相同,但排布方式与Cr有所不同,根据铬原子的价层电子排布式确定钨原子的价层电子排布式;
(4)根据晶胞结构图,在顶点的原子被6个晶胞共用,在面心的原子被2个晶胞共用,在棱上的原子被3个晶胞共用,在体心的原子,不被其他晶胞共用,用于均摊法计算出晶胞中碳原子和钨原子个数。
(1)基态Al原子的价电子排布式为3s23p1,故铝的价电子排布图为 ;基态Mg原子的核外电子排布式为1s22s22p63s2, Mg元素的3s能级为全满状态,3p能级为全空状态,体系比较稳定,能量低不容易失去一个电子,所以铝的第一电离能比镁低。
;基态Mg原子的核外电子排布式为1s22s22p63s2, Mg元素的3s能级为全满状态,3p能级为全空状态,体系比较稳定,能量低不容易失去一个电子,所以铝的第一电离能比镁低。
(2)根据该树脂的结构简式,分子中的碳原子没有孤电子对,苯环中的每个碳原子形成3个![]() 键,不是苯环上的碳原子,每个碳原子形成4个
键,不是苯环上的碳原子,每个碳原子形成4个![]() 键, 所以该物质中苯环上的碳原子采用sp2杂化,不是苯环上的碳原子采用sp3杂化;采用sp2杂化的碳原子数为6n+6m,采用sp3杂化碳原子数为2m+2n,故采用sp2杂化的碳原子数与sp3杂化碳原子数之比为:(6n+6m):(2m+2n)=3:1;
键, 所以该物质中苯环上的碳原子采用sp2杂化,不是苯环上的碳原子采用sp3杂化;采用sp2杂化的碳原子数为6n+6m,采用sp3杂化碳原子数为2m+2n,故采用sp2杂化的碳原子数与sp3杂化碳原子数之比为:(6n+6m):(2m+2n)=3:1;
(3)钨元素位于第六周期第VIB族,价电子排布的能级与Cr相同,但排布方式与Cr有所不同,铬原子的价层电子排布式为3d54s1,故钨原子的价层电子排布式5d46s2;
(4)碳和钨形成的一种化合物的晶胞模型,在此结构中钨原子数目为1+2×![]() +12×
+12×![]() +6×
+6×![]() =6,晶胞内部有6个C原子,故碳原子和钨原子个数比为6:6=1:1;以晶胞体内钨原子可知,1个钨原子周围距离钨原子最近的碳原子有6个。
=6,晶胞内部有6个C原子,故碳原子和钨原子个数比为6:6=1:1;以晶胞体内钨原子可知,1个钨原子周围距离钨原子最近的碳原子有6个。
【点晴】
本题考查元素原子结构与性质相互关系的综合应用。需要注意的是,同周期中,元素原子的第一电离能的反常现象,即IIA族、VA族元素原子的价电子排布分别为ns2、ns2np3,其结构分别满足为全满和半满状态,这两族元素原子较为稳定,故第一电离能反常。如本题第(1)小题,Mg元素与Al元素第一电离能比较中,Mg>Al,因Mg原子最外层的电子3s能级处于全充满状态,3p能级处于全空状态,体系比较稳定。
![]()


科目:高中化学 来源: 题型:
【题目】实验室制备1,2-二溴乙烷的反应原理如下所示:
第一步:CH3CH2OH![]() CH2=CH2+H2O;
CH2=CH2+H2O;
第二步:乙烯与溴水反应得到1,2-二溴乙烷。
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃下脱水生成乙醚(CH3CH2OCH2CH3)。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示(部分装置未画出):

有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/(g/cm3) | 0.79 | 2.2 | 0.71 |
沸点/(℃) | 78.5 | 132 | 34.6 |
熔点/(℃) | -130 | 9 | -116 |
请回答下列问题:
(1)写出乙烯与溴水反应的化学方程式:______。
(2)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是_____(填字母代号)。
a.引发反应 b.加快反应速率
c.防止乙醇挥发 d.减少副产物乙醚生成
(3)装置B的作用是______。
(4)在装置C中应加入____ (填字母代号),其目的是吸收反应中可能生成的SO2、CO2气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在___ (填“上”或“下”)层。
(6)若产物中有少量副产物乙醚,可用____的方法除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() 摩尔盐
摩尔盐![]() 在
在![]() 时分解生成
时分解生成![]() 、
、![]() 和
和![]() 等。某小组称取mg样品进行如下实验
等。某小组称取mg样品进行如下实验![]() 尾气处理装置省略
尾气处理装置省略![]() ,验证它的分解产物。
,验证它的分解产物。
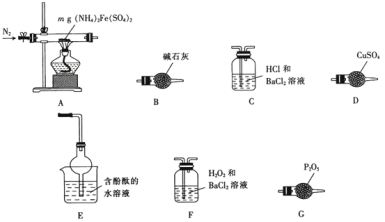
下列说法正确的是![]()
![]()
A.C中盐酸的作用是增强酸性,可以用硝酸替代盐酸
B.装置按![]() 连接可以检验
连接可以检验![]() 、
、![]() 、
、![]()
C.若实验中C、F都产生白色沉淀,则发生的反应不同,沉淀成分相同
D.实验完毕后,称量A中硬质玻璃管总质量,可以确定![]() 中x、y的值
中x、y的值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有资料显示过量的氨气和氯气在常温下可合成岩脑砂(主要成分为NH4Cl),某实验小组对该反应进行探究,并对岩脑砂进行元素测定。回答下列问题:
I.岩脑砂的制备
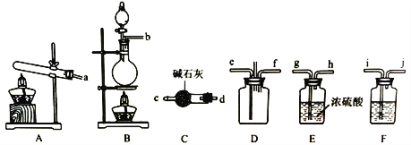
(1)该实验中用浓盐酸与二氧化锰反应制取所需氯气,写出该反应的离子方程式____________
(2)确定上述装置的合理连接顺序:a→____→ef←___(用小写字母和箭头表示,箭头方向与气流方向一致)。
(3)装置F中试剂的作用为___________
(4)装置D处有两个明显的不足之处,其中之一为:导管太细,生成的氯化铵固体可能会堵塞导管,之二为:___________。
II.岩脑砂中元素的测定:准确称取ag岩脑砂,与足量的氧化铜混合加热,利用右图装置测定岩脑砂中氮元素和氯元素的质量之比。充分加热后,G中产生红色固体,H、I装置质量增加,K中收集到无色气体。
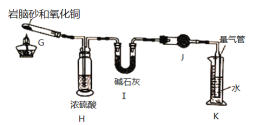
(5)写出G中发生反应的方程式______________________________________________
(6)若没有H装置,会导致测量值_____________(填“偏高”,“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学的发展、社会的进步和生活水平的提高都离不开化学的发展和各种材料的开发制造。
(1)中国高铁发展迅速,高铁建设使用的主要材料有钢铁、铝合金和玻璃等。
①高炉炼铁和制造普通玻璃都要用到的原料是________;高温下将铁矿石还原为金属铁的还原剂是________。
②钢铁、铝合金、玻璃都属于________(填字母)。
a.混合物 b.化合物 c.单质
(2)生活环境的改善,需要对生活和生产中的废弃物进行处理。
①燃煤排放的二氧化硫会被雨水吸收形成酸雨,这种酸雨在空气中久置酸性增强的原因是______________________________________(用化学方程式表示)。
②氮肥和硝酸的工业生产以及汽车等交通工具的使用,会有大量的氮氧化物(主要是![]() 和
和![]() )排放到空气中,这些氮氧化物对环境造成的影响有________(填一种即可)。氮氧化物可用氢氧化钠溶液吸收转化为
)排放到空气中,这些氮氧化物对环境造成的影响有________(填一种即可)。氮氧化物可用氢氧化钠溶液吸收转化为![]() 、________和
、________和![]() 。汽车安装尾气催化转化装置,可将尾气中的氮氧化物和一氧化碳转化为
。汽车安装尾气催化转化装置,可将尾气中的氮氧化物和一氧化碳转化为![]() 和________。
和________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 石油裂解气可以使溴水褪色,也可以使高锰酸钾溶液褪色
B. 可以用新制的氢氧化铜检验乙醇中是否含有乙醛
C. 正丙醇(CH3CH2CH2OH)和钠反应要比水和钠反应剧烈
D. CH2=CHCH3+Cl2 ![]() CH2=CHCH2 Cl+ HCl属于取代反应
CH2=CHCH2 Cl+ HCl属于取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚酯纤维的结构为:![]() ,以下是聚酯纤维的合成流程图:
,以下是聚酯纤维的合成流程图:


(1)写出产物C的结构简式:______________________。
(2)写出①和②的反应条件及试剂:
____________________;____________________。
(3)反应类型为X的反应方程式______________________,反应类型Y是___________。
(4)写出D、E生成聚酯纤维的化学方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:四甲基氢氧化铵[(CH3)4NOH ]是强碱,甲胺 (CH3NH2H2O)为弱碱。常温下,在体积均为20 mL、浓度均为0.1 mol/L的四甲基氢氧化铵溶液和甲胺溶液中,分别滴加浓度为0.1 mol/L的盐酸,溶液的导电率与盐酸体积的关系如图所示。下列说法正确的是

A. pH的相对大小: c>d
B. 在b、c、e三点中,水的电离程度最大的点是e
C. b 点溶液:c(H+)+c(CH3NH3+) = c(OH-)
D. c 点溶液:c(Cl-)>c(CH3NH3+) >c(H+) >c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+CO2(g)![]() 2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向逆方向进行的是
2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向逆方向进行的是
A.升高温度和增大压强B.降低温度和减小压强
C.降低温度和增大压强D.升高温度和减小压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com