
【题目】硫酸亚铁加热至高温会分解,生成—种金属氧化物M和两种非金属氧化物。某化学研究小组利用下列装置加热至高温使FeSO4分解。
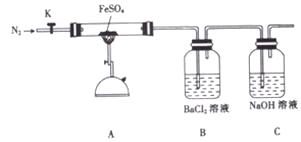
实验步骤:
将一定量FeSO4固体置于硬质玻璃管中,打开活塞K,通入一段时间N2,关闭活塞K。加热A中的玻璃管一段时间,待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却。
(1)已知M中铁元素的质量分数为70%,M的化学式为_____________。
(2)按图组装好仪器(已省略夹持仪器)并检查装置的气密性,在一定温度下按上述图示装置进行实验。
操作步骤 | 实验现象 | 用方程式解释原因 |
打开K,通入一段时间N2,关闭K。加热A中玻璃管一段时间 | 洗气瓶B中①__________ | ②______________ |
A中固体不再分解后,停止加热,打开K,缓慢通入N2至玻璃管冷却 | 硬质玻璃管最终可以看到③_______________ | ④______________ |
(3)某同学欲验证硫酸亚铁分解产物中含有的另一种非金属氧化物N。
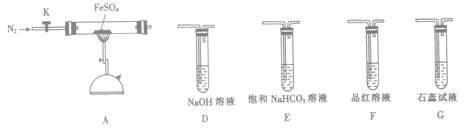
①从实验装置D、E、F、G中,选用两个装置与装置A连接进行实验,依次连接的合理顺序为A→______→______。
②能证明生成了非金属氧化物N的现象是________________。
【答案】 Fe2O3 有白色沉淀生成 SO3+H2O+BaCl2=BaSO4↓+2HCl 有红棕色固体物质生成 2FeSO4![]() Fe2O3+SO2↑+SO3↑ F D F中品红溶液褪色
Fe2O3+SO2↑+SO3↑ F D F中品红溶液褪色
【解析】(1)硫酸亚铁(FeSO4)加热至高温会分解,生成一种金属氧化物M和两种非金属氧化物。M中铁元素的质量分数为70%,氧占30%,Fe:O=![]() =2:3,化学式Fe2O3;
=2:3,化学式Fe2O3;
(2)硫酸亚铁(FeSO4)加热至高温会分解,生成一种金属氧化物M和两种非金属氧化物。发生了氧化还原反应,则两种非金属氧化物为SO2和SO3,打开K,通入一段时间的N2,关闭活塞K。加热A中的玻璃管一段时间洗气瓶B中会出现白色沉淀, SO3+H2O+BaCl2=BaSO4↓+2HCl ,A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却,硬质玻璃管中最终可以看到有红棕色固体, 2FeSO4![]() Fe2O3+SO2↑+ SO3↑ ;
Fe2O3+SO2↑+ SO3↑ ;
(3)①验证硫酸亚铁分解产物中含有的另一种非金属氧化物N为SO2,SO2能使品红溶液褪色,SO2是污染性气体,最后要用NaOH溶液吸收,装置为FD;验证硫酸亚铁分解产物中含有的另一种非金属氧化物N(SO2),F中品红溶液褪色.


科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是

A. 向BaSO4饱和溶液中加入固体Na2SO4可以由a点变到b点
B. d点无BaSO4沉淀生成
C. a点对应的Ksp大于c点对应的Ksp
D. 通过蒸发可以由d点变到c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1molL﹣1NaOH溶液500mL,根据溶液的配制情况,回答下列问题: 
(1)配制过程中需玻璃仪器有:烧杯、量筒、胶头滴管、、 .
(2)要完成本实验应称量NaOH固体的质量是 .
(3)配制溶液时,一般可以分为以下几个步骤:①计算;②称量;③;④冷却;⑤转移;⑥;⑦定容;⑧倒转摇匀.
(4)如图装置是某同学配制此溶液时转移操作的示意图,图中的错误是 .
(5)在配制过程中,如果其他操作都是正确的,下列操作会引起浓度偏低的是 . ①容量瓶不干燥,含有少量蒸馏水
②定容时俯视刻度线
③转移溶液时不慎有少量溶液洒到容量瓶外面
④定容摇匀后发现液面低于刻度线,再补加少量蒸馏水至刻度线
(6)NaOH溶液配制完成后,取100mL该溶液与100mL盐酸溶液混合,恰好完全中和,则该盐酸溶液的物质的量浓度为molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学通过实验研究钠及其化合物的有关性质,请回答相关问题.
(1)实验室中少量的钠通常保存在 中,在实验室中取用钠的仪器是 .
(2)若将钠在空气中加热,钠会燃烧发出黄色火焰,同时生成 色的固体,写出该产物与H2O反应的化学方程式: .
(3)将金属钠投入水中,发生反应的离子方程式为
(4)该同学在实验室欲配制500mL0.1mol/L NaOH溶液. ①配制溶液时肯定不需要如图所示仪器中的(填字母),配制上述溶液还需要用到的玻璃仪器是(填仪器名称).
②根据计算,该同学应用托盘天平称取NaOH的质量为 .
③该同学将所配制的NaOH溶液进行测定,发现浓度大于0.1mol/L.下列操作会引起所配浓度偏大的是 .
A.烧杯未进行洗涤
B.配制前,容量瓶中有少量蒸馏水
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
D.往容量瓶转移时,有少量液体溅出
E.在容量瓶中定容时俯视容量瓶刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线.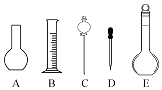
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】节能减排可以改善环境质量。下述做法正确的是( )
A. 以煤作为主要生活燃料 B. 利用太阳能、风能等替代化石能源
C. 鼓励人们购买和使用汽车 D. 大量使用含磷洗衣粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】17克NH3共有mol原子,0.1molH2S共有个氢原子;同质量的NH3和H2S中分子个数比为 . 在标准状况下,35.5g氯气的体积是 L,将其与氢气完全化合,需氢气的物质的量是mol,将生成的气体配制成1L溶液,溶质的物质的量浓度是molL﹣1 , 将此溶液取出20mL加蒸馏水制成200mL溶液,此冲稀后溶液中溶质的物质的量浓度是molL﹣1 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两个装置,下列说法错误的是

甲 乙
A.甲、乙装置中,Zn的质量均减小
B.甲、乙装置中,Cu上均有气泡产生
C.化学反应速率:乙>甲
D.甲装置中H+移向Zn,乙装置中H+移向Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸与高锰酸钾在酸性条件下能够发生反应:MnO4+H2C2O4+H+→Mn2++CO2↑+H2O(未配平).甲、乙两个实验小组分别利用酸性KMnO4溶液和H2C2O4溶液的反应来研究外界因素对反应速率的影响.
【实验设计】
甲组方案:通过测定生成CO2气体体积的方法来比较反应速率的大小.实验装置如图所示,25℃时将装置中的A溶液一次性加入B溶液(均已加入等量硫酸酸化)中.
实验编号 | A溶液 | B溶液 |
① | 2mL 0.1mol/LH2C2O4溶液 | 4mL0.0l1mol/L酸性KMnO4溶液 |
② | 2mL 0.2mol/LH2C2O4溶液 | 4mL0.01 mol/L酸性KMnO4溶液 |
(1)该反应中氧化剂和还原剂的物质的量之比为 .
(2)该实验探究的是对反应速率的影响.实现该实验目的还欠缺的仪器: . 比较①、②两组化学反应速率大小的方法是 .
乙组方案:用4mL0.0l1mol/L酸性KMnO4溶液与2mL 0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响.具体实验如下:
实验编号 | 10%硫酸的体积/mL | 温度/℃ | 其他物质 |
Ⅰ | 2 | 20 | ﹣ |
Ⅱ | 2 | 20 | 少量MnSO4粉末 |
Ⅲ | 2 | 30 | ﹣ |
Ⅳ | 1 | 20 | 1mL蒸馏水 |
(3)若要研究催化剂对化学反应速率的影响,则应对比实验(填序号,下同);若要研究温度对化学反应速率的影响,则应对比实验 .
(4)对比实验I和实验Ⅳ,可以研究硫酸的浓度对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com