
某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A. 定容时仰视刻度线
B. 所用NaOH已经潮解
C. NaOH溶解后还没有冷却就立即移入容量瓶中
D. 用带游码的托盘天平(附有砝码)称4gNaOH时误用了“左码右物”方法
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年河北省定州市高一上学期期中化学试卷(解析版) 题型:推断题
某混合物澄清透明的水溶液中,可能含有以下离子中若干种:K+、Ca2+、Fe2+、Cu2+、Cl-、CO32-、SO42-,现每次取该溶液100.00mL溶液进行以下实验:
①第一份加入AgNO3溶液发现有沉淀生成;
②第二份加足量BaCl2溶液生成沉淀,洗涤后干燥得沉淀6.27g,再将该沉淀加入足量盐酸溶解后再过滤洗涤干燥得沉淀2.33g。
请回答下列问题:
(1)根据以上实验判断,原溶液中一定不存在的离子是 ,可能存在的离子是 。
(2)原溶液中一定存在的阳离子是 ,其物质的量浓度至少为 mol/L。
(3)原溶液中一定存在的阴离子是 ,其物质的量浓度分别为 mol/L、 mol/L。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省三明市高一上期中化学试卷(解析版) 题型:选择题
下列离子方程式的书写中,正确的是( )
A.硫酸氢钾和氢氧化钡按等物质的量在溶液中反应:Ba2++OH-+H++SO42-=BaSO4↓+H2O
B.碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++CO2↑+2H2O
C.过量二氧化碳跟苛性钾反应; CO2+2OH-=CO32-+H2O
D.钠跟水反应:Na+2H2O=Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省三明市高一上期中化学试卷(解析版) 题型:选择题
有一瓶实验室敞口放置的NaOH溶液,瓶口有一层白色物质,此物质是( )
A.Na2O B.Na2O2 C.NaOH D.Na2CO3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上学期期中化学试卷(解析版) 题型:选择题
工业上ClO2常用NaClO3和Na2SO3溶液混合并加入H2SO4酸化后反应制得。在该反应中NaClO3作氧化剂,被还原成ClO2,还原剂Na2SO3被氧化成Na2SO4。该反应中NaClO3与Na2SO3的物质的量之比为( )
A.2:1 B.2:3 C.1:2 D.3:1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上学期期中化学试卷(解析版) 题型:选择题
将标准状况下的aLHCl(g)溶于1000g水中,得到的盐酸密度为b g·cm-3,则该盐酸的物质的量浓度是( )
A.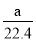 mol·L-1 B.
mol·L-1 B.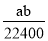 mol·L-1
mol·L-1
C.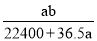 mol·L-1 D.
mol·L-1 D.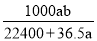 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省高一上学期期中化学试卷(解析版) 题型:选择题
下列变化必须加入还原剂的是( )
A.HCO3-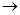 CO2 B.FeO
CO2 B.FeO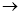 Fe3O4
Fe3O4
C.KClO3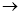 KCl D.MnO4-
KCl D.MnO4-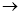 Mn2+
Mn2+
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上月考四化学试卷(解析版) 题型:选择题
某离子反应中共有H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。其中c(ClO-) 随反应进行逐渐减小。下列判断错误的是( )
A.该反应的还原剂是NH4+
B.消耗1mol氧化剂,转移2mol电子
C.氧化剂与还原剂的物质的量之比是2:3
D.反应后溶液酸性明显增强
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省杭州市五县七校高一上期中化学试卷(解析版) 题型:选择题
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁:另一份加入含bmol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的物质的量浓度为
A.(b-a) /V mol·L-1 B.2(2b-a)/V mol·L-1
/V mol·L-1 B.2(2b-a)/V mol·L-1
C.2(b-a)/V mol·L-1 D.(2b-a)/V mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com