
烃分子中若含有双键,叁键或单键的环,氢原子数就少,分子就不饱和,即具有一定的“不饱和度”,其数值可表示为:不饱和度(Ω)=双键数+环数+叁键数×2,则有机物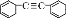 的不饱和度为
的不饱和度为
A.8 B.7 C.6 D.10
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三第二次模拟考试化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的值。下列说法正确的是
A.17.6 g丙烷中所含的共价键数目为4NA
B.常温下,pH=13的NaOH溶液中含有的OH-离子数目为0.1NA
C.标准状况下,5.6 L NO和5.6 L O2混合后的分子总数目为0.5NA
D.电解精炼铜时,若阳极质量减少64 g,则阴极得到电子的数目为2NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古鄂尔多斯市高三模拟化学试卷(解析版) 题型:填空题
[化学---选修5:有机化学基础](15分)
已知: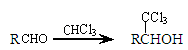 (-R表示烃基)
(-R表示烃基)
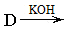 苯甲醇+苯甲酸钾
苯甲醇+苯甲酸钾
可由下列反应路线合成结晶玫瑰(只列出部分反应条件)
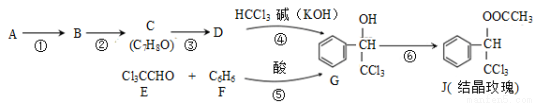
(1)A是苯的一种同系物,相同条件下,其蒸气对氢气的相对密度是46,则A的名称是 。
(2)C中的官能团是_____________。
(3)反应③的化学方程式为____________________。
(4)经反应路线④得到的副产物加水萃取、分液,能除去的副产物是 。
(5)已知: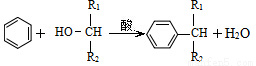 ,则经反应路线⑤得到一种副产物,其核磁共振氢谱有4种峰,各组吸收峰的面积之比为 。
,则经反应路线⑤得到一种副产物,其核磁共振氢谱有4种峰,各组吸收峰的面积之比为 。
(6)G的同分异构体L遇FeCl3溶液显色,与足量饱和溴水反应未见白色沉淀产生,则L与NaOH的乙醇溶液共热,所得有机物的结构简式为 (只写一种)。
(7)⑥的化学方程式是 。
(8)C有多种同分异构体,其中属于芳香族化合物的有 种(不包括C)。
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高二下学期第一次月考化学试卷(解析版) 题型:简答题
 短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示,其中A为地壳中含量最高的金属元素。
短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示,其中A为地壳中含量最高的金属元素。
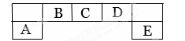
请用化学用语回答下列问题:
 (1)D元素在周期表中的位置:
(1)D元素在周期表中的位置:
(2)A、D 、E元素简单离子半径由大到小的顺序为____>_____ >_____ (填微粒符号 )
 (3)F与D同主族且相邻,其气态氢化物稳定性的大小 > (填微粒符号)
(3)F与D同主族且相邻,其气态氢化物稳定性的大小 > (填微粒符号)
(4)用高能射线照射含有10电子的D元素氢化物分子时,一个分子能释放一个电子,同时产生一种具有较高氧化性的阳离子,试写出该阳离子的电子式 ,该阳离子中存在的化学键有 。
 (5)C元素的简单氢化物与E元素的最高价氧化物的水化物反应,生成化合物K,则K的水溶液显____性(填“酸性”、“碱性”或“中性”),用离子方程式表示其原因 .
(5)C元素的简单氢化物与E元素的最高价氧化物的水化物反应,生成化合物K,则K的水溶液显____性(填“酸性”、“碱性”或“中性”),用离子方程式表示其原因 .
(6) 化合物AC导热性好,热膨胀系数小,是良好的耐热冲击材料。其中制备AC的一种方法为:用A元素的氧化物、焦炭和C的单质在1600 ~ 1750℃生成AC,每生成1 mol AC,消耗18 g碳,吸收b kJ的热量。(热量数据为25℃、101.3 kPa条件下)写出该反应的热化学方程式 。
化合物AC导热性好,热膨胀系数小,是良好的耐热冲击材料。其中制备AC的一种方法为:用A元素的氧化物、焦炭和C的单质在1600 ~ 1750℃生成AC,每生成1 mol AC,消耗18 g碳,吸收b kJ的热量。(热量数据为25℃、101.3 kPa条件下)写出该反应的热化学方程式 。
(7)在Fe和Cu的混合物中加入一定量C的最高价氧化物的水化物稀溶液,充分反应后,剩余金属m1 g;再向其中加入稀硫酸,充分反应后,金属剩余 m2 g 。下列说法正确的是 。
a.加入稀硫酸前和加入稀硫酸后的溶液中肯定都有Cu2+
b.加入稀硫酸前和加入稀硫酸后的溶液中肯定都有Fe2+
c.m1 一定大于m2
d.剩余固体m1 g 中一定有单质铜,剩余固体m2 g 中一定没有单质铜
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列离子方程式书写不正确的是
A.少量铁粉加入稀盐酸中:Fe + 2H+=Fe2++ H2↑
B.Ca(HCO3)2溶液与过量Ca(OH)2溶液反应:Ca2+ + HCO3- + OH-=CaCO3↓+ H2O
C.NH4HCO3溶液和过量Ba(OH)2溶液共热:2HCO3-+2OH- + Ba2+=BaCO3↓+ CO32- +2H2O
D.Na2S溶液中通入足量H2S:S2- + H2S=2HS-
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省邛崃市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列物质的分类方法恰当的是
序号 | 氧化物 | 酸 | 碱 | 盐 |
A | 熟石灰 | 氯酸钾 | 生石灰 | 蓝矾 |
B | 生石灰 | 次氯酸 | 纯碱 | 苏打 |
C | 过氧化氢 | 盐酸 | 碱式碳酸酮 | 氯化铁 |
D | 氧化钠 | 硫酸 | 烧碱 | 纯碱 |
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省达州市高二3月月考化学试卷(解析版) 题型:填空题
四种元素A、B、C、D,其中A元素原子的原子核内只有一个质子;B的基态原子s能级的总电子数比p能级的总电子数多1;C元素的原子最外层电子数是次外层的3倍;D是形成化合物种类最多的元素。
(1)A、D形成的某种化合物甲是一种重要的化工产品,可用作水果和蔬菜的催熟剂,甲分子中σ键和π键数目之比为________;写出由甲制高聚物的反应方程式 。
(2)A、C形成的某种化合物乙分子中含非极性共价键,乙分子属于________(“极性分子”或“非极性分子”);其电子式________;将乙加入浅绿色氯化亚铜溶液中,溶液变为棕黄色,写出该反应的离子方程式______________。
(3)写出B的基态原子电子排布图为 。与PH3相比,BA3易液化的主要原因是_____________;
(4)笑气(B2C)是一种麻醉剂,有关理论认为B2C与DC2分子具有相似的结构。故B2C的空间构型是________,其为________(填“极性”或“非极性”)分子。
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省高二4月月考化学试卷(解析版) 题型:选择题
某烷烃主链为4个碳原子的同分异构体有2种,则含相同碳原子数、主链也为4个碳原子的烯烃同分异构体有( )种
A.4 B.3 C.5 D.2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市东城区高三综合能力测试二理综化学试卷(解析版) 题型:填空题
(12分)用软锰矿(主要成分为MnO2)生产高锰酸钾产生的锰泥中,还含有18%的MnO2、3%的KOH(均为质量分数),及少量Cu、Pb的化合物等,用锰泥可回收制取MnCO3,过程如下图:
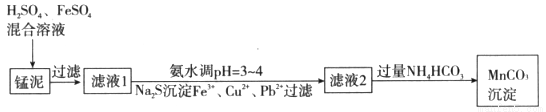
(1)锰泥中加入H2SO4、FeSO4混合溶液,反应的离子方程式是__________。
(2)经实验证明:MnO2稍过量时,起始H2SO4、FeSO4混合溶液中c(H+)/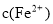 <0.7时,滤液1中能够检验出有Fe
<0.7时,滤液1中能够检验出有Fe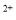 ;
;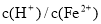 ≥0.7时,滤液1中不能检验出有Fe2+。
≥0.7时,滤液1中不能检验出有Fe2+。
①检验Fe2+是否氧化完全的实验操作是__________。
②生产时H2SO4、FeSO4混合溶液中c(H+)/c(Fe2+)控制在0.7~1之间,不宜过大,请从节约药品的角度分析,原因是__________。
若c(H+)/c(Fe2+)>1,调节c(H+)/c(Fe2+)到0.7~1的方法是__________。
(3)写出滤液2中加入过量NH4HCO3反应的离子方程式__________。
(4)上述过程锰回收率可达95%,若处理1740 kg的锰泥,可生产MnCO3__________kg(已知相对分子质量:MnO2 87;MnCO3 115)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com