
¹¤ŅµÉĻŅ»°ćŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ²ÉÓĆĻĀĮŠ·“Ó¦ŗĻ³É¼×“¼£ŗ
CO(g)£«2H2(g)  CH3OH(g)+Q
CH3OH(g)+Q
£Ø1£©ÄÜÅŠ¶Ļ·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ(Ģī×ÖÄøŠņŗÅ£¬ĻĀĶ¬)________”£
| A£®Éś³ÉCH3OHµÄĖŁĀŹÓėĻūŗÄCOµÄĖŁĀŹĻąµČ | B£®»ģŗĻĘųĢåµÄĆÜ¶Č²»±ä |
| C£®»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»±ä | D£®CH3OH”¢CO”¢H2µÄÅØ¶Č¶¼²»ŌŁ·¢Éś±ä»Æ |
| ĪĀ¶Č | 250”ę | 300”ę | 350”ę |
| K | 2.041 | 0.270 | 0.012 |
£Ø1£©CD
£Ø2£©¢Ł> ¢Ś80%£»250”ę
£Ø3£©df £Ø2·Ö£©
£Ø4£©Ń”Z£¬ĪĀ¶ČŅŖĒóµĶ£¬·“Ó¦ĖŁĀŹæģ”££Ø2·Ö£©
½āĪöŹŌĢā·ÖĪö£ŗ£Ø1£©A£®ĪŽĀŪ·“Ó¦ŹĒ·ń“ļµ½Ę½ŗāדĢ¬£¬Éś³ÉCH3OHµÄĖŁĀŹÓėĻūŗÄCOµÄĖŁĀŹŹ¼ÖÕĻąµČ£¬ĖłŅŌ²»ÄÜ×÷ĪŖÅŠ¶ĻĘ½ŗāדĢ¬µÄŅĄ¾Ż£¬“ķĪó£»B£®»ģŗĻĪļµÄÖŹĮæŹ¼ÖÕ²»±ä£¬ČŻĘ÷µÄĢå»ż²»±ä£¬ĖłŅŌ»ģŗĻĘųĢåµÄĆܶȏ¼ÖÕ²»±ä£¬ĖłŅŌ²»ÄÜ×÷ĪŖÅŠ¶ĻĘ½ŗāדĢ¬µÄŅĄ¾Ż£¬“ķĪó£»C£®·“Ó¦Ē°ŗ󣬻ģŗĻĘųĢåµÄĪļÖŹµÄĮæøı䣬ĘųĢåµÄÖŹĮæ²»±ä£¬·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬»ģŗĻĘųĢåµÄĻą¶ŌĘ½¾ł·Ö×ÓÖŹĮæ²»±ä£¬ĖłŅŌÄÜ×÷ĪŖÅŠ¶ĻĘ½ŗāדĢ¬µÄŅĄ¾Ż£¬ÕżČ·£»D£®·“Ó¦“ļµ½Ę½ŗāדĢ¬Ź±£¬CH3OH”¢CO”¢H2µÄÅØ¶Č¶¼²»ŌŁ·¢Éś±ä»Æ£¬ĖłŅŌÄÜ×÷ĪŖÅŠ¶ĻĘ½ŗāדĢ¬µÄŅĄ¾Ż£¬ÕżČ·£»¹ŹŃ”CD£»
£Ø2£©¢ŁÉżøßĪĀ¶Č£¬Ę½ŗāĻņĪüČČ·½ĻņŅĘ¶Æ£¬øł¾Ż±ķøńÖŖ£¬ĪĀ¶ČŌ½øߣ¬»ÆŃ§Ę½ŗā³£ŹżŌ½Š”£¬ĖµĆ÷Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬ĖłŅŌÕż·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬¼“”÷H£¼0£¬¶ų·Å³öµÄČČĮæQ>0£»
¢ŚĘ½ŗāŹ±Ņ»Ńõ»ÆĢ¼µÄĪļÖŹµÄĮæ=0.2mol/L”Į2L=0.4mol£¬×Ŗ»ÆĀŹ= n(CO)(·“Ó¦)/ n(CO)(·“Ó¦æŖŹ¼)”Į100%=(1?0.4)mol”Ā2mol”Į100%=80%
CO£Øg£©+2H2£Øg£©ØPCH3OH£Øg£©µ„Ī»ĪŖmol/L
·“Ó¦æŖŹ¼(mol/L) 1 3 0
·“Ó¦(mol/L) 0.8 1.6 0.8
Ę½ŗā(mol/L) 0.2 1.4 0.8
Ę½ŗā³£ŹżK="0.8" / 0.2(1.4)2 =2.04£¬ĖłŅŌĪĀ¶ČŹĒ250”ę”£
£Ø3£©a£®øĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£¬ÉżøßĪĀ¶ČĘ½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬¹Ź“ķĪó£»b£®“߻ƼĮ¶ŌĘ½ŗāŅʶÆĪŽÓ°Ļģ£¬¹Ź“ķĪó£»c£®Ōö¼ÓCOµÄÅØ¶Č£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬µ«COµÄ×Ŗ»ÆĀŹ½µµĶ£¬¹Ź“ķĪó£»d£®¼ÓČėH2¼ÓŃ¹£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬Ņ»Ńõ»ÆĢ¼µÄ×Ŗ»ÆĀŹŌö“󣬹ŹÕżČ·£»e£®¼ÓČė¶čŠŌĘųĢå¼ÓŃ¹£¬²Ī¼Ó·“Ó¦µÄĘųĢåŃ¹Ēæ²»±ä£¬Ę½ŗā²»ŅĘ¶Æ£¬¹Ź“ķĪó£»f£®·ÖĄė³ö¼×“¼£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬Ņ»Ńõ»ÆĢ¼µÄ×Ŗ»ÆĀŹŌö“󣬹ŹÕżČ·£»¹ŹŃ”df£®
£Ø4£©ŅņĪŖT1£¾T2£¾T3£¬ĖłŅŌĪĀ¶ČŌ½µĶĘ½ŗā³£ŹżŌ½“󣬷“Ó¦Īļ×Ŗ»ÆĀŹŌ½“ó£¬Ó֓߻ƼĮĶ¬µČ³Ģ¶Č¼Óæģ·“Ó¦ĖŁĀŹ£¬ĖłŅŌ¼ČÄÜŌŚµĶĪĀĻĀ×÷ÓĆÓÖÄܼÓæģ·“Ó¦ĖŁĀŹµÄ“߻ƼĮ×īŗĆŃ”ÓĆZ”£
æ¼µć£ŗ±¾Ģāæ¼²éµÄŹĒ»Æѧ·“Ó¦ŌĄķÖŖŹ¶”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
µ¼ÖĀæÕĘųĪŪČ¾µÄÖ÷ŅŖŌŅņĄ“×ŌÓŚ»ÆŹÆČ¼ĮĻČ¼ÉÕ”¢ĮņĖį¹¤ŅµŗĶĘū³µĪ²ĘųµÄÅÅ·Å£»ÖĀŹ¹“óĮ涞Ńõ»ÆĮņŗĶµŖŃõ»ÆĪļÅÅČė“óĘųÖŠ”£ĄūÓĆ»Æѧ·“Ó¦ŌĄķŃŠ¾æÖĪĄķ»·¾³ĪŪČ¾µÄ·½·ØŹĒµ±Ē°»·±£¹¤×÷µÄÖŲŅŖŃŠ¾æÄŚČŻÖ®Ņ»”£
£Ø1£©·“Ó¦ ŹĒĮņĖį¹¤ŅµÖŠµÄÖŲŅŖ·“Ó¦£»ĢįøßSO2µÄĘ½ŗā×Ŗ»ÆĀŹÓŠĄūÓŚ¼õÉŁĪ²ĘųÅÅ·Å£ŗŅŃÖŖøĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£»µ±øĆ·“Ó¦“¦ÓŚĘ½ŗāדĢ¬Ź±£¬ĪŖĮĖĢįøßSO2µÄ×Ŗ»ÆĀŹ£ŗĻĀĮŠæɲÉÓƵēėŹ©ŹĒ
ŹĒĮņĖį¹¤ŅµÖŠµÄÖŲŅŖ·“Ó¦£»ĢįøßSO2µÄĘ½ŗā×Ŗ»ÆĀŹÓŠĄūÓŚ¼õÉŁĪ²ĘųÅÅ·Å£ŗŅŃÖŖøĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£»µ±øĆ·“Ó¦“¦ÓŚĘ½ŗāדĢ¬Ź±£¬ĪŖĮĖĢįøßSO2µÄ×Ŗ»ÆĀŹ£ŗĻĀĮŠæɲÉÓƵēėŹ©ŹĒ
A£®¼ÓČėV2O5×÷“߻ƼĮ B£®ĶØČė¹żĮææÕĘų C£®øßĪĀ D£®Ōö“óŃ¹Ēæ
£Ø2£©Ņ»¶ØĢõ¼žĻĀ£¬Ļņ2LĆܱÕČŻĘ÷ÖŠĶØČė2molSO2(g)”¢1molO2(g)ŗĶ0.2SO3(g),2minŗó·“Ó¦“ļµ½Ę½ŗāŹ±,²āµĆSO2µÄ×Ŗ»ÆĀŹĪŖ50%£¬ŌņøĆæÉÄę·“Ó¦µÄĘ½ŗā³£ŹżK=_________£»ÓĆO2µÄÅØ¶Č±ä»Æ±ķŹ¾“ÓO-2minÄŚøĆ·“Ó¦µÄĘ½¾łĖŁĀŹv=_________£»ŗćĪĀĻĀ£¬ČōĻņČŻĘ÷ÖŠŌŁ¼ÓČė2molSO2(g)£¬ŌņÖŲŠĀ“ļµ½Ę½ŗāŹ±SO2µÄ×Ü×Ŗ»ÆĀŹ____________50%(Ģī”°>”±”¢”°<”±”¢”°=”±)
£Ø3£©ÄÜĖµĆ÷øĆ·“Ó¦ŅŃ¾“ļµ½Ę½ŗāדĢ¬µÄŹĒ
A£® B£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä£®
B£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä£®
C£® D£®ČŻĘ÷ÄŚĪļÖŹµÄĆܶȱ£³Ö²»±ä£®
D£®ČŻĘ÷ÄŚĪļÖŹµÄĆܶȱ£³Ö²»±ä£®
£Ø4£©ŌŚ“߻ƼĮ×÷ÓĆĻĀÓĆCH4½«µŖŃõ»ÆĪļ»¹ŌĪŖN2æÉŅŌĻū³żµŖŃõ»ÆĪļ“ųĄ“µÄĪŪČ¾£¬ ĒėŠ“³öCH4ÓėNO·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ_________£»ĪĀ¶ČĪŖT1Ź±ŌŚĆܱÕČŻĘ÷ÖŠŃŠ¾æCH4“߻ƻ¹ŌµŖŃõ»ÆĪļµÄ·“Ó¦£¬·“Ó¦¹ż³ĢÖŠ²śĪļN2µÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬ĒėŌŚĶ¼ÖŠ²¹»³öĪĀ¶ČĪŖT2(T2>T1)Ź±£¬n(N2)µÄ±ä»ÆĒśĻߣØŅŃÖŖøĆ·“Ó¦ŹĒ·ÅČČ·“Ó¦£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŌŚÄ³Ņ»ČŻ»żĪŖ5 LµÄĆܱÕČŻĘ÷ÄŚ£¬¼ÓČė 0.3 molµÄCOŗĶ0.3 molµÄH2O£¬ŌŚ“߻ƼĮ“ęŌŚŗĶ800”ęµÄĢõ¼žĻĀ¼ÓČČ£¬·¢ÉśČēĻĀ·“Ó¦£ŗCO£Øg£©£«H2O£Øg£© CO2£Øg£©£«H2£Øg£© ¦¤H£¾0£¬·“Ó¦ÖŠCO2µÄÅضČĖꏱ¼ä±ä»ÆĒéæöČēĶ¼£ŗ
CO2£Øg£©£«H2£Øg£© ¦¤H£¾0£¬·“Ó¦ÖŠCO2µÄÅضČĖꏱ¼ä±ä»ÆĒéæöČēĶ¼£ŗ
£Ø1£©øł¾ŻĶ¼ÉĻŹż¾Ż£¬·“Ó¦æŖŹ¼ÖĮ“ļµ½Ę½ŗāŹ±£¬COµÄ»Æѧ·“Ó¦ĖŁĀŹĪŖv£ØCO£©£½ mol/£ØL”¤min£©-1£¬øĆĪĀ¶ČĻĀµÄĘ½ŗā³£ŹżK£½ ”£
£Ø2£©ŌŚĢå»ż²»±äµÄĢõ¼žĻĀ£¬øıäĻĀĮŠĢõ¼žÖŲŠĀ“ļµ½Ę½ŗāŹ±ÄÜŹ¹Ę½ŗā³£ŹżKŌö“óµÄÓŠ £ØĢī×ÖÄø£©
AÉżøßĪĀ¶Č£»B½µµĶĪĀ¶Č£»CŌö“óŃ¹Ē棻D¼õŠ”Ń¹Ē棻E¼ÓČė“߻ƼĮ£»GŅĘ³öŅ»Ńõ»ÆĢ¼ĘųĢå
£Ø3£©ČēŅŖŅ»æŖŹ¼¼ÓČė0.1 molµÄCO”¢0.1 molµÄH2O”¢0.2 molµÄCO2ŗĶ0.2 molµÄH2£¬ŌŚĻąĶ¬µÄĢõ¼žĻĀ£¬·“Ó¦“ļĘ½ŗāŹ±£¬c£ØCO£©£½ mol/L”£
£Ø4£©Čō±£³ÖĪĀ¶ČŗĶČŻĘ÷µÄĢå»ż²»±ä£¬ŌŚ£Ø1£©ÖŠÉĻŹöĘ½ŗāĢåĻµÖŠ£¬ŌŁ³äČė0.3mol µÄĖ®ÕōĘų£¬ÖŲŠĀ“ļµ½Ę½ŗāŗó£¬COµÄ×Ŗ»ÆĀŹ £ØĢī”°Éżøß”±”¢”°½µµĶ”±»¹ŹĒ”°²»±ä”±£©£¬CO2µÄÖŹĮæ·ÖŹż £ØĢī”°Éżøß”±”¢”°½µµĶ”±»¹ŹĒ”°²»±ä”±£©”£
£Ø5£©ŌŚ“߻ƼĮ“ęŌŚŗĶ800”ęµÄĢõ¼žĻĀ£¬ŌŚÄ³Ņ»Ź±æĢ²āµĆc£ØCO£©£½c£ØH2O£©£½0.09mol/L,c£ØCO2£©£½c£ØH2£©£½0.13mol/L,Ōņ“Ė·“Ó¦ŹĒ·ń“¦ÓŚĘ½ŗāדĢ¬ £ØĢī”°ŹĒ”±»ņ”°·ń”±£©,Čōƻӊ“¦ÓŚĘ½ŗāדĢ¬ŌņøĆ·“Ó¦Ļņ ŅĘ¶Æ”££ØĢī”°Õż·½Ļņ”±»ņ”°Äę·½Ļņ”±£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŌŚĢå»ż¹Ģ¶ØµÄĆܱÕČŻĘ÷ÖŠ£¬½ųŠŠČēĻĀ»Æѧ·“Ó¦£ŗN2O4£Øg£© 2NO2£Øg£©£¬Ęä»ÆŃ§Ę½ŗā³£ŹżKŗĶĪĀ¶ČtµÄ¹ŲĻµČēĻĀ±ķ£ŗ
2NO2£Øg£©£¬Ęä»ÆŃ§Ę½ŗā³£ŹżKŗĶĪĀ¶ČtµÄ¹ŲĻµČēĻĀ±ķ£ŗ
| t /”ę | 80 | 100 | 120 |
| K | 1.80 | 2.76 | 3.45 |
  | 0 | 20 | 40 | 60 | 80 | 100 |
| n£ØN2O4£© | 2.80 | A | 2.00 | c | d | 1.60 |
| n£ØNO2£© | 0 | 0.96 | b | 2.08 | 2.40 | 2.40 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
»īŠŌĢææÉ“¦Ąķ“óĘųĪŪČ¾ĪļNO”£T”ꏱ£¬ŌŚ1LĆܱÕČŻĘ÷ÖŠ¼ÓČėNOĘųĢåŗĶĢæ·Ū£¬·¢Éś·“Ӧɜ³ÉĮ½ÖÖĘųĢåAŗĶB£¬²āµĆø÷ĪļÖŹµÄĪļÖŹµÄĮæČēĻĀ£ŗ
| | »īŠŌĢæ/mol | NO/mol | A/mol | B/mol |
| ĘšŹ¼×“Ģ¬ | 2.030 | 0.100 | 0 | 0 |
| 2 minŹ± | 2.000 | 0.040 | 0.030 | 0.030 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
µŖ»Æ¹č(Si3N4)ŹĒŅ»ÖÖŠĀŠĶĢՓɲÄĮĻ£¬ĖüæÉÓÉŹÆÓ¢Óė½¹ĢæŌŚøßĪĀµÄµŖĘųĮ÷ÖŠ£¬ĶعżŅŌĻĀ·“Ó¦ÖĘµĆ£ŗ3SiO2(s)+6C(s)+ 2N2(g)  Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)
£Ø1£©øĆ·“Ó¦µÄŃõ»Æ¼ĮŹĒ £¬2molN2²Ī¼Ó·“Ó¦×ŖŅʵē×ÓŹżĪŖ £»
£Ø2£©øĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK£½”””””””””” ””£»
£Ø3£©ČōCOµÄÉś³ÉĖŁĀŹĪŖv(CO)£½18mol”¤L-1”¤min-1£¬ŌņN2µÄĻūŗÄĖŁĀŹĪŖv(N2)£½
£Ø4£©“ļµ½Ę½ŗāŗó£¬øıäijŅ»Ķā½ēĢõ¼ž£Ø²»øıäN2”¢COµÄĮ棩£¬·“Ó¦ĖŁĀŹvÓėŹ±¼ätµÄ¹ŲĻµČēĶ¼”£Ķ¼ÖŠt4Ź±ŅżĘšĘ½ŗāŅĘ¶ÆµÄĢõ¼žæÉÄÜŹĒ £»Ķ¼ÖŠ±ķŹ¾Ę½ŗā»ģŗĻĪļÖŠCOµÄŗ¬Įæ×īøßµÄŅ»¶ĪŹ±¼äŹĒ ”£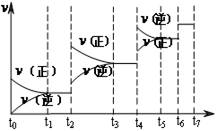
£Ø5£©ČōøĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ K£½729£¬ŌņŌŚĶ¬ĪĀ¶ČĻĀ1LĆܱÕČŻĘ÷ÖŠ£¬×ćĮæµÄSiO2ŗĶCÓė2mol N2³ä·Ö·“Ó¦£¬ŌņN2µÄ×Ŗ»ÆĀŹŹĒ (ĢįŹ¾£ŗ272 = 729)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
°±ĘųŹĒÖŲŅŖ»Æ¹¤²śĘ·Ö®Ņ»”£“«Ķ³µÄ¹¤ŅµŗĻ³É°±¼¼ŹõµÄ·“Ó¦ŌĄķŹĒ£ŗ
N2£Øg£©£«3H2£Øg£© 2NH3£Øg£© ¦¤H£½£92.4 kJ/mol”£ŌŚ500 ”ę”¢20 MPaŹ±£¬½«N2”¢H2ÖĆÓŚŅ»øö¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£¬·“Ó¦¹ż³ĢÖŠø÷ÖÖĪļÖŹµÄĮæÅØ¶Č±ä»ÆČēĶ¼ĖłŹ¾£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
2NH3£Øg£© ¦¤H£½£92.4 kJ/mol”£ŌŚ500 ”ę”¢20 MPaŹ±£¬½«N2”¢H2ÖĆÓŚŅ»øö¹Ģ¶ØČŻ»żµÄĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£¬·“Ó¦¹ż³ĢÖŠø÷ÖÖĪļÖŹµÄĮæÅØ¶Č±ä»ÆČēĶ¼ĖłŹ¾£¬»Ų“šĻĀĮŠĪŹĢā£ŗ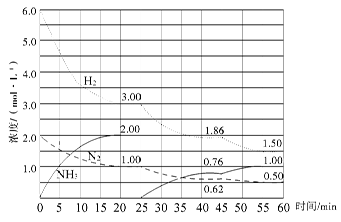
£Ø1£©¼ĘĖć·“Ó¦ŌŚµŚŅ»“ĪĘ½ŗāŹ±µÄĘ½ŗā³£ŹżK£½ ”££Ø±£Įō¶žĪ»Š”Źż£©
£Ø2£©²śĪļNH3ŌŚ5”«10 min”¢25”«30minŗĶ45”«50 minŹ±Ę½¾ł·“Ó¦ĖŁĀŹ£ØĘ½¾ł·“Ó¦ĖŁĀŹ·Ö±šŅŌv1”¢v2”¢v3±ķŹ¾£©“ӓ󵽊”ÅÅĮŠ“ĪŠņĪŖ ”£
£Ø3£©H2ŌŚČż“ĪĘ½ŗā½×¶ĪµÄĘ½ŗā×Ŗ»ÆĀŹ·Ö±šŅŌ¦Į1”¢¦Į2”¢¦Į3±ķŹ¾£¬ĘäÖŠ×īŠ”µÄŹĒ ”£
£Ø4£©ÓɵŚŅ»“ĪĘ½ŗāµ½µŚ¶ž“ĪĘ½ŗā£¬Ę½ŗāŅĘ¶ÆµÄ·½ĻņŹĒ____________£¬²ÉČ”µÄ“ėŹ©ŹĒ____________
£Ø5£©ĒėŌŚĻĀĶ¼ÖŠÓĆŹµĻß±ķŹ¾25”«60min ø÷½×¶Ī»ÆŃ§Ę½ŗā³£ŹżKµÄ±ä»ÆĶ¼Ļń”£
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
ŌŚČŻ»żĪŖ1 LµÄĆܱÕČŻĘ÷ÖŠ£¬½ųŠŠČēĻĀ·“Ó¦£ŗ A(g)£«2B(g) 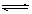 C(g)£«D(g)£¬ŌŚ²»Ķ¬ĪĀ¶ČĻĀ£¬DµÄĪļÖŹµÄĮæn(D)ŗĶŹ±¼ätµÄ¹ŲĻµČēĶ¼”£
C(g)£«D(g)£¬ŌŚ²»Ķ¬ĪĀ¶ČĻĀ£¬DµÄĪļÖŹµÄĮæn(D)ŗĶŹ±¼ätµÄ¹ŲĻµČēĶ¼”£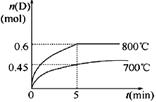
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©700”ꏱ£¬0”«5minÄŚ£¬ŅŌB±ķŹ¾µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ_______”£
£Ø2£©ÄÜÅŠ¶Ļ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ__________”£
A£®ČŻĘ÷ÖŠŃ¹Ēæ²»±ä B£®»ģŗĻĘųĢåÖŠc(A)²»±ä
C£®vÕż(B)£½2vÄę(D) D£®c(A)£½c(C)
£Ø3£©Čō×ī³õ¼ÓČė1.0 mol AŗĶ2.2 mol B£¬ĄūÓĆĶ¼ÖŠŹż¾Ż¼ĘĖć800”ꏱµÄĘ½ŗā³£ŹżK£½___ _______£¬øĆ·“Ó¦ĪŖ__________·“Ó¦(Ģī”°ĪüČČ”±»ņ”°·ÅČČ”±)”£
£Ø4£© 800”ꏱ£¬Ä³Ź±æĢ²āµĆĢåĻµÖŠĪļÖŹµÄĮæÅضČČēĻĀ£ŗc(A)£½0.06 mol/L£¬c(B)£½0.50 mol/L£¬c(C)£½0.20 mol/L£¬c(D)£½0.018 mol/L£¬Ōņ“ĖŹ±øĆ·“Ó¦______ ____(Ģī”°ĻņÕż·½Ļņ½ųŠŠ”±”¢”°ĻņÄę·½Ļņ½ųŠŠ”±»ņ”°“¦ÓŚĘ½ŗāדĢ¬”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
¹¤ŅµÉĻĄūÓĆCOŗĶĖ®ÕōĘųŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦ÖĘČ”ĒāĘų£ŗCO(g)+H2O(g)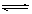 CO2(g)+H2(g)Ä³ŃŠ¾æŠ”×é·Ö±šŌŚĢå»ż¾łĪŖ2LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ¼ÓČėŅ»¶ØĮæµÄ·“Ó¦Īļ£¬Ź¹Ęä·¢Éś·“Ó¦£¬Ļą¹ŲŹż¾ŻČēĻĀ£ŗ
CO2(g)+H2(g)Ä³ŃŠ¾æŠ”×é·Ö±šŌŚĢå»ż¾łĪŖ2LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ¼ÓČėŅ»¶ØĮæµÄ·“Ó¦Īļ£¬Ź¹Ęä·¢Éś·“Ó¦£¬Ļą¹ŲŹż¾ŻČēĻĀ£ŗ
| ČŻĘ÷±ąŗÅ | ĪĀ¶Č”ę | ĘšŹ¼Įæ/mol | Ę½ŗāĮæ/mol | “ļµ½Ę½ŗāµÄŹ±¼ä/min | “ļµ½Ę½ŗāŹ±ĢåĻµÄÜĮæµÄ±ä»Æ/kJ | ||
| CO | H2O | CO2 | H2 | ||||
| ¢Ł | 650 | 1 | 2 | 0£®4 | 0£®4 | 5 | 16£®4 |
| ¢Ś | 650 | 2 | 4 | | | t1 | Q1 |
| ¢Ū | 900 | 2 | 4 | 1£®6 | 1£®6 | t2 | Q2 |
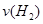 =__________ӣ
=__________”£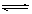 CO2(g)+H2(g) ”÷H= -41kJ/mol
CO2(g)+H2(g) ”÷H= -41kJ/mol²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com