
【题目】工业上可由乙苯生产苯乙烯:![]()
![]() ,下列说法正确的是( )
,下列说法正确的是( )
A.可用酸性高锰酸钾溶液鉴别乙苯和苯乙烯
B.苯乙烯能使溴水褪色,是因为两者发生了加成反应
C.乙苯和苯乙烯苯环上的一氯代物均为3种
D.乙苯和苯乙烯分子内共平面的碳原子数最多均为7个
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】下列有关用水杨酸和乙酸酐制备阿司匹林(乙酰水杨酸)的说法中不正确的是( )
A.制备阿司匹林的反应属于取代反应
B.待反应结束后向锥形瓶中加水,冰水浴中冷却结晶,减压过滤,用少量冷水淋洗锥形瓶收集所有晶体
C.粗产品中常混有聚合物杂质,可利用![]() 溶液溶解、过滤、洗涤、盐酸酸化、结晶等操作进行精制
溶液溶解、过滤、洗涤、盐酸酸化、结晶等操作进行精制
D.可用![]() 溶液检验阿司匹林中是否含有未反应完的水杨酸
溶液检验阿司匹林中是否含有未反应完的水杨酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷化硼![]() 是一种具有超高热导率的新型半导体材料,其制备原理为
是一种具有超高热导率的新型半导体材料,其制备原理为![]() 。下列说法错误的是( )
。下列说法错误的是( )
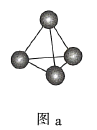

A.图a表示![]() 结构,
结构,![]() 分子中成键电子对与孤电子对的数目之比为3:1
分子中成键电子对与孤电子对的数目之比为3:1
B.图b表示晶态单质硼![]() 的基本结构单元,该基本结构单元为正二十面体
的基本结构单元,该基本结构单元为正二十面体
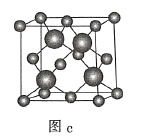
C.图c表示![]() 晶胞结构,
晶胞结构,![]() 原子的配位数为4
原子的配位数为4
D.该反应所涉及的元素中,I的原子半径最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,W、Z同主族,Y的族序数等于其周期数,X、Y、Z的最外层电子数之和等于10,W、Z形成的一种化合物能使品红溶液褪色。下列说法正确的是( )
A.原子半径:W>X>Y>Z
B.W、X、Y三种元素组成的化合物的水溶液呈中性
C.常温下,Y易溶于Z的最高价氧化物对应的水化物的浓溶液
D.W、X、Z三种元素组成的某种化合物与盐酸反应时,可能有单质Z析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)第四周期中,未成对电子数最多的元素是________,(填名称)它位于第________族;核外电子排布式是__________________。它有________种运动状态不同的电子,其价电子排布图为:______________。
(2)已知NH5为离子化合物,写出其电子式:________。
(3)某同学根据掌握的知识分析Mg的核外电子排布为![]() 。该同学所画的电子排布图违背了________。
。该同学所画的电子排布图违背了________。
(4)在基态 14C原子中,核外存在________对自旋相反的电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料制取复合氧化钴的流程如下:
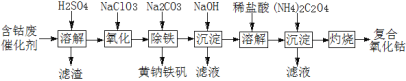
(1)用H2SO4溶解后过滤,得到的滤渣是____(填化学式)。将滤渣洗涤2~3次,再将洗液与滤液合并的目的是____。
(2)在加热搅拌条件下加入NaClO3,将Fe2+氧化成Fe3+,反应的离子方程式是____。
(3)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]。
3Fe2++2[Fe(CN)6]3 =Fe3[Fe(CN)6]2↓(蓝色沉淀)
4Fe3++3[Fe(CN)6]4 =Fe4[Fe(CN)6]3↓(蓝色沉淀)
确定Fe2+是否氧化完全的方法是____。(仅供选择的试剂:铁氰化钾溶液、亚铁氰化钾溶液、铁粉、KSCN溶液)
(4)向氧化后的溶液中加入适量的Na2CO3调节酸度,使之生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的离子方程式:____。
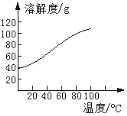
(5)已知CoCl2的溶解度曲线如图所示。向碱式碳酸钴沉淀中加入足量稀盐酸边加热边搅拌至完全溶解后,需趁热过滤的原因是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最新研究表明,咖啡中含有的咖啡酸能使人心脑血管更年轻。咖啡酸的球棍模型如图所示,下列有关咖啡酸的叙述不正确的是( )

A.咖啡酸的分子式为C9H8O4
B.咖啡酸中的含氧官能团只有羧基、酚羟基
C.咖啡酸可以发生氧化反应、消去反应、酯化反应、加聚反应
D.![]() 是咖啡酸的一种同分异构体,1mol该物质最多可消耗3molNaOH
是咖啡酸的一种同分异构体,1mol该物质最多可消耗3molNaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。当向其中加入少量酸或碱时,溶液的酸碱性变化不大。回答下列问题:
(1)将该溶液两等分,向其中加入少量盐酸时,发生反应的离子方程式为______;另一份加入少量KOH溶液时,发生反应的离子方程式为______。
(2)现将0.04molL-1HA溶液和0.02molL-1NaOH溶液等体积混合,得到缓冲溶液。
①若HA为HCN,该缓冲溶液显碱性,则溶液中c(Na+)______c(CN-)。(填“<”“=”或“>”);
②若HA为CH3COOH,该缓冲溶液显酸性。则溶液中所有的离子按浓度由大到小排列的顺序是______。
(3)缓冲溶液一般是由浓度较大的弱酸及其共轭碱所组成,其pH值的近似计算公式为:pH=pK酸+lg[c共轭碱/c酸]。人体血液中的H2CO3-HCO3-平衡起到缓冲作用。实测某人血液的pH=7.2,c(![]() )=2.3×10-2mol/L,且已知血液中的H2CO3的pKa1=6.2。则此人血液中的c(H2CO3)=______mol/L。
)=2.3×10-2mol/L,且已知血液中的H2CO3的pKa1=6.2。则此人血液中的c(H2CO3)=______mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com