
【题目】草酸(乙二酸)存在于自然界的植物中。草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水。草酸晶体(H2C2O4·2H2O)无色,熔点为101 ℃,易溶于水,受热脱水、升华,170 ℃以上分解。回答下列问题:

(1)装置C中可观察到的现象是_________________________________,装置B的主要作用是________。
(2)请设计实验验证草酸的酸性比碳酸强____________________________________。
【答案】有气泡逸出,澄清石灰水变浑浊 冷凝(水蒸气、草酸等),防止挥发出来的草酸进入装置C反应生成草酸钙沉淀,干扰CO2的检验 向碳酸氢钠溶液中滴加草酸溶液,观察是否产生气泡,若有气泡产生,说明草酸酸性强于碳酸
【解析】
根据草酸的性质熔点为101 ℃,易溶于水,受热脱水、升华,170 ℃以上分解,草酸受热生成二氧化碳,二氧化碳使澄清石灰水变浑浊。
(1)根据草酸的性质熔点为101 ℃,易溶于水,受热脱水、升华,170 ℃以上分解,草酸受热分解产生CO2可使澄清石灰水变浑浊,冰水的作用是冷却挥发出来的草酸,避免草酸进入装置C反应生成草酸钙沉淀,干扰CO2的检验,故答案为:有气泡逸出,澄清石灰水变浑浊;冷凝(水蒸气、草酸等),防止挥发出来的草酸进入装置C反应生成草酸钙沉淀,干扰CO2的检验。
(2)利用强酸制弱酸的原理设计,向NaHCO3溶液中滴加草酸溶液,观察是否产生气泡即可证明草酸酸性强于碳酸,故答案为:向碳酸氢钠溶液中滴加草酸溶液,观察是否产生气泡,若有气泡产生,说明草酸酸性强于碳酸。


科目:高中化学 来源: 题型:
【题目】高温时空气中的N2和O2会反应生成NO而污染大气:N2(g)+O2(g)=2NO(g)。试通过计算说明在1 200 ℃的条件下,此反应能否正向自发进行?估算自发进行的最低温度是多少______?[已知该反应:ΔH=+180.50 kJ·mol-1,ΔS=247.7 J·mol-1·K-1]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知取H2(g)+2ICl(g)=I2(g)+2HCl(g),该反应分①②两步进行,其能量曲线如图所示,下列有关说法正确的是( )
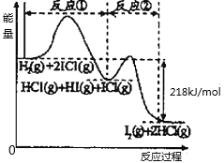
A.反应①为吸热反应
B.反应①和②均是同种元素间发生的氧化还原反应
C.反应①比反应②的速率慢,与相应正反应的活化能有关
D.H2(g) +2ICl(g)=I2(g)+2HCl(g) △H=-218kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本反应类型的关系如图所示,下列化学反应属于阴影3区域的是

A.2HClO![]() 2HCl+O2↑
2HCl+O2↑
B.NH4HCO3![]() NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O=4Fe(OH)3
D.Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:
H2(g)+![]() O2(g)
O2(g)![]() H2O(g) △H1
H2O(g) △H1
![]() N2(g)+O2(g)
N2(g)+O2(g)![]() NO2(g) △H2
NO2(g) △H2
![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g) △H3
NH3(g) △H3
则反应4NH3(g)+7O2(g)=4NO2(g)+6H2O(g)的△H为( )
A.△H1+△H2+△H3B.2△H1+2△H2-2△H3
C.6△H1+4△H2+4△H3D.6△H1+4△H2-4△H3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将含有0.4 mol CuSO4和0.1 mol NaCl的水溶液用惰性电极电解一段时间后,若在一个电极上得到6.4g Cu,则另一电极上生成气体(在标准状况)的体积为
A.1.12 LB.1.68 LC.2.24 LD.3.36L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知常温下几种弱酸或弱碱的电离平衡常数(Ka或Kb)如下表所示:
酸或碱 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HCN | 5×10-10 |
NH3H2O | 1.8×10-5 |
H2SO3 | K1=1.5×10-2,K2=1.1×10-7 |
回答下列问题:
(1)CH3COONH4的水溶液呈中性,其理由是_____________,溶液中各离子浓度大小的关系是___________________。
(2)等物质的量浓度的下列五种溶液:①NH3H2O ②(NH4)2SO3 ③NaHSO3 ④Na2SO3
⑤H2SO3溶液中水的电离程度由大到小的排列顺序为________(填序号)。
(3)向25 mL 0.10 molL-1盐酸中滴加氨水至过量,该过程中离子浓度大小关系可能正确的是________(填字母)。
A.c(Cl-)=c(NH4+)>c(H+)=c(OH-) B. c(NH4+)>c(Cl-)=c(H+)>c(OH-)
C.c(NH4+)>c(OH-)>c(Cl-)>c(H+) D.c(OH-)>c(NH4+)>c(H+)>c(Cl-)
(4)在室温下,0.05 molL-1的NaCN溶液的pH约为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL0.1mol·L-1NaOH溶液中加入0.1mol·L-1的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )

A.b点所示溶液中[A-]>[HA]
B.a、b两点所示溶液中水的电离程度相同
C.pH=7时,[Na+]=[A-]+[HA]
D.a点所示溶液中[Na+]>[A-]>[H+]>[HA]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盖斯定律指出:化学反应的反应热只与反应的始态和终态有关,而与具体反应途径无关。物质A在一定条件下可发生一系列转化,由图判断下列错误的是
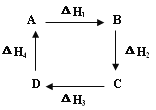
A.ΔH1+ΔH2+ΔH3+ΔH4=1
B.A→D,ΔH=-ΔH4
C.ΔH1+ΔH2 =-ΔH3-ΔH4
D.B→D ,ΔH=ΔH2+ΔH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com