
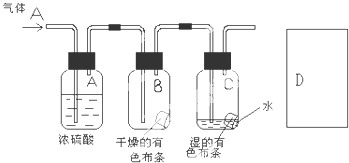
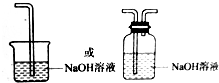
 ,
, ;
;
| ||
| ||


科目:高中化学 来源: 题型:
 目前已研制出一种用磺酸类质子作溶剂的酸 性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )
目前已研制出一种用磺酸类质子作溶剂的酸 性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )| A、通入乙醇的电极为该电池的正极 |
| B、放电过程中,电源内部的H+从正极区向负极区迁移 |
| C、该电池的正极反应为:4H++O2+4e-=2H2O |
| D、用该电池做电源,用惰性电极电解饱和NaCl溶液时,每消耗0.2 mol C2H5OH,阴极产生标准状况下气体的体积为13.44 L |
查看答案和解析>>
科目:高中化学 来源: 题型:
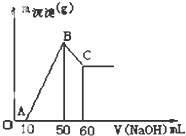 把一小块镁铝金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.
把一小块镁铝金溶于100mL盐酸中,然后向其中滴入1mol?L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol/L的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(OH-)>c(H+) |
| B、0.1 mol/L的NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) |
| C、将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-) |
| D、在25℃100 mL NH4Cl溶液中:c(H+)=c(NH3?H2O)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
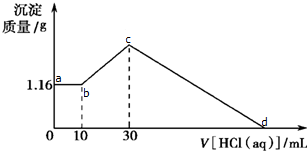 将m g由NaOH、MgCl2、AlCl3三种固体组成的混合物投入足量水中,得到一悬浊液,将该悬浊液分为两等份:一份经过滤、洗涤、干燥得1.16g白色沉淀,在另一份悬浊液中逐滴加入1mol?L-1的HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示.
将m g由NaOH、MgCl2、AlCl3三种固体组成的混合物投入足量水中,得到一悬浊液,将该悬浊液分为两等份:一份经过滤、洗涤、干燥得1.16g白色沉淀,在另一份悬浊液中逐滴加入1mol?L-1的HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| 电解 |
| A、G、Y、Q、Z、X |
| B、X、Z、Q、G、Y |
| C、X、Z、Q、Y、G |
| D、G、Q、Y、Z、X |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com