
【题目】使用如图所示装置进行化学小实验,请填写下列空白: 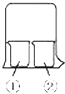
(1)若①中放一片湿润的红色石蕊试纸,②装有浓氨水,可观察到的实验现象为
(2)若①装有AlCl3溶液,②装有浓氨水,可观察到的实验现象为
(3)若①装有浓硝酸,②装有浓氨水,可观察到的实验现象为
(4)若①装有浓硝酸,②装有Na2SO3溶液,实验时有无色气体产生,该气体逐渐变为红棕色,用化学方程式表示无色气体变为红棕色的原因
【答案】
(1)石蕊试纸变蓝
(2)①中有白色沉淀
(3)烧杯中有白烟生成
(4)2NO+O2=2NO2
【解析】解:(1)浓氨水具有挥发性,挥发出的氨气为碱性气体,能够与水反应生成一水合氨,一水合氨电离生成氢氧根离子,能够使石蕊试纸变蓝, 所以答案是:石蕊试纸变蓝;(2)浓氨水以挥发,氨气与水反应生成一水合氨,与氯化铝反应生成氢氧化铝沉淀;
所以答案是:①中有白色沉淀生成;(3)浓硝酸、浓氨水易挥发,硝酸与氨气反应生成硝酸铵,所以会看到产生大量白烟;
所以答案是:烧杯中有白烟生成;(4)一氧化氮不稳定,与氧气反应生成红棕色的二氧化氮,化学方程式:2NO+O2=2NO2 , 所以答案是:2NO+O2=2NO2 .
【考点精析】通过灵活运用氨的化学性质,掌握与水反应,NH3是惟一能使润湿的红色石蕊试纸交蓝的气体,常用此性质检验NH3;与酸反应:NH3+HCl=NH4Cl(生成白烟);与O2反应:4NH3+5O2=4NO+6H2O+Q;


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】下列关于氯气的叙述中不正确的是
A. 氯气呈液态时称为液氯 B. 氯气的密度比空气大
C. 氯气的水溶液含有多种分子 D. 氯气在碱性溶液中漂白性会增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,有甲、乙两容器,甲体积可变压强不变,乙保持体积不变。向两容器中分别充入1molA、3molB,此时两容器体积均为500mL,温度为T℃。保持温度不变发生反应:A(g)+3B(g) ![]() 2C(g)+D(s) ΔH<0
2C(g)+D(s) ΔH<0
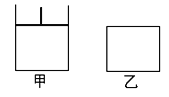
(1)下列选项中,能表明甲和乙容器中反应一定达到平衡状态的是 。
A.混合气体的总质量不随时间改变
B.2 v正(C) = 3v逆(B)
C.A、B转化率相等
D.物质D的质量不随时间改变
(2)2min后甲容器中反应达到平衡,测得C的浓度为2mol/L,此时甲容器的体积为_______mL。
(3)当甲乙两容器中反应都达平衡时,甲和乙中B的转化率α甲(B) _________α乙(B)。(填“>”“<”或“=”)
(4)其它条件不变,甲中如果从逆反应方向开始反应建立平衡,要求平衡时C的物质的量与(2)中平衡时C的物质的量相等,则需要加入C的物质的量n(C)=________mol,加入D的物质的量n(D)应该满足的条件为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定原理在中学化学实验中有着极为重要的应用,现欲采用滴定的方法测定样品中硫酸亚铁的质量分数(约45%),根据反应:
2KMnO4+10FeSO4+8H2SO4 ═ 2MnSO4+5Fe2(SO4)3+K2SO4+8H2O。
步骤如下:
①称量样品3.0 g配成100 mL溶液;
②取20.00 mL待测液,置于锥形瓶中,再加入适量硫酸;
③将0.1 mol/L的标准KMnO4溶液装入滴定管,调节液面至a mL处(见下图);

④滴定待测液至滴定终点时,滴定管液面读数为6;
⑤重复滴定2~3次;
⑥计算。
(1)实验步骤③中的溶液体积读数为________mL。
(2)实验步骤①、③中还需要使用的最主要的仪器分别为:①________、③________。
(3)在步骤④的滴定操作中是否需要在待测液中加入指示剂________。(填“是”或“否”)
(4)若滴定时每次消耗KMnO4溶液体积的平均值为V mL,则绿矾样品的纯度为________。(列出算式即可)如果步骤③中读数时俯视,则最终结果________。(填“偏大”、“不变”或“偏小”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积为2L的容器中加入1mol N2和6mol H2进行可逆反应:N2+3H22NH3 , 2min后测得N2的物质的量为0.6mol,则:
(1)2min内,N2的物质的量减少了0.4mol,H2的物质的量减少了mol,NH3的物质量增加了mol.
(2)若用N2的浓度变化来表示该反应的反应速率,则v(N2)=mol/(Lmin).
(3)若用H2的浓度变化来表示该反应的反应速率,则v(H2)=mol/(Lmin).
(4)若用NH3的浓度变化来表示该反应的反应速率,则v(NH3)=mol/(Lmin).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C8H10O的芳香族化合物,遇三氯化铁溶液不显色,能与金属钠反应放出氢气,满足条件的同分异构体有( )
A.大于10种
B.10种
C.6种
D.5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com