
| A. | CH4 | B. | NH3 | C. | BF3 | D. | SO3 |
分析 微粒中立体构型是平面三角形说明中心原子价层电子对个数是3且不含孤电子对,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数.
解答 解:A.CH4分子中碳原子价层电子对个数=4+$\frac{1}{2}$(4-4×1)=4,且不含孤电子对,所以其立体构型是正四面体形,故A错误;
B.氨气分子中氮原子价层电子对个数=3+$\frac{1}{2}$(5-3×1)=4,且含有一个孤电子对,所以其立体构型是三角锥形,故B错误;
C.BF3中价层电子对个数=3+$\frac{1}{2}$(3-3×1)=3,不含孤电子对,所以空间构型是平面三角形,故C正确;
D.SO3中价层电子对个数=3+$\frac{1}{2}$(6-2×3)=3,立体构型为平面三角形,故D正确;
故选CD.
点评 本题考查了粒子空间构型的判断,根据价层电子对互斥理论来分析解答即可,难点是孤电子对个数的计算,题目难度中等.


 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案科目:高中化学 来源: 题型:选择题
| A. | 元素金属性:Z>W | |
| B. | X与Y可形成多种共价化合物 | |
| C. | 化合物Z2Y2中既含离子键,又含共价键 | |
| D. | Y元素只能形成一种单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
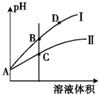 已知H2CO3的Ka1=4.2×10-7、Ka2=5.6×10-11;HClO的Ka=3.0×10-8,HF的Ka=3.5×10-4.
已知H2CO3的Ka1=4.2×10-7、Ka2=5.6×10-11;HClO的Ka=3.0×10-8,HF的Ka=3.5×10-4.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n1=n2 | B. | n1>n2 | C. | n1<n2 | D. | C( F-)<C(CN-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
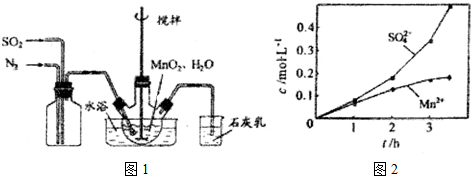
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤⑥⑦ | B. | ②③④⑤⑦ | C. | ①④⑤⑥⑦ | D. | ①③⑤⑥⑦ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com