
【题目】下列物质与水充分混合,能得到溶液的是( )
A. CCl4 B. 苯
C. 花生油 D. CH3COOH
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 按系统命名法,化合物![]() 的名称为2, 4-二乙基-丙基辛烷
的名称为2, 4-二乙基-丙基辛烷
B. 若两种二肽互为同分异构体,则二者的水解产物一定不相同
C. 分子式为C5H5O2Cl并能与饱和NaHCO3溶液反应产生气体的有机物有(不含立休结构)有12种
D. 某有机物的结构简式是 ,该有机物能够发生加成反应、取代反应、缩聚反应和消去反应
,该有机物能够发生加成反应、取代反应、缩聚反应和消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的两种固态物质熔化或升华时,克服微粒间相互作用力属于同种类型的是( )
A.碘和氯化钾B.金刚石和蓝矾C.二氧化硅和干冰D.冰和冰醋酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种物质随着X的变化,Y发生相应的变化,其变化关系如图所示。

(1)若X表示的是物质的量,则Y表示的不可能是_____(填序号,下同)
①物质的量 ②物质的体积 ③物质所含分子或原子的数目 ④物质的摩尔质量
(2)若A、B、C均为气体且压强恒定时,X表示的是温度,则Y表示的可能是______。
①气体的质量 ②气体的分子数 ③气体的体积 ④气体的摩尔质量
(3)若A、B、C均为气体,Y表示在相同条件下气体的体积,X表示的是气体的质量。
①相同条件下A、B、C三种气体的密度由大到小的顺序是_____(用字母A、B、C表示,下同)。
②A、B、C三种气体的摩尔质量由大到小的顺序是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学家屠呦呦因开创性地运用萃取的原理从中草药中分离出青蒿素并应用于疟疾治疗获得今年的诺贝尔医学奖。萃取实验中用到的主要仪器是 ( )
A. 长颈漏斗 B. 分液漏斗
C. 圆底烧瓶 D. 蒸馏烧瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
氯吡格雷是一种血小板聚集抑制剂,该药物以![]() 为原料的合成路线如图:
为原料的合成路线如图:
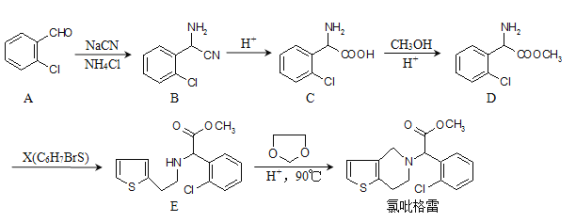
请根据以上信息,结合自己掌握的知识和具有的经验回答下列问题:
(1)分子C中无氧官能团的名称为____________。 命名为__________。
命名为__________。
(2)D→E的反应类型是_________反应。
(3)X的结构简式为___________________。
(4)下列叙述正确的是________(填序号)。
A.A物质中所有原子均可共面 B.C物质可发生取代、氧化、还原反应
C.![]() 在水中溶解度小 D.E中有两个手性碳原子
在水中溶解度小 D.E中有两个手性碳原子
(5)分子C在一定条件下生成一种含有3个六元环的产物的化学方程式为_____________。
(6)同时满足下列两个条件的B的同分异构体共有_____种(不包括B)。
①与B含有相同的官能团;②苯环上的取代基不超过2个。
(7)已知:![]() ,则由乙醇、甲醇为有机原料制备化合物
,则由乙醇、甲醇为有机原料制备化合物![]() 需要经历的反应类型有______(填序号)。
需要经历的反应类型有______(填序号)。
①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应
写出制备化合物![]() 的最后一步反应:______________________。
的最后一步反应:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Mg、Al的有关性质的叙述正确的是( )
A.还原性:Na>Mg>Al
B.第一电离能:Na<Mg<Al
C.电负性:Na>Mg>Al
D.碱性:NaOH<Mg(OH)2<Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校环保小组学生处理污水样品时,需要配制450mL0.1mol/L硫酸。
(1)如图所示仪器中,配制上述溶液肯定不需要的仪器是_____(填字母),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是______(填仪器名称)。

(2)如果用5.0mol/L的硫酸来配制上述硫酸,则需该硫酸的体积为_____。
(3)在容量瓶的使用方法中,下列操作正确的是____(填字母)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水接近标线l~2cm处,用滴管加蒸馏水至标线
D.定容后,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(4)定容时,若仰视刻度线,则所配溶液物质的量浓度___(填“偏大”“偏小”“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017·新课标Ⅲ]砷(As)是第四周期ⅤA族元素,可以形成As2S3、As2O5、H3AsO3、H3AsO4等化合物,有着广泛的用途。回答下列问题:
(1)画出砷的原子结构示意图____________。
(2)工业上常将含砷废渣(主要成分为As2S3)制成浆状,通入O2氧化,生成H3AsO4和单质硫。写出发生反应的化学方程式________。该反应需要在加压下进行,原因是________________________。
(3)已知:As(s)+ ![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+ ![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+ ![]() O2(g)=As2O5(s) ΔH3
O2(g)=As2O5(s) ΔH3
则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
(4)298 K时,将20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,发生反应:![]() (aq)+I2(aq)+2OH(aq)
(aq)+I2(aq)+2OH(aq)![]()
![]() (aq)+2I(aq)+ H2O(l)。溶液中c(
(aq)+2I(aq)+ H2O(l)。溶液中c(![]() )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。

①下列可判断反应达到平衡的是__________(填标号)。
a.溶液的pH不再变化
b.v(I)=2v(![]() )
)
c.c(![]() )/c(
)/c(![]() )不再变化
)不再变化
d.c(I)=y mol·L1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
③tm时v逆_____ tn时v逆(填“大于”“小于”或“等于”),理由是_____________。
④若平衡时溶液的pH=14,则该反应的平衡常数K为___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com