
����Ŀ����25 ��ʱ��AgCl�İ�ɫ����Һ�У����μ����Ũ�ȵ�KI��Һ��Na2S��Һ���۲쵽���������ȳ��ֻ�ɫ���������ճ��ֺ�ɫ��������֪�й����ʵ��ܶȻ�Ksp(25 ��)���£�
AgCl | AgI | Ag2S | |
Ksp | 1.8��10��10 | 8.51��10��16 | 6.3��10��50 |
��������������ǣ� ��
A.����ת����ʵ�ʾ��dz����ܽ�ƽ����ƶ�
B.�ܽ��С�ij�������ת��Ϊ�ܽ�ȸ�С�ij���
C.AgCl�����ڵ����ʵ���Ũ�ȵ�NaCl��CaCl2��Һ�е��ܽ�̶���ͬ
D.25 ��ʱ���ڱ���AgCl��AgI��Ag2S��Һ�У�����Ag����Ũ�Ȳ�ͬ
���𰸡�C
��������
A. ����ת����ʵ�ʾ�������������ת��Ϊ�����ܵ����ʣ������ڳ����ܽ�ƽ����ƶ�����A��ȷ��
B. ������ͬ���͵��������Σ�һ��������ܶȻ���ij�������ת�����ܶȻ�С�ij���������AgCl�İ�ɫ����Һ�м���KI��Һ��������AgI��������B��ȷ��
C. �����ܶȻ��dz�������������Ũ�ȴ���������Ũ��С����C����
D. ����AgCl��AgI��Ag2S��Һ��Ag+��Ũ�ȷֱ�Ϊ��![]() ��1��10-5mol/L��
��1��10-5mol/L��![]() ��3��10-8mol/L��
��3��10-8mol/L��![]() ��2��10-16mol/L��Ag+��Ũ�Ȳ�ͬ����D��ȷ��
��2��10-16mol/L��Ag+��Ũ�Ȳ�ͬ����D��ȷ��
��ĿҪ��ѡ�����ģ���ѡC��


 Сѧ��10���ӿ������100��ϵ�д�
Сѧ��10���ӿ������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������ܺ����Ա��㷺Ӧ�������ࡢ���ӡ������ȹ�ҵ���϶�ӰҺ������Ҫ��Na3Ag(S2O3)2��ʽ���ڣ�ʵ�����÷϶�ӰҺ�Ʊ�Ag�ľ���������ͼ��ʾ��
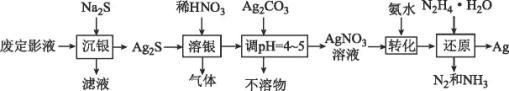
ע������ԭ��ʱ����Ag+ֱ����N2H4H2O��Ӧ���ڼ��ң����Բ��ü��백ˮ��ʹAg+�백�γ�[Ag(NH3)2]+������Ag+��Ũ�ȣ��Ӷ���Ӧ����Ag+������������ʹ��Ӧ�ܹ�ƽ�Ƚ��С�
�ش��������⣺
��1����������ʱ������������___(�ѧʽ����
��2��N2H4H2O(ˮ���£�Ϊ��ɫ������״����Һ�壬����ǿ��ԭ�ԣ�ʵ�����Ʊ�ԭ��ΪNaClO+2NH3=N2H4H2O+NaCl�������õ���ʵ��װ����ͼ��ʾ��
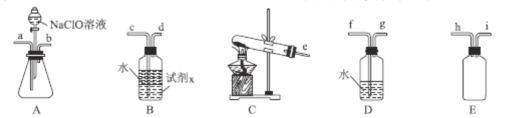
�ٱ�ʵ�����ò�����װ����___��(����ĸ�����Լ�x��___(�ѧʽ����дһ�֣���
�ڼ���NaClO��ҺʱҪ�����μӣ�Ŀ����___��
�۰����������ҵķ�������װ�õ�����˳��Ϊ___(�������ӿ�Сд��ĸ����
��3��AgNO3����������ֽ⡣������������AgNO3��Һ����Ũ���ɻ��AgNO3���壬ʵ��װ����ͼ��ʾ��

��ʹ����ձõ�Ŀ����___��
�ڲⶨAgNO3����Ĵ���(���ʲ����뷴Ӧ����ȡ2.00g�Ʊ���AgNO3���壬��ˮ�ܽ⣬���ݵ�100mL��ȷ��ȡ25.00mL��Һ���ữ����뼸��NH4Fe(SO4)2��Һ��ָʾ��������0.1000molL-1NH4SCN����Һ�ζ�������NH4SCN����Һ��ƽ�����Ϊ29.00mL���������AgNO3����������Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������е�һ����������巢����Ӧ��xA(g) ��yB(g)![]() z C(g)��ƽ��ʱ���A��Ũ��Ϊ0.50 mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ��Ϊ0.30 mol/L�������й��ж���ȷ���ǣ� ��
z C(g)��ƽ��ʱ���A��Ũ��Ϊ0.50 mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ��Ϊ0.30 mol/L�������й��ж���ȷ���ǣ� ��
A.x��y < zB.ƽ��������Ӧ�����ƶ�
C.C����������½�D.B��ת��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���� ( )��
A.���������������������ֱ���ȫȼ�գ����߷ų�������
B.����C(ʯī)��C(���ʯ) ��H=+119kJ��mol��L-1 ����֪�����ʯ��ʯī�ȶ�
C.��ϡ��Һ�У�H��(aq)+OH-(aq)=H2O(l) ��H=-57.31 kJ��mol-1��������0.5mol H2SO4��Ũ������1mol NaOH��Һ��ϣ��ų�����������57.3 kJ
D.��101kPaʱ��2g H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2(g)+O2(g)=2H2O(l) ��H =+285.8 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��LiFePO4��ؾ����ȶ��Ըߡ���ȫ���Ի����Ѻõ��ŵ㣬�����ڵ綯��������ط�ӦΪ��FePO4+Li ![]() LiFePO4����ص�����������LiFePO4������������ʯī����U�������Ϊ����ʡ������й�LiFePO4���˵����ȷ���� �� ��
LiFePO4����ص�����������LiFePO4������������ʯī����U�������Ϊ����ʡ������й�LiFePO4���˵����ȷ���� �� ��
A.�ɼ�����������ߵ���ʵĵ�����
B.�ŵ�ʱ����ڲ�Li+���ƶ�.
C.�������У���ظ������ϵ���������
D.���ʱ�����������ӦΪ��FePO4+Li++e-=LiFePO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��������ͨ��5 min����ͭ�缫���������ӣ��Իش�
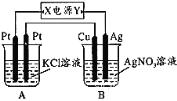
�ٵ�Դ�缫X������Ϊ________(��������������������)��
�ڵ���B�������ĵ缫��Ӧʽ��________��
����KCl��Һ�������200 mL����ͭ�缫����������2.16gʱA����Һ��pH=_____(���Ե��ǰ����Һ����ı仯)����Ҫʹ�������Һ�ָ�������ǰ��ȫ��ͬ��״̬����Ӧ����____________(�����ʵ����༰����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ö��Ե缫��ⷨ�Ʊ�����[H3BO3��B(OH) 3]�Ĺ���ԭ����ͼ��ʾ(��Ĥ����Ĥ�ֱ�ֻ���������Ӻ�������ͨ��)�������й�˵����ȷ���ǣ� ��

A. �������������������������Ϊ1��2 B. b���ĵ缫��ӦʽΪ2H2O��2e��=O2��+4H+
C. ��Ʒ���з����ķ�Ӧ��B(OH)3+OH��=B(OH)4�� D. ÿ����1 mol H3BO3��Ʒ��NaOH��Һ����22g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�һ�����ܱ������У�����һ������һ������������̼������ѧ��Ӧ��C(s)+2NO(g)![]() CO2(g)+N2(g)��ƽ��ʱc(NO)���¶�T�Ĺ�ϵ��ͼ��ʾ��������˵����ȷ���ǣ� ��
CO2(g)+N2(g)��ƽ��ʱc(NO)���¶�T�Ĺ�ϵ��ͼ��ʾ��������˵����ȷ���ǣ� ��
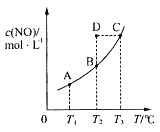
A.�÷�Ӧ�Ħ�H>0
B.���÷�Ӧ��T1��T2��ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1<K2
C.��T2��ʱ������Ӧ��ϵ����״̬D�����ʱv��>v��
D.��״̬B��C��D��ѹǿ�ֱ�Ϊp(B)��p(C)��p(D)����p(C)=p(D)>p(B)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2�ڹ�ҵ������Ҫ����;����ش�
I.��CrO3��������CO2��������(C2H6)����ϩ(C2H4)�ķ�Ӧ��������:
��C2H6(g)![]() C2H4(g)+H2(g) ��H1��
C2H4(g)+H2(g) ��H1��
��3H2(g)+2CrO3(s) =3H2O(g)+Cr2O3(s) ��H2��
��Cr2O3(s)+3CO2(g)=3CO(g)+2CrO3(s) ��H3��
(1)��ӦC2H6(g)+CO2(g)![]() C2H4(g)+CO(g)+H2O(g)�ķ�Ӧ����H=____________ (�ú���H1����H2����H3�Ĵ���ʽ��ʾ)��
C2H4(g)+CO(g)+H2O(g)�ķ�Ӧ����H=____________ (�ú���H1����H2����H3�Ĵ���ʽ��ʾ)��
(2)��2L�ĺ����ܱ������г���0.1molC2H6(g)��0.1molCO2(g)������(1)�з�Ӧ��C2H6(g)��ƽ��ת����[a(C2H6)]���¶�(T)�Ĺ�ϵ��ͼ��ʾ��
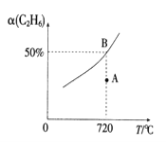
������Ӧ�¶��£�A��ķ�Ӧ��v(��)____v(��)(����>������<������=��)��
���������Ǹ���Ӧ�ķ�����Ϊ�����(C2H6)�����˽������Pʱ����ϵ�з�������⣬���ɲ�ȡ�Ĵ�ʩ��___________(��дһ��)��
��.�����Ϊ2L���ܱ������У��������»�ѧ��Ӧ��CO2(g)+H2(g)![]() CO(g)+H2O(g)���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���ʾ��
CO(g)+H2O(g)���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���ʾ��
T/�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)�÷�ӦΪ_________��Ӧ(��������������������)��ԭ��Ϊ_________________��
(4)830���£����������зֱ����2molH2��2molCO2��10s��ﵽƽ�⣬�����ʱ����v(H2)=________��ת������(CO2)=___________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com