
����Ŀ��ijͬѧ�������ʵ�鷽�����Է���KCl��BaCl2���ֹ�������Իش��������⣺

��ѡ�Լ���Na2SO4��Һ��K2SO4��Һ��K2CO3��Һ������
(1)�����ٵ�������____________�������ڵ�������_____________��
(2)�Լ�a��____________������B��___________�����ѧʽ��
(3)�����Լ�b�������Ļ�ѧ��Ӧ����ʽΪ��______________________________________��
(4)�÷����ܷ�ﵽʵ��Ŀ�ģ�________�������ܣ�Ӧ��θĽ������ܣ����ʲ��ûش�_________��
(5)��Ҫ�ⶨԭ�������KCl��BaCl2����������������Ҫȷ���������������⣬���ٻ�Ҫ��õ�������_________��������
���𰸡��ܽ� ���� K2CO3 BaCl2 BaCO3+2HCl=BaCl2+H2O+CO2�� ���� ��Һ���й�����CO32-δ��ȥ��Ӧ����ϡ�����ȥ BaCl2
��������
����KCl��BaCl2���ֹ��������������ˮ��Ȼ��������K2CO3ʹBaCl2ת��Ϊ���������˺�����������������BaCl2��Һ�����������ᾧ�������ɵù���BaCl2��������������ҺΪKCl��K2CO3�Ļ���Ӧ�����������ɵ�KCl���Դ˽����⡣
����KCl��BaCl2���ֹ��������������ˮ��Ȼ��������K2CO3ʹBaCl2ת��Ϊ���������˺�����������������BaCl2��Һ�����������ᾧ�������ɵù���BaCl2��������������ҺΪKCl��K2CO3�Ļ���Ӧ�����������ɵ�KCl��
(1)�������ǽ������ܽ⣬�����Һ��������Ϊ���������ԵĹ����Һ��ķ��룬Ϊ���ˣ�
(2)�����ܽ��������K2CO3��Һ��ʹBaCl2ת��Ϊ������Ȼ����ˣ��õ�BaCO3�����������м������ᣬBaCO3�����ᷴӦ������BaCl2��Һ�����������ᾧ�������ɵù���BaCl2�������Լ�a��K2CO3������B��BaCl2��
(3)��BaCO3�м���HCl���������ֽⷴӦ����BaCl2��H2O��CO2���÷�Ӧ�Ļ�ѧ����ʽΪ��BaCO3+2HCl=BaCl2+H2O+CO2����
(4)��ҺΪKCl��K2CO3�Ļ���ֱ�ӽ�������Ũ���ᾧ����õľ���ΪKCl��K2CO3�Ļ�����˸÷������ܴﵽʵ��Ŀ�ģ��Ľ������ǣ������ᾧǰӦ��������ϡ���ᣬ��������̼���ת�����Ȼ��أ�
(5)�����ܽ��������K2CO3ʹBaCl2ת��Ϊ̼�ᱵ���������˺���������Լ�b����ɽ�̼�ᱵת����BaCl2��Һ��Ȼ���������ᾧ�������ɵù���BaCl2����Ҫ�ⶨԭ�������KCl��BaCl2����������������Ҫȷ���������������⣬���ٻ�Ҫ��õ������ǹ���B�����A1������������BΪBaCl2����õ�����������A1Ϊ̼�ᱵ����ϱ�Ԫ���غ�����Ȼ��������õ���


 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л���˵����ȷ���ǣ� ��
A.ҽ�������ƾ���Ũ��Ϊ95%
B.��������Ԫ������ɫ
C.���ࡢ��֬�������ʶ��Ǹ߷��ӻ�����
D.������ˮ������ղ���Ϊ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ֳּ����ǻ������ݲɼ������������Ͷ�ý���������ɵ�һ��������������ϵͳ������ʵʱ��������ֱ�۵��ص㣬��ͼ�������ֳּ����õ��������ʵ����仯ͼ����������20ml0.2mol/LH2A��Һ�еμ�0.2mol/LNaOH��Һ������˵����ȷ���ǣ�������

A. H2A��ˮ�еĵ��뷽��ʽ�ǣ�H2A = 2H+ + A2-
B. ��V(NaOH)=20mLʱ�����У�c(Na+)��c(HA-)��c(H+)��c(A2-)��c(OH-)
C. ��V(NaOH)=30mLʱ�����У�2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2c(OH-)
D. ��V(NaOH)=40mLʱ������Һ��ˮ�ĵ����ܵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���淴Ӧ��mA(g)+nB(g) ![]() pC(g) ��H ���ܱ������н��У���ͼ��ʾ����Ӧ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B�ڻ�������еİٷֺ�����B%���Ĺ�ϵ���ߣ������߷��������ж���ȷ���ǣ� ��
pC(g) ��H ���ܱ������н��У���ͼ��ʾ����Ӧ�ڲ�ͬʱ��t���¶�T��ѹǿP�뷴Ӧ��B�ڻ�������еİٷֺ�����B%���Ĺ�ϵ���ߣ������߷��������ж���ȷ���ǣ� ��

A. T1<T2��P1>P2��m+n>p����H>0
B. T1>T2��P1<P2��m+n>p����H>0
C. T1>T2��P1<P2��m+n<p����H<0
D. T1>T2��P1>P2��m+n>p����H>0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ԭ�ӵ�������ag,12Cԭ�ӵ�������bg����NAֻ��ʾ�����ӵ���������ֵ��������˵������ȷ����( )
�ٸ���ԭ�ӵ����ԭ������Ϊ![]() ��mg����ԭ�ӵ����ʵ���Ϊ
��mg����ԭ�ӵ����ʵ���Ϊ![]() mol
mol
�۸���ԭ�ӵ�Ħ��������aNA g ��ag����ԭ�������ĵ�����Ϊ16NA
A. �٢� B. �ڢ� C. �٢� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������أ���ǵ��ͨ;��������Ŀ�ĸ���Ĵ�����2018��10��23����ʽͨ�����������ҹ����̽���������������ʵ�ִ��Խ���������²����о��������ش�ͻ�ƣ��ش��������⣺
��1������һ�����˵Ľṹ���ϣ��ȸ��ᡢ����Ӳ��
�ٻ�̬��ԭ�ӵļ۵����Ų�ʽΪ______������ͬ���ڵ�Ԫ���У���̬ԭ�ӵ�δ�ɶԵ�����������ͬ����_____��
���ѵ�Ӳ�ȱ������ԭ����_______________________________��
�۹�ҵ���ƽ����Ѳ��ý�����ԭ�������ѡ��Ƚ�TiO2������̿�ۻ�ϼ�����1000��1100K�����Ȼ�����������TiCl4���÷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ_______________________��
��2���纣��������Ҫ�ṹ����Ϊ������������������Bipy���ṹ��ͼ���γɶ�������

��1mol Bipy������![]() ��_____mol��̼ԭ���ӻ���ʽ��___________________��
��_____mol��̼ԭ���ӻ���ʽ��___________________��
��Bipy�ķе�Ϊ260�����ṹ�������������������ӽ��Ļ����ϩ���ṹ����ͼ���ķе�Ϊ42��5����ǰ�߽ϴ��ԭ����______________________________��
��3��̼������������ĥ���ϡ���ͼΪ������IJ��ֽṹ��̼ԭ��Ƕ������ľ����϶�������ƻ�ԭ�н����ľ����γ���϶�������塢Ҳ��Ϊ��϶�����

���ڸýṹ�У�ÿ����ԭ����Χ������ԭ�������̼ԭ����____����
�ڼ���ò��־�������Ϊd/cm3��̼����Ħ������ΪMg��mol���ܶ�Ϊdg��cm3�����ӵ�����NA���������ݱ�ʾΪ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������(FeC2O4��2H2O����Է�������Ϊ180)�ʵ���ɫ��������������Ӱ����ijʵ��С����������һϵ��̽����
I.�����������������ȷֽ�����̽����
(1)�������ɷֵ�̽����С���Ա��������װ��(���ظ�ѡ��)����ʵ�飺

��װ��D������Ϊ___________��
�ڰ������������ҵķ�������װ�õ�����˳��Ϊ___________��β������װ��(�������ӿڵ���ĸ���)��
��ʵ��ǰ��ͨ��һ��ʱ��N2����Ŀ��Ϊ______________________��
��ʵ��֤������������к���CO�����ݵ�ʵ������Ϊ______________________��
(2)�������ɷֵ�̽������ַ�Ӧ��A����Ӧ���в�����ɫ���塣�������Ͽ�֪����ɫ�������ΪFe��FeO��С���Ա���ʵ��֤������ɷ�ֻ��FeO�������������Ϊ___________��
(3)����(1)��(2)���ۣ���֪A����Ӧ���з�����Ӧ�Ļ�ѧ����ʽΪ___________��
��.��������������Ʒ���ȵIJⶨ
��ҵ�ƵõIJ������������г�����FeSO4���ʣ��ⶨ�䴿�ȵIJ������£�
����1����ȡm g��������������Ʒ������ϡH2SO4�У����250mL��Һ��
����2��ȡ������Һ25.00mL����c mol�� L ��1KMnO4��Һ�ζ����յ㣬���ı�ҺV1mL��
����3����Ӧ����Һ�м�������п�ۣ���ַ�Ӧ��������ϡH2SO4������cmol��L��1KMnO4����Һ�ζ����յ㣬���ı�ҺV2mL��
(4)����3�м���п�۵�Ŀ��Ϊ____________________________________________��
(5)��������������Ʒ�Ĵ���Ϊ____________________________________________��������1������Һʱ����Fe2+����������ⶨ�����___________(�ƫ�ߡ�����ƫ�͡����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ�����мס�������Ԫ��Ũ�ȱ仯��ijֲ���������ʵĹ�ϵ�����з�����ȷ����(����)

A.��ֲ�������Լ�Ԫ�ص����������Ԫ��
B.����������Ԫ��Ũ��ΪBʱ��ʩ����Ԫ�صķ����������ڸ�ֲ������
C.����ֲ�������������ʱ���Լס���Ԫ�ص����������
D.�������ּס���Ԫ�ع�Ӧ����ȿ��ܻᵼ�¸�ֲ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й����л��������˵����ȷ����
A. �������Ȼ�߷��ӻ���������ṹ�Ƚϸ���
B. ���������Ը��i�����Һ����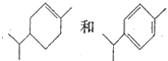
C. �������Ϊ90%���Ҵ���Һ��ʹ�����ʱ��ԣ�������ҽ������
D. �ױ���һ������2һ�������һ����ﶼ��4��(�����������칹)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com