
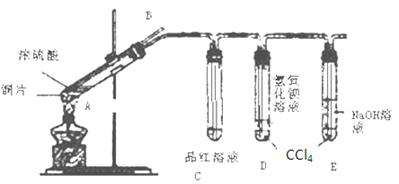
| 物质 | 溶解度(g/100水) | 物质 | 溶解度(g/100水) |
| Ca(OH)2 | 0.173 | Ba(OH)2 | 3.89 |
| CaCO3 | 0.0013 | BaSO3 | 0.016 |
| Ca(HCO3)2 | 16.60 | | |
| 实验方案 | 现象 |
| 方案1:取少量溶液于试管中,加入稀盐酸,加热,用①检验产生的气体。 | ② |
| 方案2:取少量溶液于试管中,加入③ 溶液并观察现象。 | ④ |
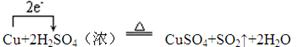 (或双线桥法)
(或双线桥法)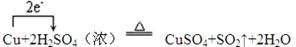 。
。

 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.②③④ | C.全部 | D.①③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
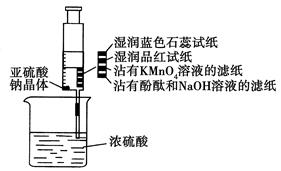
| A.蓝色石蕊试纸先变红后褪色 |
| B.沾有KMnO4溶液的滤纸褪色,证明了SO2的漂白性 |
| C.品红试纸褪色,证明了SO2的漂白性 |
| D.沾有酚酞和NaOH溶液的滤纸褪色,证明了SO2的漂白性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下都能用铝容器贮存 | B.露置在空气中,容器内酸液的质量都增加 |
| C.常温下都能与铜较快反应 | D.露置在空气中,容器内酸液的质量都减少 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.大于14NA | B.等于14NA | C.小于14NA | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
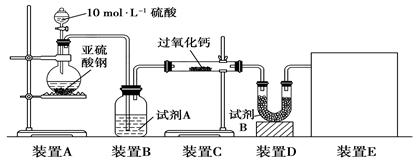
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
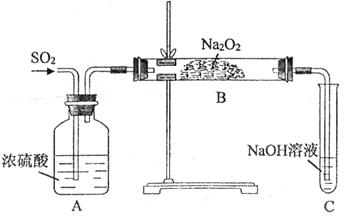
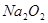 和
和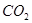 的反应,用类比的方法推理
的反应,用类比的方法推理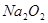 与
与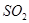 反应的固体产物为__________。另一部分同学依据
反应的固体产物为__________。另一部分同学依据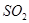 的强还原性和
的强还原性和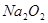 的强氧化性,猜想产物中含有
的强氧化性,猜想产物中含有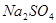 。为检验生成物中是否存在
。为检验生成物中是否存在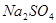 ,他们设计了如下实验方案:
,他们设计了如下实验方案: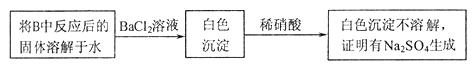
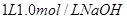 溶液中缓慢通入
溶液中缓慢通入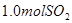 气体,请分析通入
气体,请分析通入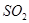 物质的量与溶液中溶质组成的关系,填写下表空格。
物质的量与溶液中溶质组成的关系,填写下表空格。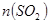 的范围 的范围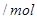 | 溶液中溶质的化学式 |
| (0,0.5) | __________ |
| __________ | 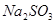 、 、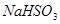 |
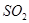 物质的量的变化曲线。(作图时请在起点、拐点和终点注明坐标)
物质的量的变化曲线。(作图时请在起点、拐点和终点注明坐标)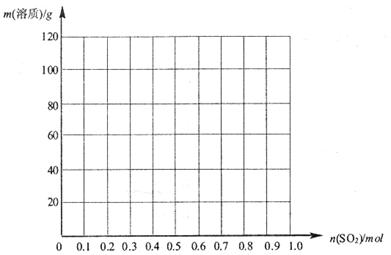
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 现 象 | 解 释 |
| A | 浓HNO3在光照条件下变黄 | 浓硝酸不稳定,分解产生NO2能溶于浓硝酸 |
| B | KI淀粉溶液中通入Cl2,溶液变蓝 | Cl2能与淀粉发生显色反应 |
| C | 某溶液中加入HNO3酸化的Ba(NO3)2溶液,有白色沉淀生成 | 说明该溶液中含有SO42- |
| D | 向盐酸中加入浓硫酸时产生白雾 | 说明浓硫酸具有脱水性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com